Estrutura de iodeto de sódio (NAI), propriedades, usos, riscos

- 2783
- 792
- Alfred Kub
Ele iodeto de sódio É um composto inorgânico formado por um átomo de Na NA de sódio e um átomo de iodo. Sua fórmula química é NAI. É um sólido branco que tende a absorver a água do meio ambiente, ou seja, é higroscópico. Tão higroscópico que se diz que é delicado, porque quando o tempo passa, é dissolvido na água que absorveu.
O iodeto de sódio tem várias aplicações na área de medicina, por exemplo, serve para tornar as secreções brônquicas menos grossas (muco), por isso é usado para tratar bronquite e asma.
 Iodeto sólido de sódio nai. Nenhum autor legível por máquina fornecido. Walkerma assumiu (com base em reivindicações de direitos autorais). [Domínio público]. Fonte: Wikimedia Commons.
Iodeto sólido de sódio nai. Nenhum autor legível por máquina fornecido. Walkerma assumiu (com base em reivindicações de direitos autorais). [Domínio público]. Fonte: Wikimedia Commons. Como o elemento iodo é um micronutriente para o corpo, o iodeto de sódio nai é usado nas soluções que são injetadas em pacientes que não podem ser alimentados pela boca. Também é usado em determinados dispositivos que servem para detectar doenças através da radiação gama.
Tem um uso importante na medicina veterinária para tratar várias doenças em animais, principalmente mamíferos. NAI também é usado como reagente em laboratórios de química orgânica.
[TOC]
Estrutura
O iodeto de sódio é formado por um cátion de sódio+ e um ânion de iodeto eu-, Portanto, é um composto iônico.
 Yoduro ânion i- (grande) e cátion de sódio na+ (pequeno). Claudio Pistilli [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons.
Yoduro ânion i- (grande) e cátion de sódio na+ (pequeno). Claudio Pistilli [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons. O íons iodeto é muito maior que o íon de sódio, no entanto, no sólido, eles são perfeitamente acoplados, formando cristais cúbicos.
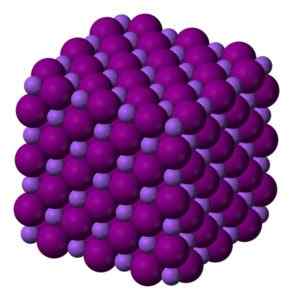 No vidro nai sólido, os íons de sódio e iodeto são perfeitamente acoplados e formam um vidro cúbico. Benjah-BMM27 [domínio público]. Fonte: Wikimedia Commons.
No vidro nai sólido, os íons de sódio e iodeto são perfeitamente acoplados e formam um vidro cúbico. Benjah-BMM27 [domínio público]. Fonte: Wikimedia Commons. Nomenclatura
Iodeto de sódio
Propriedades
Estado físico
Sólido branco de cristais delicados (absorve a água rapidamente do meio ambiente). Cristais cúbicos.
Peso molecular
149,89 g/mol
Pode atendê -lo: Justus von LiebigPonto de fusão
661 ° C
Ponto de ebulição
1304 ° C
Densidade
3,67 g/cm3
Solubilidade
Muito solúvel em água: 184 g/100 ml de água a 25 ° C. Álcool solúvel: 42,57 g/100 ml de álcool. Acetona solúvel: 39,9 g/100 ml de acetona.
ph
8-9.5 (é preparado ligeiramente alcalino para ser mais estável).
Propriedades quimicas
Torna -se marrom se for exposto ao ar, pois libera iodo i2. Suas soluções aquosas são igualmente afetadas.
O iodeto de sódio nai reage com agentes oxidantes que produzem iodo I2. Com agentes oxidantes muito fortes, como o ácido perclórico, a reação pode ser violenta.
Outras propriedades
É delicado, ou seja, muito higroscópico. Absorver rapidamente a umidade ambiental. Pode absorver até 5% do seu peso à água.
Sabor salino e um pouco amargo.
Obtenção
O iodeto de sódio pode ser obtido do iodo I2 Hidróxido de sódio NaOH. Também pode ser preparado por reação entre carbonato de sódio e uma solução de iodeto ácido.
Usos na medicina
Para tratamento de asma e bronquite
O NAI é usado como expectorante quando há secreções brônquicas muito tenazes, serve para liquef.
 Os brônquios são a parte ramificada dos pulmões. Em alguns casos, a bronquite pode ser tratada com iodeto de sódio. Autor: OpenClipart-Vectors. Fonte: Pixabay.
Os brônquios são a parte ramificada dos pulmões. Em alguns casos, a bronquite pode ser tratada com iodeto de sódio. Autor: OpenClipart-Vectors. Fonte: Pixabay. É usado em bronquite e asma. Não deve ser administrado depois que a tosse "solta". Mas em pacientes com bronquite crônica ou asma, ela pode ser prescrita mais ou menos continuamente se for alcançado alívio.
Em comida intravenosa
O iodeto de sódio é uma fonte de iodo e pode ser fornecido como um suplemento para a nutrição parenteral total, que é um tipo de alimento intravenoso.
No diagnóstico e tratamento da tireóide
Em sua forma radioativa, a NAI tem sido usada como uma ferramenta de diagnóstico para avaliar a função e a estrutura da tireóide de alguns pacientes.
Pode atendê -lo: tabela periódica, para que éA terapia com iodeto de sódio tem sido usada para tratar hipertireoidismo, mas geralmente não controla completamente as manifestações da doença e depois de um tempo seu efeito benéfico desaparece.
Ao continuar o tratamento com iodeto, o hipertireoidismo pode retornar à sua intensidade inicial ou se tornar mais grave do que no começo.
Em câmeras gama
Câmeras gama são instrumentos que permitem capturar imagens derivadas da radiação gama. Eles são usados em medicina nuclear para o diagnóstico de algumas doenças.
A câmara gama usa um cristal de iodeto de sódio como um detector de radiação gama do paciente, que foi injetado por via intravenosa uma quantidade muito pequena de uma substância radioativa.
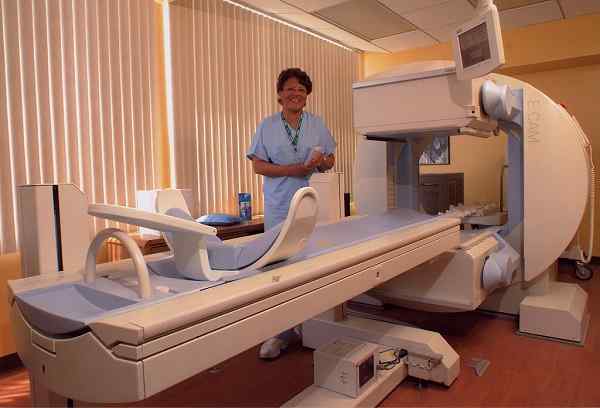 Equipamento de câmera gama, que permite detectar certas doenças através da radiação gama. Brendaicm [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikimedia Commons.
Equipamento de câmera gama, que permite detectar certas doenças através da radiação gama. Brendaicm [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikimedia Commons. Em medicina veterinária
Na medicina veterinária, tem sido usado para eliminar vermes anelados, lesões cancerígenas e em certas doenças inflamatórias nos cães de cães.
É usado para tratar a micose, inflamações crônicas das articulações, laringite, bronquite e pleurite em algumas espécies de animais. É usado para remover vermes de gatos de gatos.
 Algumas doenças de gatos podem ser tratadas com iodeto de sódio. Autor: espeto. Fonte: Pixabay.
Algumas doenças de gatos podem ser tratadas com iodeto de sódio. Autor: espeto. Fonte: Pixabay. Também é usado como meio de raios X de bexiga de alguns animais.
O iodeto de sódio é usado como ajuda no tratamento da actinomicose e actinobacilose em gado (pode ser em vacas, ovelhas e cabras).
Actinomicose ou "mandíbula de borracha" é uma infecção dos ossos da mandíbula, nos quais os ossos aumentam de tamanho, causam dor e o animal não pode ser alimentado corretamente.
Actinobacilosis ou "língua de madeira" é uma infecção na língua que incha e o animal não pode mastigar comida.
Pode servir você: ácido sulfúrico (H2SO4)O iodeto de sódio contribui com outros medicamentos para curar as duas doenças.
O iodeto de sódio também é usado como expectorante em doenças de vacas, cavalos e ovelhas.
 Algumas doenças que afetam as vacas podem ser tratadas com iodeto de sódio NAI. Autor: Ulrike Leone. Fonte: Pixabay.
Algumas doenças que afetam as vacas podem ser tratadas com iodeto de sódio NAI. Autor: Ulrike Leone. Fonte: Pixabay. Outros usos
Em reações químicas orgânicas
O iodeto de sódio foi um dos primeiros sais usados para despida.
Para extrair microplásticos de areia contaminados
O iodeto de sódio tem sido usado para extrair microplásticos (pedaços de plástico muito pequenos) de areia contaminada com este material.
A poluição microplástica foi observada em vários ambientes naturais, como rios, lagos, mares, oceanos, costas e até em ambientes submarinos, por isso é uma preocupação global.
Os microplásticos são ingeridos por animais marinhos e terrestres, causando sérios danos à saúde.
 Os plásticos descartados nas praias levam à alta poluição da areia e do mar. Com iodeto de sódio, você pode medir quanta microplástica existem na areia. Autor: h. Hach. Fonte: Pixabay.
Os plásticos descartados nas praias levam à alta poluição da areia e do mar. Com iodeto de sódio, você pode medir quanta microplástica existem na areia. Autor: h. Hach. Fonte: Pixabay. A medida da quantidade de microplásticos que uma determinada área possui é realizada pegando uma parte da areia e imergindo -a na solução de iodeto de sódio.
Dessa maneira, o microplástico flutuará. As soluções de iodeto de sódio têm densidade adequada para micropartículas plásticas para flutuar, mesmo o plástico mais denso.
Embora o iodeto de sódio seja caro, os métodos estão sendo criados para reutilizar e reduzir os custos deste procedimento.
Riscos
Se o iodeto de sódio entrar em contato com o ácido perclorico HCLO4.
É irritante para olhos, pele e trato respiratório. Ingerido pode afetar a tireóide. Pode causar sensibilização no corpo.
É prejudicial aos fetos de mulheres grávidas, porque se elas a ingerir ou inalar, podem causar morte ao bebê ou danos muito graves e permanentes.
A overdose de iodeto de sódio pode causar "iodismo" caracterizado por excesso de saliva, espirros, conjuntivite, dor de cabeça, febre, laringite, entre outros sintomas.
Referências
- OU.S. Biblioteca Nacional de Medicina. (2019). Iodeto de sódio. Centro Nacional de Informações sobre Biotecnologia. Recuperado de PubChem.NCBI.Nlm.NIH.Gov.
- Cherry, s.R. et al. (2012). A câmera gama. Em física em medicina nuclear (quarta edição). Recuperado de cientedirect.com.
- Kedzierski, m. et al. (2016). Extração de microplásticos eficientes da areia. Uma metodologia econômica baseada na reciclagem de iodeto de sódio. Boletim de Poluição Marinha 2016, recuperado de Elsevier.com.
- Van medidor, D.C. et al. (2008). Doenças infecciosas do trato gastrointestinal. Em Desses de Catinho de Laticínios de Rebeun. Recuperado de cientedirect.com.
- Fry, a.J. (1991). Redução. Na compreensão da síntese orgânica. Recuperado de cientedirect.com.
- Jovem, j.PARA. (2004). Iodeto de sódio. Journal of Chemical Education, vol. 81, não. 3 de março de 2004. Recuperado de bares.ACS.org.
- « Estrutura de silicato de sódio (Na2SIO3), propriedades, usos, riscos
- Perímetro do círculo Como tirá -lo e fórmulas, exercícios resolvidos »

