Estrutura de silicato de sódio (Na2SIO3), propriedades, usos, riscos

- 1487
- 220
- Alfred Kub
Ele silicato de sódio É um composto inorgânico formado por dois íons de ná de sódio+ e um ânion Siio Silicato32-. Diz -se também que é formado por uma molécula de sílica sio2 e um de óxido de sódio na2QUALQUER. Sua fórmula química pode ser expressa como NA2SiO3 ou também na2QUALQUER.SiO2.
No entanto, a composição do silicato de sódio pode variar dependendo do relacionamento SIO2/N / D2Ou em peso ou toupeiras. É também chamado de silicato solúvel ou vidro solúvel. Pode ser obtido em poeira, peças grandes semelhantes a cristais ou na forma de soluções.
 Silicato de sódio Na2SiO3 sólido. Ondřej Mangl [Domínio Público]. Fonte: Wikimedia Commons.
Silicato de sódio Na2SiO3 sólido. Ondřej Mangl [Domínio Público]. Fonte: Wikimedia Commons. O silicato de sódio tem amplo uso em detergentes e sabonetes, porque permite amolecer a água, tornando a limpeza mais eficaz. Também faz parte de produtos como o creme de barbear.
É a matéria -prima para preparar catalisadores de sílica SIIO2. Suas soluções são usadas como cola em muitas aplicações, variando de papel adesivo e papelão, vidro, porcelana, moldes refratários, cimento e discos abrasivos.
Sendo um material completamente não combustível, é usado para fabricar tecidos à prova de fogo, pois é um retardador de incêndio e como revestimento de equipamentos de proteção.
[TOC]
Estrutura
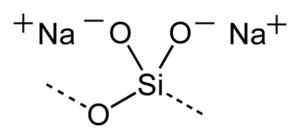 Estrutura simplificada de polímeros em soluções de silicato de sódio. Benjah-BMM27 [domínio público]. Fonte: Wikimedia Commons.
Estrutura simplificada de polímeros em soluções de silicato de sódio. Benjah-BMM27 [domínio público]. Fonte: Wikimedia Commons. A fórmula geral de silicatos de sódio é xsio2/N / D2Ou onde x é motivo ou peso molar.
Razão molar significa número de moles de Sio2 dividido pelo número de moles de na2QUALQUER. Razão no peso significa peso SIO2 Dividido entre o peso de NA2QUALQUER.
Adicionando mais álcalis (NA2O) A razão molar ou peso é alterada.
Uma solução de silicato de sódio com uma razão molar baixa, por exemplo, 1/1 (1 mol de Sio2 e 1 mol de Na2O) contém principalmente monômeros SIO44- e dímeros s2QUALQUER52- Além dos íons Na+.
Uma solução com uma alta proporção molar, como 3,3/1 (3,3 moles de Sio2 Para cada mol de Na2O) Tem uma alta proporção de espécies poliméricas ou silício e polímeros de oxigênio.
Pode atendê -lo: o que é o erristenoo?Nomenclatura
-Silicato de sódio
-Gestilicato de sódio
-Vidro solúvel
-Vidro de água (inglês Copo de água)
-Silicato solúvel
Propriedades
Estado físico
-Sólido em pedaços grandes como cristais verdes azuis
-Incolor para pó branco
-Soluções aquosas incolores.
Peso molecular
Da fórmula NA2SiO3: 122.063 g/mol.
Ponto de fusão
N / D2SiO3: 1089 ° C
Densidade
Depende do relacionamento SIO2/N / D2QUALQUER.
Solubilidade
Quando está na forma de grandes pedaços de vidro esverdeado, é solúvel em água se for aquecido e sob alta pressão. A poeira é um pouco mais solúvel, mas em ambos os casos sua solubilidade depende da quantidade de sódio ou NA2Ou o que possui.
Quanto maior o teor de sódio (na forma de um Na2O) mais rápido se dissolve.
ph
Suas soluções aquosas são fortemente alcalinas.
Propriedades quimicas
Se prepara comercialmente nas relações SIO2/N / D2Ou em peso variando de 1,5 a 3,3. À medida que o SIO aumenta2 No relacionamento, a solubilidade na água e na alcalinidade diminui.
Ao dissolver o silicato sólido na água, misturas gelatinosas ou muito viscosas podem ser formadas.
O pó de silicato de sódio pode ser delicioso, ou seja, se tiver uma grande quantidade de NA2Ou tende a absorver facilmente o ambiente do ambiente.
Se o pH de suas soluções for reduzido pela adição de ácido, um gel é formado.
Outras propriedades
Não é inflamável.
Obtenção
Para obter silicatos de sódio, a areia de sílica sio é baseada2 Com carbonato de sódio na2Co3 Anidro em um forno aberto. A razão molar de areia para carbonato de sódio pode variar comercialmente de 0,5 a 3,75.
 Depósitos de areia de sílica em uma área da Índia. ರವಿಮುಂ [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons.
Depósitos de areia de sílica em uma área da Índia. ರವಿಮುಂ [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons. Formulários
Em sabonetes e detergentes
Os silicatos de sódio estão entre os primeiros compostos que foram usados em formulações de detergentes.
 Os detergentes geralmente contêm silicato de sódio em sua composição. Autor: Karunasanghvi. Fonte: Pixabay.
Os detergentes geralmente contêm silicato de sódio em sua composição. Autor: Karunasanghvi. Fonte: Pixabay. Silicato de sódio seqüestros de cálcio caíions de cálcio2+ e magnésio mg2+, eliminando o que é chamado de dureza da água, ou seja, amolecendo -a. Ao fazer isso, precipitados insolúveis são formados, por isso é usado em pequenas quantidades.
Pode atendê -lo: células eletrolíticasA ação do silicato de sódio permite que o detergente funcione sem os íons mencionados que afetam o processo de limpeza.
Em catalisadores e géis de sílica
Os géis de sílica geralmente preparam uma solução de silicato de sódio a pH menor que 10 ou 11. O tempo necessário para gelificar varia.
 Gel de sílica. Para prepará -lo, o silicato de sódio é necessário. Desiclantes [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikimedia Commons.
Gel de sílica. Para prepará -lo, o silicato de sódio é necessário. Desiclantes [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikimedia Commons. A sílica pode ser preparada misturando o silicato de sódio com um forte ácido mineral. O silicato de sódio é usado em bases de fabricação para catalisadores, pois é a fonte de sílica sio2.
Como adesivo ou cola
Soluções aquosas concentradas de silicato de sódio são usadas como adesivos e selantes. Eles podem manter temperaturas até 1100 ° C.
As principais aplicações da cola de silicato de sódio estão em papel adesivo, papelão ondulado ou ondulado, caixas e papelão. Também para colar ou aglomerar madeira ou aderir metal a vários tipos de materiais.
 O papelão ondulado ou corrugado é fabricado usando cola de silicato de sódio. Autor: Stux. Fonte: Pixabay.
O papelão ondulado ou corrugado é fabricado usando cola de silicato de sódio. Autor: Stux. Fonte: Pixabay. Serve para colar vidro, porcelana, cerâmica, têxteis, couro, etc. Para se juntar aos recipientes de vidro à prova de fibra de vidro, vidro óptico e de impacto.
Ele permite preparar cimentos refratários para construir tanques, chaleiras, fornos e moldes para fundição de metal, bem como fazer morteiros ou cimentos para impermeabilizados ou ácidos à prova de ácido.
Os silicatos de sódio podem reagir com fluoretos de silício para produzir cimentos resistentes ao ácido, com baixa tendência à contração e uma expansão térmica semelhante à do aço.
Eles também são usados para fazer cimentos para discos abrasivos usados para polir.
Em fluidos de perfuração de petróleo
O silicato de sódio tem sido usado por muitos anos como rejunte química durante a perfuração de certos tipos de formações com permeabilidade muito alta, como as que são constituídas por areia.
Alta permeabilidade significa que permite que os líquidos passem facilmente.
Pode atendê -lo: compostos orgânicosÉ adicionado junto com um composto que ativa o silicato para formar um polímero. Este polímero fornece força, rigidez e reduz a permeabilidade em solos granulares.
Sendo o solo menos permeável, o líquido não passa livremente e dessa maneira a perda de fluido é evitada durante a fase de perfuração do poço.
 Poço de petróleo. Petróleo_RIG_NT8.JPG: *Trabalho derivado: Mudgineer (Talk) OIL_RIG_NT.PNG: Trabalho de Tosakaderivative: Malyszkz [CC por 3.0 (https: // CreativeCommons.Org/licenças/por/3.0)]. Fonte: Wikimedia Commons.
Poço de petróleo. Petróleo_RIG_NT8.JPG: *Trabalho derivado: Mudgineer (Talk) OIL_RIG_NT.PNG: Trabalho de Tosakaderivative: Malyszkz [CC por 3.0 (https: // CreativeCommons.Org/licenças/por/3.0)]. Fonte: Wikimedia Commons. Em várias aplicações
Silicato de sódio também tem uma variedade de usos. Alguns são mencionados abaixo.
-Nos produtos de cuidados diários, por exemplo, é um componente de cremes de barbear.
-No tratamento de água.
-No branqueamento de têxteis como lã.
-Em branqueamento de polpa de papel. Por exemplo, para branquear madeira moída, uma mistura contém peróxido de hidrogênio e silicato de sódio, entre outros ingredientes, entre outros ingredientes. O silicato de sódio é usado para sequestrar íons metálicos, que tendem a acelerar a decomposição do peróxido.
-Para a fabricação de tecidos à prova de fogo. Como retardador de incêndio e como revestimento de equipamentos de proteção.
-Em pigmentos de sílica.
-Para detectar grãos de milho infestados por insetos. Uma mistura de silicato de sódio e água é usada onde os grãos infestados flutuam na superfície rapidamente.
-Em eletrodeposição de zinco.
-Para limpar metais.
-Na flotação mineral, é usado como um lodo e dispersante de lodo e como condicionador da superfície mineral.
-Impregnar madeira.
Riscos
Silicato de sódio para seu alto teor alcalino é uma forte pele irritante, olhos e membranas mucosas. Se ingerido, pode ser tóxico e irritar as membranas mucosas semelhantes às soluções de refrigerante cáustica.
Deve ser armazenado separadamente de ácidos fortes, metais e halogênios, como o flúor, com o qual reage violentamente.
Referências
- Ebnejjad, s. (2015). Características de materiais adesivos. Silicatos solúveis (potássio e silicato de sódio). No manual de adesivos e preparação da superfície. Recuperado de cientedirect.com.
- Fink, j.K. (2012). Aditivos de perda de fluidos. Metassilicato de sódio. No Guia do Engenheiro de Petróleo para Químicos e Fluidos do Campo de Petróleo (Segunda Edição). Recuperado de cientedirect.com.
- OU.S. Biblioteca Nacional de Medicina. (2019). Silicato de sódio. Centro Nacional de Informações sobre Biotecnologia. Recuperado de PubChem.NCBI.Nlm.NIH.Gov.
- Kirk-Othmer. (1984). Enciclopédia de tecnologia química, 3ª ed., John Wiley e Sons.
- Maeda, k. et al. (2007). De zeólitos a materiais porosos de MOF - os 40º Aniversário da Conferência Internacional de Zeólito. Em estudos em ciência da superfície e catálise. Recuperado de cientedirect.com.
- Chopade, s.P. E Nagarajan, K. (2000). Formulações de detergente: troca de íons. Na enciclopédia da ciência da separação. Recuperado de cientedirect.com.
- Garcia-lodeiro, i. et al. (2015). Insights cruciais sobre o design da mistura de ligantes à base de cimento ativados por alcalinismo. Efeito de silicatos: grau de polimerização solúvel de silicato. No manual de cimento alcalini, morteiros e concretos ativados. Recuperado de cientedirect.com.
- « História da luz, natureza, comportamento, propagação
- Estrutura de iodeto de sódio (NAI), propriedades, usos, riscos »

