Força de coesão
- 921
- 269
- Ernesto Bruen
O que são forças de coesão?
As Forças de coesão São as forças de atração intermoleculares que mantêm algumas moléculas com outras. Dependendo da intensidade das forças de coesão, uma substância está em estado sólido, líquido ou gasoso. O valor das forças de coesão é uma propriedade intrínseca de cada substância.
Esta propriedade está relacionada à forma e estrutura das moléculas de cada substância. Uma característica importante das forças de coesão é que elas diminuem rapidamente quando a distância aumenta. Então, eles são chamados forças de coesão para as forças de atração que ocorrem entre as moléculas da mesma substância.
As Forças de repulsão Eles são aqueles que resultam da energia cinética (energia devido ao movimento) de partículas. Esta energia faz com que as moléculas estejam constantemente em movimento. A intensidade desse movimento é diretamente proporcional à temperatura em que a substância é.
Para causar a mudança de status de uma substância, é necessário aumentar sua temperatura por meio de transmissão de calor. Isso faz com que as forças de repulsão da substância aumentem, que, se aplicável, pode acabar assumindo a mudança de estado.
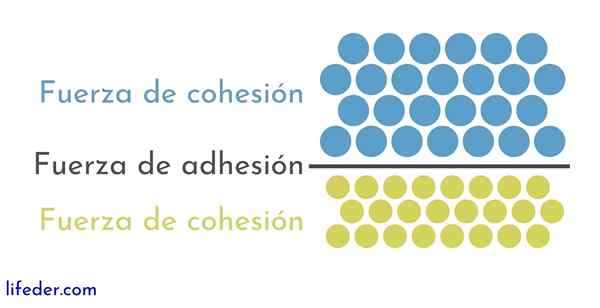
Por outro lado, é importante e necessário distinguir entre coesão e adesão:
- A coesão se deve às forças de atração entre partículas adjacentes da mesma substância.
- A adesão é o resultado da interação que ocorre entre superfícies de diferentes substâncias ou corpos.
Essas duas forças parecem relacionadas a vários fenômenos físicos que afetam líquidos, por isso é importante uma boa compreensão de um e outro.
Pode atendê -lo: Vy Canis majoris: descoberta, características, estrutura, treinamento e evoluçãoForças de coesão em sólidos, líquidos e gases
 Átomos nos três principais estados da matéria
Átomos nos três principais estados da matéria Em sólidos
Em geral, nas forças de coesão de sólidos, são muito altas e são dadas intensamente nas três direções do espaço.
Dessa maneira, se uma força externa for aplicada a um corpo sólido, pequenos deslocamentos das moléculas ocorrem entre si.
Além disso, quando a força externa desaparece, as forças de coesão são fortes o suficiente para retornar às moléculas em sua posição original, recuperando a posição antes da aplicação da força.
Em líquidos
Pelo contrário, nas forças de coesão líquidas são altas apenas em duas das direções espaciais, enquanto são muito fracas entre as camadas fluidas.
Assim, quando uma força é aplicada em uma direção tangencial em um líquido, essa força quebra os laços fracos entre as camadas. Isso faz com que as camadas líquidas escorreguem sobre o outro.
Então, quando a aplicação da força conclui, as forças de coesão não têm força suficiente para re -colocar as moléculas líquidas em sua posição original.
Além disso, em líquidos, a coesão também se reflete na tensão da superfície, causada por uma força desequilibrada direcionada para o interior do líquido, agindo nas moléculas da superfície.
Da mesma forma, a coesão também é observada quando a transição do estado líquido para o estado sólido é dado, devido ao efeito da compressão de moléculas líquidas.
Em gases
Nos gases, as forças de coesão são desprezíveis. Dessa forma, as moléculas Gase estão em movimento constante, pois, no caso deles, as forças de coesão são incapazes de mantê -las ligadas entre si.
Pode servir a você: vantagem mecânica: fórmula, equações, cálculo e exemplosPortanto, nos gases, as forças de coesão só podem ser vistas quando ocorre o processo de liquefação, que ocorre quando as moléculas gasosas são compactadas e as forças de atração são fortes o suficiente para produzir a transição do estado do estado para o estado líquido.
Exemplos de forças de coesão
Freqüentemente, as forças de coesão são combinadas com as forças de adesão para dar origem a certos fenômenos físicos e químicos.
Por exemplo, as forças de coesão, juntamente com as da adesão, permitem explicar alguns dos fenômenos mais comuns que ocorrem em líquidos; Este é o caso de menisco, tensão superficial e capilaridade.
Portanto, no caso de líquidos, é necessário distinguir entre as forças de coesão, que ocorrem entre as moléculas do mesmo líquido; e os da adesão, que ocorrem entre as moléculas do líquido e o sólido.
Tensão superficial

A tensão superficial é a força que ocorre tangencialmente e por unidade de comprimento na borda da superfície livre de um líquido que está em equilíbrio. Esta força contrai a superfície líquida.
Por fim, a tensão superficial ocorre porque as forças que ocorrem nas moléculas líquidas são diferentes na superfície do líquido do que as que ocorrem dentro.
Menisco
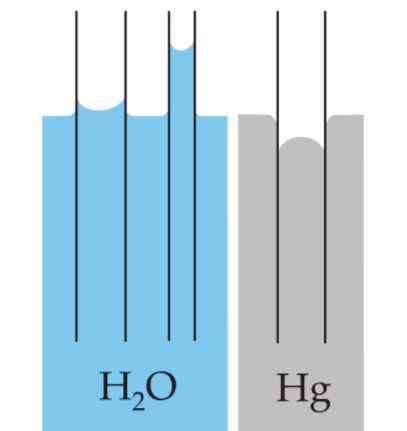
A curvatura criada na superfície dos líquidos é chamada menisco quando confinada em um contêiner. Esta curva é produzida pelo efeito que a superfície do recipiente tem no líquido que o contém.
Pode atendê -lo: medidores de pressãoA curva pode ser convexa ou côncava, dependendo se a força entre as moléculas do líquido e as do recipiente são de atração - como é o caso de água e vidro - ou são de repulsão, como é o caso entre mercúrio e vidro.
Capilaridade
 Exemplo de capilaridade
Exemplo de capilaridade A capilaridade é uma propriedade de fluidos que lhes permite subir ou descer através de um tubo capilar. É a propriedade que permite, em parte, a ascensão da água dentro das plantas.
Um líquido sobe através do tubo capilar quando as forças de coesão são inferiores às de adesão entre o líquido e as paredes do tubo. Dessa maneira, o líquido continuará subindo até que o valor da tensão superficial seja igual ao peso do líquido contido no tubo capilar.
Pelo contrário, se as forças de coesão forem maiores que as da adesão, a tensão superficial descerá ao líquido e a forma de sua superfície será convexa.
Referências
- Coesão (Química) (N.d.). Na Wikipedia. Recuperado de.Wikipedia.org.
- Tensão superficial (n.d.). Na Wikipedia. Recuperado de.Wikipedia.org.
- Capilaridade (n.d.). Na Wikipedia. Recuperado de es.Wikipedia.org.
- Irã. Levine; "Físico -química" volume 1; Quinta edição; 2004; MC Graw Hillm.
- Moore, John W.; Stanitski, Conrad L.; Jurs, Peter C. (2005). Química: a ciência molecular. Belmont, CA: Brooks/Cole.
- Branco, Harvey e. (1948). Física da faculdade moderna. Van Nostrand.


