Estrutura de di -hidroxiacetona, propriedades, obtenção, usos
- 4137
- 766
- Dennis Heidenreich
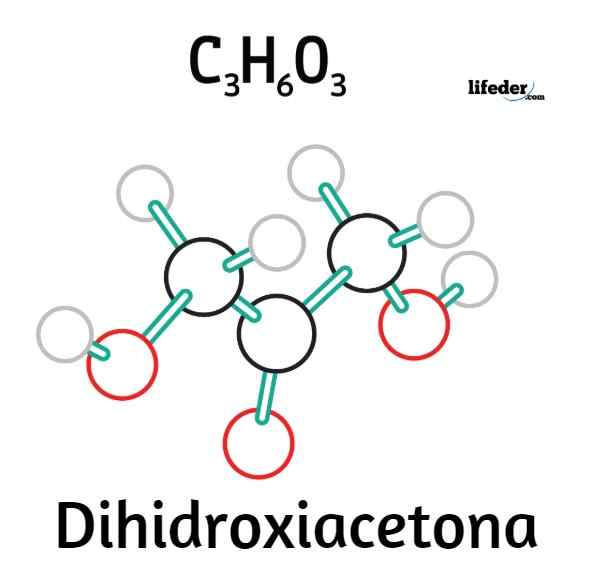
O Di -hidroxiacetona É um sacarídeo ou açúcar que consiste no cetoso mais simples de todos, e cuja fórmula molecular é c3H6QUALQUER3. É, portanto, um isômero estrutural do gliceraldeído, sendo capaz de ser considerado uma versão oxidada da glicerina. Seu nome é abreviado com as cartas DHA, tanto em inglês quanto em espanhol, também o conhecendo com os nomes 1,3-di-hidroxiacetona, glicóneo ou 1.3-di-hidroxi-2-propanona.
Ao contrário de outros açúcares, o DHA não possui carbonos assimétricos, por isso não possui configuração D ou L ou apresenta atividade óptica; isto é, você não pode desviar a luz polarizada. O que ele compartilha em comum com os açúcares, sendo um Zea, é um sabor doce característico e uma grande solubilidade na água.
 Fórmula estrutural de di -hidroxiacetona
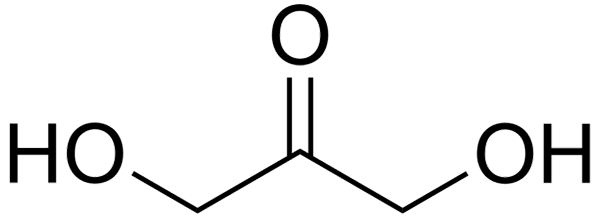
Fórmula estrutural de di -hidroxiacetona Na imagem superior, temos a fórmula estrutural de di -hidroxiacetona. Grupo C = O Central é a razão pela qual o DHA é uma lettose.
O DHA é capaz de reagir com os grupos amina das queratinas que compõem a superfície mais externa da nossa pele, chamada Stratum Corneum, produzindo pigmentos de tonalidades laranja que acabam dando a aparência de um bronzeado natural. É por isso que o DHA é usado como um ingrediente ativo nos produtos de bronze sem sol.
[TOC]
Estrutura

Na imagem superior, temos a estrutura de uma molécula DHA representada com um modelo de esferas e barras. Como pode ser visto, as esferas vermelhas correspondem a átomos de oxigênio. Sua geometria é quase plana, já que os grupos OH e H se destacam um pouco do plano formado pelos três átomos de carbono e pelo atômico de oxigênio carbonil.
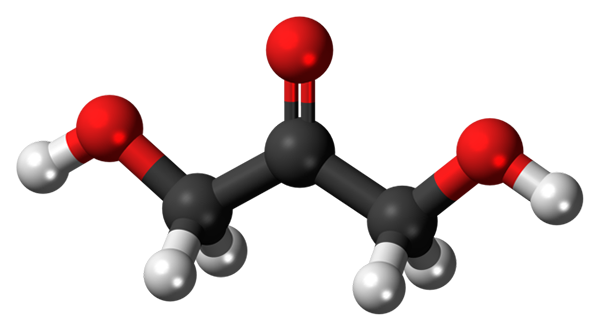 Estrutura molecular da di -hidroxiacetona. Fonte: Jynto / CC0
Estrutura molecular da di -hidroxiacetona. Fonte: Jynto / CC0 A molécula do DHA é bastante polar. Os grupos C = O e C-OH deixam uma alta densidade eletrônica, enquanto o esqueleto de carbono é um pouco de elétrons.
Pode atendê -lo: acetofenonaSuas interações intermoleculares são, portanto, baseadas nas forças dipolo-dipolo, especialmente as de pontes de hidrogênio. Tudo isso contribui para o DHA existe como um sólido cristalino em condições normais.
Propriedades da di -hidroxiacetona
Aparência física
Sólido cristalino colorido, com um cheiro e sabor doces e característicos. É altamente higroscópico, por isso absorve a umidade do meio ambiente.
Massa molar
90.078 g/mol
Ponto de fusão
89 a 91 ºC. Esse valor impreciso se deve ao fato de que nem todas as moléculas de DHA estão no estado explicado, mas que a grande maioria deles forma crepúsculo.
Ponto de ebulição
Indeterminado, pois quebra.
Solubilidade
É muito solúvel em água, com uma solubilidade aproximada de 930 kg/L a 25 ºC. Isso se deve ao seu caráter altamente polar e à capacidade da água de hidratá -lo, formando pontes de hidrogênio com qualquer um dos três átomos de oxigênio de sua molécula. No entanto, se dissolve lentamente em uma mistura de estanol de água 1:15.
Hidrólise e dissolução
No estado sólido, o DHA tende a existir como um domer. A transformação seria a mostrada abaixo:
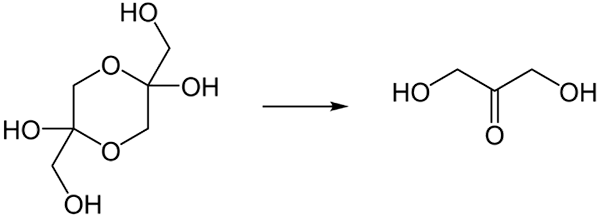 A conversão do dímero do DHA para o seu monômero quando dissolvida na água. Fonte: Steffen 962 na Wikipedia alemã / domínio público
A conversão do dímero do DHA para o seu monômero quando dissolvida na água. Fonte: Steffen 962 na Wikipedia alemã / domínio público Sendo o DHA em sua forma monomérica muito higroscópica, rapidamente quando estava secando e absorvendo a umidade retorna para estabelecer o dímero com seu anel de dioxan.
Obtenção e síntese
Naturalmente, o DHA pode ser obtido extraindo -o de juncos de açúcar ou beterraba açucarada.
Por outro lado, quando se trata de sintetizá -lo ou produzir, existem várias alternativas, todas baseadas na reação de oxidação da glicerina. Um deles é oxidar glicerina ou glicerol com peróxido de hidrogênio usando sais ferrosos, como catalisadores. Em outra reação, glicerina com ar, oxigênio ou benzoquinona oxida, mas usando catalisadores especiais de paládio.
Pode servir a você: Modelo Atomico de Perrina: Características, PostulaTambém temos o método de produção comercial do DHA, no qual a glicerina é oxidada usando bactérias de ácido acético em um processo de fermentação.
Durante a síntese do DHA, também há gliceraldeído, seu isômero estrutural.
Riscos
Os riscos em torno do DHA não são totalmente claros. Em sua forma fosfatada, a di-hidroxiacetona fosfato, é um produto da glicólise e um intermediário no metabolismo da frutose, uma vez que a enzima trisomerase de trisorofosfato o transforma em D-gliceraldeído 3-fosfato. No entanto, uma dose excessiva de DHA, de acordo com estudos médicos, pode alterar negativamente todo esse mecanismo, até causando morte celular.
É por isso que o DHA é considerado perigoso se for ingerido ou se, acima de tudo, é inalado. Além disso, existem estudos que confirmam que suas aplicações tópicas aumentam a concentração de espécies oxigenadas reativas (EROs), que atacam células da pele que produzem seu envelhecimento e o aparecimento de rugas.
Essa reação colateral parece ainda mais acentuada quando a pele impregnada com DHA é exposta aos raios UV do sol, de modo que os riscos de danos à pele aumentam.
Os especialistas, portanto, recomendam não usar o DHA em espaços ao ar livre imediatamente após a aplicação das loções de bronzeamento na pele.
Para reduzir esse risco, as loções contêm aditivos, como óleos vegetais e antioxidantes, além de microcapsulas que liberam gradualmente o DHA.
Usa a di -hidroxiacetona
 As loções bronzeadas que contêm DHA são uma opção mais segura quando a pele está se bronzeando sem se expor aos raios do sol
As loções bronzeadas que contêm DHA são uma opção mais segura quando a pele está se bronzeando sem se expor aos raios do sol A di -hidroxiacetona é sinônimo de cosméticos, pois é o ingrediente ativo de muitos produtos de bronzeamento, ser cremes, esparsagens, máscaras, loções etc. Ao aplicar esses bronzeadores na pele, ocorre a reação do Mailrd, responsável por isso adquire uma cor mais laranja, sem visitar a praia ou se expor a longas horas sob o sol da manhã.
Pode atendê -lo: impenetrabilidade químicaNo início, em 1960, o bronzeado era exagerado, a tal ponto que, durante décadas, o público em geral rejeitou esse tipo de curtidor. No entanto, desde então, as formulações estavam melhorando, de modo que os bronzeados pareciam mais naturais, radiantes e agradáveis à vista, garantindo riscos mais baixos após seus usos.
Várias marcas, incluindo canal Coco, diminuíram as concentrações de DHA para um máximo de 20%, também incorporando -lhes eritrule, outro açúcar que também reage com proteínas da pele e componentes que neutralizam os efeitos dos raios UV. Eles também procuraram prolongar a durabilidade do bronzeado após a aplicação.
Atualmente, novos produtos de bronzeamento chegam ao mercado, que permanecerão em expansão até que os estudos médicos certifiquem que o bronzeado não usa os possíveis riscos da aplicação tópica de DHA, que se acredita ser capaz de se absorver nas camadas mais profundas da pele.
Referências
- Graham Solomons t.C., Craig b. Fryhle. (2011). Química orgânica. (10º Edição.). Wiley Plus.
- Carey f. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Morrison e Boyd. (1987). Quimica Organica. (Quinta edição). Addison-Wesley Iberoamericana.
- Cyriminna, r., Fidalgo, a., Ilharco, l. M., & Pagliaro, M. (2018). Di -hidroxiacetona: uma visão atualizada de um importante bioproduto. Química, 7(3), 233-236. doi.org/10.1002/aberto.201700201
- Wikipedia. (2020). Di -hidroxiacetona. Recuperado de: em.Wikipedia.org
- Centro Nacional de Informações sobre Biotecnologia. (2020). Di -hidroxiacetona. Resumo do PubChem Comunund para CID 670. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Mary Gallagher. (2018). Exposição à di -hidroxiacetona em produtos de bronzeamento sem sol, compreendendo os riscos. Associação de Enfermeiras de Dermatologia. Doi: 10.1097/JDN.0000000000000366

