Estrutura de brometo de potássio (KBR), propriedades, usos
- 850
- 94
- Terrence King IV
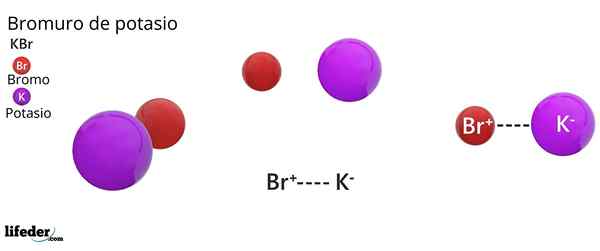
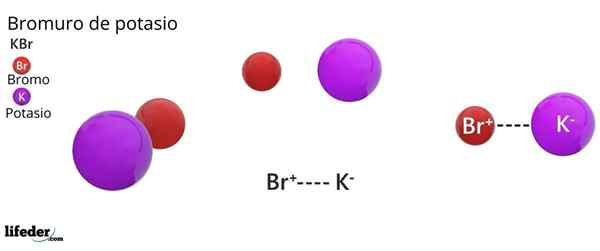
Ele brometo de potássio É um sal inorgânico cuja fórmula química é kbr. É formado pela união eletrostática de um ânion de brometo, BR-, E um cátion de potássio, k+, em uma proporção 1: 1; isto é, temos a mesma quantidade de BR- A partir de k+ Em cristais KBr.
O brometo de potássio é um sal sólido ou cristalino, é inodoro, muito solúvel em água e pouco solúvel em etanol e etanol. Foi usado durante a parte final do século XIX e grande parte do século XX no tratamento da epilepsia e como um sedativo.
Até 1975, continuou a vender livremente, o ano em que seu uso diminuiu devido aos efeitos tóxicos que produziu nos pacientes. Atualmente, ainda é usado em várias espécies de animais no tratamento de convulsões, embora a partir de 1912 tenha sido substituído por fenobarbital de sódio.
O brometo de potássio é usado em estudos ópticos correspondentes à região infravermelha próxima do espectro eletromagnético. Também serve como material usado no campo da fotografia.
[TOC]
Tipo de link
O brometo de potássio é um sal binário, produto da combinação de um átomo de bromo com um estado de oxidação -1, com um átomo de potássio com um estado de oxidação +1. Portanto, uma atração elétrica entre o íon Br é estabelecida- E o K Ion+.
Esse tipo de interação elétrica ou eletrostática é conhecida como uma ligação iônica, que se dissocia quando o sal de brometo de potássio se dissolve na água, liberando os íons k+ e br-.
Esses íons são desintegrados pelos proprietários de água.
Estrutura de brometo de potássio
 Estrutura de cristal FCC do KBR: as esferas marrons correspondem ao BR-, enquanto as esferas violeta correspondem aos cátions k+
Estrutura de cristal FCC do KBR: as esferas marrons correspondem ao BR-, enquanto as esferas violeta correspondem aos cátions k+ O brometo de potássio apresenta uma estrutura cristalina cúbica centrada na face (FCC) Cúbico cúbico de rosto), igual ao observado em cloreto de sódio.
Pode atendê -lo: Faraday constanteNesta estrutura, cada ânion br- Está ligado ou coordenado com seis cátions+, E por sua vez, cada k+ Tem seis br- Como vizinhos em redes cristalinas.
Nomenclatura
O brometo de potássio é classificado como halogeneto de halogeneidade ou metal alcalino. Os nomes desses sais são construídos eliminando a letra final do nome do halogênio (cloro, bromo, iodo, fluorina e astato), com exceção do fluoreto, e substituindo a letra final pelo sufixo -Uro. O nome do metal é escrito abaixo sem modificação.
Por exemplo: cloreto de sódio, iodeto de potássio, fluoreto de cálcio, etc. É por isso que o KBR é chamado brometo de potássio ou brometo de potássio (de acordo com a nomenclatura tradicional).
Propriedades de brometo de potássio
 Disco de relógio com grânulos KBR. Fonte: Walkerma via Wikipedia.
Disco de relógio com grânulos KBR. Fonte: Walkerma via Wikipedia. Aspecto físico
Grânulos de vidro incolor, cristalino ou branco.
Cheiro
Lavatório
Sabor
Em uma alta concentração, tem um sabor amargo e picante.
Massa molar
119.02 g/mol
Densidade
2.74 g/cm3 a 25 ºC
Ponto de fusão
734 ºC
Ponto de ebulição
1435 ºC
Solubilidade em água
535 g/l a 0 ºC
678 g/l a 25 ºC
1020 g/l a 100 ºC
1 grama do sal é dissolvido em 1 ml de água fervente, o que indica que é muito solúvel em água.
Solubilidade em glicerol
217 g/l
1 grama de brometo de potássio se dissolve em 4.6 ml de glicerol.
Solubilidade de etanol
47.6 g/l A 80 ºC.
1 grama de brometo de potássio se dissolve em 250 ml de etanol.
Densidade do vapor
7.14 no relacionamento aéreo tomado como unidade.
Estabilidade
Estável se armazenado nas condições recomendadas. Incompatível com agentes oxidantes, ácidos fortes, trifluoreto de bromo e bromo.
Decomposição
Quando aquecido para decomposição emite produtos nocivos, como brometo de hidrogênio e óxido de potássio.
Pode atendê -lo: Configuração eletrônica do kernel: construção, exemplosÍndice de Refração (ND)
1.559
ph
Em solução aquosa produz um pH neutro, cerca de 7.
ponto de ignição
1435 ºC
Dissolução e reatividade
Em solução aquosa, o KBR é completamente dissociado para causar uma solução de pH neutro.
O sal é uma fonte de brometo que pode ser usada para produção de brometo de prata, AGBR, composto usado no desenvolvimento de fotografias:
KBR (AC) +AGNO3 (AC) → AGBR (S) +KNO3 (AC)
Além disso, o KBR é um agente redutor fraco, incompatível com mercúrio e sais de prata. Produz uma reação violenta com o trifluoreto de bromo. Pode reagir com muitos sais, alcalóides e amido.
Também reage com os ácidos, por exemplo, com ácido sulfúrico concentrado, liberando brometo de hidrogênio.
Formulários
Epilepsia e tratamento de convulsões
As propriedades anticonvulsivas do brometo de potássio foram expostas pela primeira vez por Sir Charles Locock, em uma reunião da Real Medicina e Sociedade Chirurgical em 1857, que promoveu seu uso no tratamento da epilepsia.
O brometo de potássio foi usado como medicamento prioritário no tratamento da epilepsia e como sedativo até 1912, quando o fenobarbital do sódio foi anunciado.
Mesmo assim, continuou a ser usado como um complemento ao fenobarbital de sódio no tratamento de convulsões da epilepsia.
No ano de 1975, devido ao seu caráter tóxico, o FDA U.S. (Food & Drug Administration) decidiu não recomendar o uso de brometo de potássio, tanto em humanos quanto em animais. No entanto, alguns países continuaram a administrá -lo.
O brometo de potássio foi usado como hipnótico e sedativo em gado, cavalos, ovelhas e porcos. Também foi usado no tratamento de cólicas e tetania em cavalos e no tratamento de convulsões em cães.
Óptica infravermelha
Devido à transparência do brometo de potássio em uma variedade de comprimentos de onda entre a luz ultravioleta e o infravermelho próximo, é usado como um componente das janelas para várias radiação eletromagnética, especialmente radiação infravermelha.
Pode atendê -lo: osmolaridadeVárias técnicas são usadas nesse sentido. Um deles consiste na elaboração de dois discos cristalinos de brometo de potássio, colocando um filme do material a ser analisado no infravermelho nos álbuns. Os estudos são realizados no infravermelho próximo entre 780 nm e 3000 nm.
Fotografia
 O KBR fazia parte dos materiais usados para processar as primeiras fotografias do século XX
O KBR fazia parte dos materiais usados para processar as primeiras fotografias do século XX O brometo de potássio teve numerosos usos e aplicações na fotografia, por exemplo: tem sido usado para formular desenvolvedores de fotografia, na fabricação de filmes fotográficos, como um filme espessor e como uma alvejante de cor em cores.
É usado na melhoria da diferenciação entre os cristais de halogenetos de prata expostos e não expostos, no aumento da densidade de impressão de negativos finos e como halogeneto secundária, em combinação com iodetos, para o processamento de papel negativo no papel.
Também tem sido usado em combinação com bicloreto de mercúrio, sulfato de cobre ou potássio Ferianurio em arquibancadas fotográficas. Também serviu como limitador nos desenvolvedores alcalinos usados para placas de gelatina e documentos de desenvolvimento.
Análises químicas
O KBR é usado para determinar a avaliação de cobre e prata, na análise polarográfica do indiano, cádmio e arsênico.
Outros usos
É usado nos processos de gravação de litografia, no processamento de petróleo, na estabilização térmica do nylon, na fabricação de fibras e, finalmente, na fabricação de sabonetes especiais.
Referências
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- Shiver & Atkins. (2008). Química Inorgânica. (Quarta edição). Mc Graw Hill.
- Dia, r., & Underwood, um. (1986). Química analítica quantitativa (Quinta ed.). Pearson Prentice Hall.
- Wikipedia. (2020). Brometo de potássio. Recuperado de: em.Wikipedia.org
- Centro Nacional de Informações sobre Biotecnologia. (2021). Brometo de potássio. Resumo do PubChem Comunund para CID 253877. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- EMEA. (1999). Brometo, sal de potássio: relatório de resumo. [PDF]. Recuperado de: Ema.Europa.UE
- Sevier b.V. (2020). Brometo de potássio. Cientedirect. Recuperado de: ScientEdirect.com

