Estrutura de óxido de titânio (iv), propriedades, usos

- 3873
- 985
- Conrad Schmidt
Ele Óxido de titânio (IV) É um sólido inorgânico branco cristalino cuja fórmula química é tio2, Portanto, também é conhecido como dióxido de titânio. Existe em três formas cristalinas: Rutilo, Anatasa e Brookita. Embora na natureza seja geralmente colorida devido à presença de impurezas como ferro, cromo ou vanádio, o tio2 puro é usado como um pigmento branco.
Entre suas características, podemos destacar que a solubilidade do tio2 Depende consideravelmente de sua história química e térmica. Assim como o quando é aquecido a altas temperaturas (900 ºC), torna -se quimicamente inerte. Suas fontes mais importantes são ilmenita (ferro e óxido de titânio), rutilo e anatase.
 Poeira de dióxido de titânio. O uploader original era Walkingerma na Wikipedia inglesa. [Domínio público]
Poeira de dióxido de titânio. O uploader original era Walkingerma na Wikipedia inglesa. [Domínio público] Ocorre principalmente em um grau adequado para uso como pigmento, o que garante suas excelentes propriedades de dispersão de luz em aplicações que requerem opacidade e brilho branco.
Também ocorre como material ultrafino, para aplicações nas quais a transparência e a absorção máxima dos raios ultravioleta (UV) são necessários. Por exemplo, como um componente de filtros solares para a pele. Nestes, o tio2 Ele atua como um filtro, bloqueando assim a absorção desses raios.
Por causa de sua inércia química, é o pigmento branco preferido. No entanto, a Food and Drug Administration dos Estados Unidos, ou FDA (sigla para inglês OU.S. Administração de Alimentos e Medicamentos), estabeleceu os parâmetros para uso seguro em alimentos e cosméticos.
Há também um limite de exposição ao pó de óxido de titânio, pois quando a poeira é inalada, ele pode ser depositado nos pulmões.
Pode atendê -lo: calcógenos ou anfumos[TOC]
Estrutura
O tio2 Tem três modificações cristalinas: Rutilo, Anatasa e Brookita. Essas variedades cristalinas são todas na natureza.
Rutilo
O Rutho cristaliza no sistema tetragonal com duas unidades2 para cada célula. O titânio é coordenado octaéconicamente. Foi demonstrado por estudos calorimétricos que Rutilo é a forma cristalina mais estável.
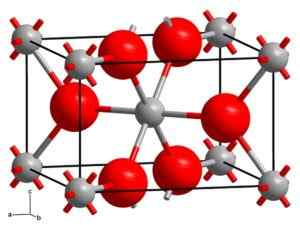 Estrutura cristalina de rutilo. Bolas cinzas: titânio, bolas rosa: oxigênio. Estado sólido [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)] Fonte: Wikipedia Commons
Estrutura cristalina de rutilo. Bolas cinzas: titânio, bolas rosa: oxigênio. Estado sólido [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)] Fonte: Wikipedia Commons Anatasa
Esta forma se cristaliza no sistema tetragonal, mas a anatase é apresentada na forma de octoms muito distorcidos de átomos de oxigênio em relação a cada átomo de titânio, dois deles sendo relativamente próximos. Tem 4 unidades de tio2 Para cada célula cristalina.
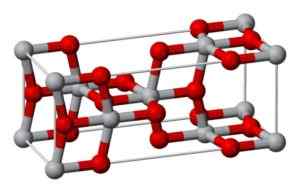 Estrutura cristalina da anatase. Benjah-BMM27 [Domínio Público] Fonte: Wikipedia Commons
Estrutura cristalina da anatase. Benjah-BMM27 [Domínio Público] Fonte: Wikipedia Commons Brookita
Cristaliza no sistema Ortorrombic, com 8 unidades TIO2 Para cada célula cristalina.
Propriedades
Estado físico
Sólido cristalino.
Dureza mohs
Rutilo: 7-7.5.
Anatasa: 5.5-6.
Peso molecular
79,87 g/mol.
Ponto de fusão
Rutilo: 1830-1850 ºC.
Anatasa: Quando o aquecimento se torna Rutilo.
Densidade
Rutilo: 4.250 g/cm3
Anatasa: 4.133 g/cm3
Brookita: 3.895 g/cm3
Solubilidade
Insolúvel em água e solventes orgânicos. Ele se dissolve lentamente em HF e H2SW4 Concentrado quente. Insolúvel em hcl e hno3.
ph
7.5.
Índice de refração
Rutilo: 2,75 a 550 nm.
Anatasa: 2,54 a 550 nm.
Tem o maior índice de refração de todos os pigmentos inorgânicos.
Outras propriedades
A anatase é rapidamente transformada em rutilo a temperaturas acima de 700 ºC. O tio2 que foi calcinado a 900 ° C é dissolvido fracamente em bases, ácido fluorhorérico e ácido sulfúrico quente. Não é atacado por ácidos inorgânicos fracos ou ácidos orgânicos. Não é facilmente reduzido ou oxidado.
Pode servir a você: Scandio: História, Propriedades, Reações, Riscos e UsosAnatase e Rutil.
Nomenclatura
-Dióxido de titânio
-Rutilo
-Anatasa
-Brookita
-Titania
Formulários
Pigmentos brancos
O uso mais importante do óxido de titânio (IV) é como um pigmento branco em uma ampla variedade de produtos, que incluem tintas, lacas, adesivos, plásticos, tintas de papel e impressão. Isso se deve ao seu alto índice de refração e sua inércia química.
 Fonte: pexels.com
Fonte: pexels.com Dióxido de titânio usado como pigmento branco deve ter alta pureza. Sua opacidade e brilho derivam de sua capacidade de dispersar a luz. É mais brilhante que o diamante. Somente Rutilo e Anatase têm boas propriedades de pigmentação.
Plásticos
Nos plásticos, o tio2 Minimiza a fragilidade e rachaduras que podem ocorrer como resultado da exposição à luz.
É o pigmento mais importante na fabricação de itens de plástico de PVC externos, porque fornece proteção UV ao material.
A forma cristalina ideal neste caso é Rutilo. Nesta aplicação, o rutilo deve ter um revestimento superficial de zircônio, sílica ou alumínio, para minimizar o efeito fotocatalítico do tio2 Na degradação do PVC.
Outros usos
Outros usos incluem esmaltes vítreo usados em aço fundido e ferro, o que confere opacidade e resistência ao ácido.
Na indústria têxtil, é usada nos guias de threads, para que eles estejam facilmente deslizando durante o fio. O atrito entre fios e guias gera eletricidade estática. Para dissipar, o tio2 Deve ser queimado a 1300 ºC, a fim de ter maior condutividade elétrica.
Pode atendê -lo: fluoreto de lítio: estrutura, propriedades, obtenção, usosOutras aplicações incluem pigmentação de tinta para impressão. Como revestimento de papel, o tio2 Torna isso mais branco, brilhante e mais opaco.
É usado em cosméticos para ajudar a cobrir as imperfeições da pele, bem como para dar pasta de dente branca e sabão.
Ele permite proteger alimentos, bebidas, suplementos e produtos farmacêuticos da degradação prematura produzida pelo efeito da luz, estendendo a vida útil do produto.
É um componente na produção de vidro, cerâmica e eletrocerâmico. É usado em elementos de circuito elétrico. Também é usado no sensor de oxigênio do sistema de escape de veículos a motor.
O tio2 O Ultrafino é usado como um componente dos bloqueadores solares, pois é um forte absorvente dos raios ultravioleta (UV), UV-A e UV-B. Os raios UV-A causam rugas e envelhecimento da pele, e UV-B causam queimaduras e eritema.
As nanopartículas do tio2 Eles são usados como reações químicas Catalyst Support Material.
A anatase é uma fotocatização eficaz que oxida compostos orgânicos. Enquanto menores são suas partículas, mais eficaz é.
Referências
- Algodão, f. Albert e Wilkinson, Geoffrey. (1980). Química inorgânica avançada. John Wiley & Sons.
- Kirk-Othmer (1994). Enciclopédia de tecnologia química. Volume 19 e 24. Quarta edição. John Wiley & Sons.
- Fatos de segurança química. (2019). Dióxido de titânio. Recuperado de: ChemicalSafetyfacts.org
- Wypych, George. (2015). Aditivos de PVC. No formulário de PVC (segunda edição). Recuperado de cientedirect.com
- Denning, r. (2009). Melhorando produtos de lã usando nanotecnologia. Em avanços na tecnologia de lã. Recuperado de cientedirect.com
- Biblioteca Nacional de Medicina. (2019). Dióxido de titânio. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- « Função do perfil da tireóide de hormônios, importância, quantificação
- Chulachaqui Características e lenda »

