Estrutura do tripolifosfato de sódio (Na5p3310), propriedades, usos, impacto, impacto
- 3124
- 606
- Orlando MacGyver
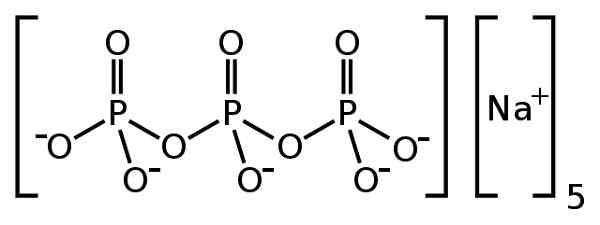
Ele tripolifosfato de sódio É um composto inorgânico formado por cinco íons de ná de sódio+ e um íon pupolifosfato P3QUALQUER105-. Sua fórmula química é na5P3QUALQUER10. O íon tripolifosfato contém três unidades de fosfato ligadas entre si e é o que é chamado de fosfato condensado.
O ânion do tripolifosfato P3QUALQUER105- Tem a capacidade de capturar íons como CA cálcio2+ E magnésio mg2+, Portanto, tripoliff de sódio.
 Sodium na tripolifosfato5P3QUALQUER10. BenRR101 [domínio público]. Fonte: Wikimedia Commons.
Sodium na tripolifosfato5P3QUALQUER10. BenRR101 [domínio público]. Fonte: Wikimedia Commons. O tripolifosfato de sódio também é usado como fonte de fósforo na alimentação de animais de pastagem e no tratamento de algumas doenças de outros tipos de animais. Também serve para engrossar e dar textura a alguns alimentos processados, como cremes, pudim e queijos.
Na indústria agrícola, é usado em fertilizantes em grânulos para impedir que eles se grudem e podem permanecer soltos.
Embora tenha havido discussões sobre o impacto ambiental do tripolifosfato de sódio que é adicionado aos detergentes, atualmente estima -se que ele não contribua consideravelmente para danificar o ambiente, pelo menos por meio de detergentes.
[TOC]
Estrutura química
O tripolifosfato de sódio faz parte dos fosfatos condensados de maneira assim chamada porque são várias unidades de fosfato juntas uns com os outros. Nesse caso, o íon tripolifosfato é um fosfato de condensado linear porque possui uma estrutura de tipo de cadeia linear, com ligações fosforus-oxigênio-fosforas (P-O-P) (P-O-P).
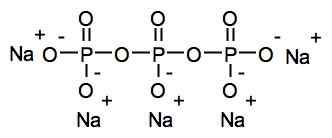 Estrutura química de tripolifosfato de sódio. Roland.Chem [GFDL (http: // www.gnu.Org/copyleft/fdl.html)]. Fonte: Wikimedia Commons.
Estrutura química de tripolifosfato de sódio. Roland.Chem [GFDL (http: // www.gnu.Org/copyleft/fdl.html)]. Fonte: Wikimedia Commons. Nomenclatura
- Tripolifosfato de sódio
- Trifosfato de sódio
- Pentasodio tifosfato
- Stpp (sigla em inglês Tripolifato de sódio)
Propriedades
Estado físico
Sólido branco cristalino.
Peso molecular
367,86 g/mol.
Ponto de fusão
622 ° C.
Densidade
2,52 g/cm3
Solubilidade
Solúvel em água: 20 g/100 ml a 25 ° C e 86,5 g/100 ml a 100 ° C.
Pode atendê -lo: o que são funções químicas inorgânicas?ph
Uma solução de 1% de tripolifosfato de sódio tem um pH de 9,7-9,8.
Propriedades quimicas
É um agente de seqüestro de íons, ou seja, pode capturar íons e ficar junto com eles. Forma complexa com muitos metais.
Se uma solução de tripolifosfato de sódio for aquecida por um longo tempo, ela tende a se tornar ortofosfato de sódio3Po4.
Outras propriedades
É um pouco higroscópico. Forma Hidratos estáveis, ou seja, compostos que têm moléculas de água (sem ter reagido com isso) de fórmula na5P3QUALQUER10.NH2Ou onde n pode valer entre 1 e 6.
Segundo algumas fontes, uma quantidade de 20 mg de tripolifosfato de sódio em um litro de água não afeta o cheiro, o sabor ou o pH da referida água.
Obtenção
O tripolifosfato de sódio é preparado por desidratação de ortofosfatos (como o fosfato monossódico Nah2Po4 E dis -ffosfat na2HPO4) a temperaturas muito altas (300-1200 ° C):
Nah2Po4 + 2 NA2HPO4 → Na5P3QUALQUER10 + 2 h2QUALQUER
Também pode ser obtido por calcinação controlada (significa aquecimento de temperatura muito alta) de ortofosfato de sódio Na3Po4 Com carbonato de sódio na2Co3 e ácido fosfórico H3Po4.
Formulários
Em detergentes
O tripolifosfato de sódio tem a propriedade de formar compostos com certos íons, mantendo -os. Ele também tem propriedades de dispersão de partículas sujas e as mantém em suspensão.
Por esse motivo, é amplamente utilizado em formulações de detergentes para capturar e imobilizar íons de cálcio CA2+ e magnésio mg2+ de água (das águas duras e tão folhadas) e para manter a suja na água suspensa.
Os íons acima mencionados interferem na ação de limpeza. Ao pegá -los, o tripolifosfato impede que esses íons precipitem juntamente com o agente de limpeza ou aderindo da suja no tecido que impedem a mancha de decolar disso.
Dizem que, neste caso. Portanto, é usado em detergentes para roupas e detergentes automáticos da máquina de lavar louça.
Pode atendê -lo: seringa PascalComo forma hidratos estáveis, os detergentes que o possuem em sua formulação podem ser instantaneamente secos por spray (orvalho muito fino) formando pós secos.
 Poeira detergente que pode conter o tripolifosfato de sódio. Autor: Frank Habel. Fonte: Pixabay.
Poeira detergente que pode conter o tripolifosfato de sódio. Autor: Frank Habel. Fonte: Pixabay. Para uso veterinário
O tripolifosfato de sódio é usado como suplemento em soluções líquidas como fonte de fósforo para gado.
 A feed de vacu pode ser complementada com o tripolifosfato de sódio como fonte de fósforo. Autor: Herney Gómez. Fonte: Pixabay.
A feed de vacu pode ser complementada com o tripolifosfato de sódio como fonte de fósforo. Autor: Herney Gómez. Fonte: Pixabay. Também serve para evitar cálculos renais em gatos, para os quais esses animais são fornecidos por via oral. No entanto, deve ser dada atenção na dose, pois pode causar diarréia.
 O tripolifosfato de sódio em doses muito baixas pode prevenir rins em gatos. Autor: Scott Payne. Fonte: Pixabay.
O tripolifosfato de sódio em doses muito baixas pode prevenir rins em gatos. Autor: Scott Payne. Fonte: Pixabay. Em medicina
O tripolifosfato de sódio tem sido usado na preparação de nanopartículas para transporte adequado e liberação de medicamentos para quimioterapia ao câncer. Também tem sido usado em nanopartículas para o tratamento de infecções por fungos nos pulmões.
 Tripolifosfato está sendo testado na preparação de nanofarmacais para curar infecções fúngicas nos pulmões. Autor: OpenClipart-Vectors. Fonte: Pixabay.
Tripolifosfato está sendo testado na preparação de nanofarmacais para curar infecções fúngicas nos pulmões. Autor: OpenClipart-Vectors. Fonte: Pixabay. Na indústria de alimentos
É usado em produtos lácteos, como cápsulas, chantilly, creme de leite e queijo.
 Crector azedo pode conter o tripoliff de sódio para melhorar sua textura. Autor: Welikodub. Fonte: Pixabay.
Crector azedo pode conter o tripoliff de sódio para melhorar sua textura. Autor: Welikodub. Fonte: Pixabay. Em outros alimentos, é usado como seqüestrador de íons, para dar textura, como espessante e como conservante.
Outros usos
- Como estabilizador de peróxidos
- Nos fluidos de perfuração de petróleo, funciona como um emulsificante e dispersante para controlar a viscosidade da lama.
Pode atendê -lo: metais ferrosos- Na agricultura, é usado como um agente anti -recipiente de certos fertilizantes ou produtos agrícolas, isso significa que eles os impede de se aderirem e o fertilizante pode ser facilmente distribuído. Também é usado em fórmulas de pesticidas aplicadas ao cultivo de culturas.
 Fábrica de fertilizantes. Às vezes tripoliff de sódio de sódio. Van Twin [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikimedia Commons.
Fábrica de fertilizantes. Às vezes tripoliff de sódio de sódio. Van Twin [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikimedia Commons. Impacto ambiental
O uso de produtos com fosfatos foi identificado como um dos colaboradores da eutrofização das águas no planeta.
A eutrofização é o crescimento exagerado e acelerado de algas e espécies de plantas aquáticas que levam a uma forte diminuição do oxigênio disponível na água, levando à destruição ao ecossistema afetado (morte da maioria das espécies animais nele).
 A eutroficação é o crescimento exagerado de algas em um lago, rio ou mar. F. Lamiot (trabalho próprio) [CC BY-SA 2.5 (https: // CreativeCommons.Org/licenças/BY-SA/2.5)]. Fonte: Wikimedia Commons.
A eutroficação é o crescimento exagerado de algas em um lago, rio ou mar. F. Lamiot (trabalho próprio) [CC BY-SA 2.5 (https: // CreativeCommons.Org/licenças/BY-SA/2.5)]. Fonte: Wikimedia Commons. Na década de 1980, surgiu a controvérsia de que o uso de tripolifosfato de sódio em detergentes estava contribuindo para a eutrofização.
Atualmente, sabe -se que limitar o uso de detergentes com tripoliff de sódio.
De fato, existem países que consideram o tripolifosfato de sódio como um componente ambientalmente amigável dos detergentes e promove seu uso.
Riscos
O tripolifosfato de sódio está irritando a pele e os olhos. O contato visual pode causar danos a estes. O contato prolongado da pele pode produzir dermatite.
Se ingerido em grandes quantidades, pode causar náusea, vômito e diarréia, também gerando uma redução séria no íon cálcio no sangue. Nos animais, causou diminuição de cálcio nos ossos.
É considerado um composto seguro sempre que os padrões de fabricação do produto em que é usado são seguidos.
Referências
- Liu, e. E Chen, J. (2014). Ciclo de fósforo. Módulo de referência em sistemas terrestres e ciências ambientais. Enciclopédia de ecologia (segunda edição). Vol. 4, 2014, pp.181-191. Recuperado de cientedirect.com
- OU.S. Biblioteca Nacional de Medicina. (2019). Tripolifato de sódio. Centro Nacional de Informações sobre Biotecnologia. Recuperado de PubChem.NCBI.Nlm.NIH.Gov.
- Mukherjee, b. et al. (2017). Administração pulmonar de nanocarreadores de medicamentos biodegradáveis para mais eficácia tratamento de infecções fúngicas em pulmões: insights baseados em descobertas recentes. Em sistemas multifuncionais para entrega combinada, biossensing e diagnóstico. Recuperado de cientedirect.com.
- Kirk-Othmer. (1991). Enciclopédia de tecnologia química. 4º Nova York, John Wiley e Sons.
- Burckett st. Laurent, J. et al. (2007). Limpeza de lavanderia de têxteis. No manual para limpeza/descontaminação de superfícies. Recuperado de cientedirect.com.
- Budavari, s. (Editor). (mil novecentos e noventa e seis). O índice Merck. NJ: Merck e Co., Inc.
- Salahuddin, n. e galal, para. (2017). Melhorando a entrega de medicamentos quimioterápicos por ferramentas de nanoprecisão. Em nanruturas para terapia contra o câncer. Recuperado de cientedirect.com.
- « Estrutura de oxalato de sódio (Na2C2O4), propriedades, usos, riscos
- Propriedades, usos, estruturas, riscos, riscos, »

