Tensão superficial causas, exemplos, aplicações e experimentos

- 3571
- 824
- Lonnie MacGyver
O tensão superficial É uma propriedade física que todos os líquidos presentes e são caracterizados pela resistência que suas superfícies se opõem a qualquer aumento em sua área. É o mesmo que dizer que essa superfície procurará a área menos possível. Esse fenômeno interlige vários conceitos químicos, como coesão, adesão e forças intermoleculares.
A tensão superficial é responsável pela formação das curvaturas da superfície dos fluidos em recipientes tubulares (cilindros graduados, colunas, tubos de teste, etc.). Estes podem ser côncavos (Vale curvados) ou convexos (cúpula curva). Muitos fenômenos físicos podem ser explicados considerando as mudanças sofridas pela tensão superficial de um líquido.
 As formas esféricas adotadas por gotas de água nas folhas são em parte devido à sua tensão superficial. Fonte: Foto tirada pelo usuário do Flickr Tanakawho [CC por (https: // CreativeCommons.Org/licenças/por/2.0)]
As formas esféricas adotadas por gotas de água nas folhas são em parte devido à sua tensão superficial. Fonte: Foto tirada pelo usuário do Flickr Tanakawho [CC por (https: // CreativeCommons.Org/licenças/por/2.0)] Um desses fenômenos é a tendência de que as moléculas de líquidos precisam aglomerar -se na forma de gotas, quando descansam em superfícies que os repelem. Por exemplo, as gotas de água que vemos acima das folhas não podem molhá -la devido à sua colina, superfície hidrofóbica.
No entanto, chega um momento em que a gravidade exerce seu papel e a queda é derramada como uma coluna de água. Fenômeno semelhante ocorre nas gotas esféricas de Mercúrio quando um termômetro é derramado.
Por outro lado, a tensão das águas superficiais é a mais importante de todas, pois contribui e organiza o status dos corpos microscópicos em meios aquosos, como células e suas membranas lipídicas. Além disso, essa tensão é responsável pela água evaporar lentamente e alguns corpos mais densos que podem flutuar em sua superfície.
[TOC]
Causas de tensão superficial
A explicação do fenômeno da tensão da superfície está no nível molecular. As moléculas de um líquido interagem entre si, para que sejam coesas em seus movimentos erráticos. Uma molécula interage com seus vizinhos ao lado e aqueles que estão acima ou sob ela.
No entanto, isso não acontece o mesmo com as moléculas da superfície do líquido, que estão em contato com o ar (ou qualquer outro gás), ou com um sólido. As moléculas de superfície não podem coesas com as do ambiente externo.
Como resultado, eles não experimentam nenhuma força que os atrai; Somente abaixo, de seus vizinhos do meio líquido. Para neutralizar esse desequilíbrio, as moléculas de superfície são "espremidas", porque só então elas conseguem superar a força que as empurra para baixo.
Pode atendê -lo: silicato de sódio (Na2SIO3): estrutura, propriedades, usos, riscosUma superfície é então criada onde as moléculas estão em uma disposição mais tensa. Se uma partícula quiser penetrar no líquido, ele deve primeiro atravessar essa barreira molecular proporcional à tensão superficial do referido líquido. O mesmo se aplica a uma partícula que deseja escapar para o ambiente externo das profundezas do líquido.
Portanto, sua superfície se comporta como se fosse um filme elástico que mostra resistência a deformar.
Unidades
A tensão superficial é geralmente representada com o símbolo γ e é expressa em unidades N/m, força por comprimento. No entanto, na maioria das vezes sua unidade é dyn/cm. Um pode se tornar o outro através do próximo fator de conversão:
1 dyn/cm = 0,001 n/m
Tensão da água superficial
A água é o oeste e o mais surpreendente de todos os líquidos. Sua tensão superficial, assim como várias de suas propriedades, têm um valor incomumente alto: 72 dyn/cm à temperatura ambiente. Este valor pode aumentar para 75,64 dyn/cm, a uma temperatura de 0 ºC; ou diminuir para 58,85 ºC, a uma temperatura de 100 ºC.
Essas observações fazem sentido se for considerado que a barreira molecular está tensa ainda mais em temperaturas próximas ao ponto de congelamento, ou "solto" um pouco mais ao redor do ponto de ebulição.
A água tem uma grande tensão superficial após suas pontes de hidrogênio. Se estes são notórios dentro do líquido, eles são ainda mais na superfície. As moléculas de água estão fortemente entrelaçadas pela formação de interações dipolo-dipolo do tipo H do tipo H2OH OH.
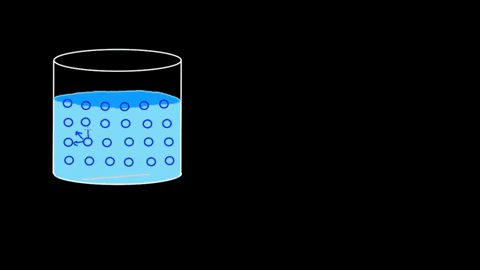 As moléculas de água se atraem; Eles estão ligados por pontes de hidrogênio
As moléculas de água se atraem; Eles estão ligados por pontes de hidrogênio A eficiência de suas interações é tal que a barreira molecular aquosa pode até sustentar alguns corpos antes que eles afundem. Nas seções de aplicações e experimentos, esse ponto será retomado.
Outros exemplos
Todos os líquidos têm tensões de superfície, em menor ou maior grau que a da água, ou se são substâncias ou soluções puras. Quão fortes e tensos são as barreiras moleculares de seus superficiais, dependerá diretamente de suas interações intermoleculares, além de fatores estruturais e de energia.
Gases condensados
Por exemplo, moléculas de gase em estado líquido apenas interagem entre si por meio de forças dispersivas em Londres. Isso concorda com o fato de que suas tensões superficiais têm valores baixos:
-Hélio líquido, 0,37 dyn/cm a -273 ºC
Pode servir você: cloreto de amônio (NH4Cl)-Nitrogênio líquido, 8,85 dyn/cm a -196 ºC
-Oxigênio líquido, 13,2 Dyn/cm A -182 ºC
A tensão superficial do oxigênio líquido é maior que a do hélio, porque suas moléculas têm maior massa.
Líquidos apolares
De líquidos apolares e orgânicos, espera -se que eles tenham tensões superficiais mais altas do que a desses gases condensados. Entre alguns deles, temos o seguinte:
-Dietileter, 17 dyn/cm a 20 ºC
-n-Hexano, 18,40 dyn/cm a 20 ºC
-n-Octane, 21,80 dyn/cm a 20 ºC
-Tolueno, 27,73 dyn/cm a 25 ºC
Uma tendência semelhante é observada para esses líquidos: a tensão superficial é aumentada à medida que suas massas moleculares aumentam. No entanto, o n-O octano deve, de acordo com isso, ter a maior tensão superficial e não o tolueno. Aqui as estruturas e geometrias moleculares entram em jogo.
As moléculas de tolueno, plano e anilares têm interações mais eficazes do que as do n-octano. Portanto, a superfície do tolueno é "tensa" do que a superfície do n-octano.
Líquidos polares
Sendo dipolo-dipol mais forte. Mas nem sempre é o caso. Entre alguns exemplos que temos:
-Ácido acético, 27,60 dyn/cm a 20 ºC
-Acetona, 23,70 dyn/cm a 20 ºC
-Blood, 55,89 dyn/cm a 22 ° C
-Etanol, 22,27 dyn/cm a 20 ºC
-Glicerol, 63 dyn/cm a 20 ºC
-Cloreto de sódio fundido, 163 dyn/cm a 650 ºC
-Solução de 6 m, 82,55 dyn/cm a 20 ºC
Espera -se que o cloreto de sódio fundido tenha uma enorme tensão superficial: é um líquido viscoso e iônico.
Por outro lado, Mercúrio é um dos líquidos com a maior tensão superficial: 487 Dyn/cm. Nele, sua superfície é composta por átomos de mercúrio fortemente coesos, muito mais do que as moléculas de água podem ser.
Formulários
 Alguns insetos usam a tensão superficial da água para andar nela. Fonte: Pixabay.
Alguns insetos usam a tensão superficial da água para andar nela. Fonte: Pixabay. Somente a tensão superficial não possui aplicações. No entanto, isso não significa que não está envolvido em vários fenômenos diários, que se não houvesse, eles não aconteceriam.
Por exemplo, mosquitos e outros insetos são capazes de caminhar pela água. Isso ocorre porque suas pernas hidrofóbicas repelem a água, ao mesmo tempo que sua pequena massa lhes permite.

A tensão superficial também atende a um papel na umidade do fluido. Quanto maior sua tensão superficial, menor a tendência de vazar pelos poros ou filhotes de um material. Além disso, são pequenos líquidos úteis para limpar superfícies.
Pode atendê -lo: reação de neutralizaçãoDetergentes
É aqui onde os detergentes agem, reduzindo a tensão superficial da água e ajudando -a a cobrir superfícies maiores; Ao melhorar sua ação degente. Ao diminuir sua tensão superficial, acomoda moléculas de ar, com as quais as bolhas se formam.
Emulsões
Por outro lado, tensões mais altas estão ligadas à estabilização de emulsões, muito importante na formulação de diferentes produtos de produtos.
Experimentos simples
 Clipe de metal flutuando devido à tensão da água superficial. Fonte: Alvesgaspar [CC BY-S (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]
Clipe de metal flutuando devido à tensão da água superficial. Fonte: Alvesgaspar [CC BY-S (https: // CreativeCommons.Org/licenças/BY-SA/3.0)] Finalmente, algumas experiências que podem ser feitas em qualquer espaço doméstico serão citadas.
Experiência de clipe
Em um copo com água fria, um clipe metálico é colocado em sua superfície. Como visto na imagem superior, o clipe permanecerá à tona graças à tensão superficial da água. Mas se um pouco de lava loza for adicionado ao vidro, a tensão da superfície diminuirá dramaticamente e o clipe afundará repentinamente.

Barco de papel
Se tivermos um navio de papel ou uma paleta de madeira e, se você lavar o pouco ou o detergente, ele será adicionado na cabeça de um swab, ocorrerá um fenômeno interessante: haverá uma repulsa que os espalhará em direção às bordas do vidro. O navio de papel e a paleta de madeira se afastarão do cotonete manchado de detergente.

Outro experimento semelhante e mais gráfico é repetir a mesma operação, mas em um balde de água pulverizado com pimenta preta. As partículas de pimenta preta se afastarão e a superfície passará de pimenta para ser cristalina, com as bordas nas bordas.
Referências
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- Wikipedia. (2020). Tensão superficial. Recuperado de: em.Wikipedia.org
- USGS. (s.F.). Tensão superficial e água. Recuperado de: USGS.Gov
- Jones, Andrew Zimmerman. (12 de fevereiro de 2020). Tensão superficial - definição e experimentos. Recuperado de: pensamento.com
- Susanna Lauren. (15 de novembro de 2017). Por que a tensão superficial é importante? Biolin Scientific. Recuperado de: blog.Biolinscientific.com
- Ciência dos pais novatos. (7 de novembro de 2019). O que é tensão superficial | Experiência científica legal. Recuperado de: RookieParenting.com
- Jessica Mock. (2020). Experiência de tensão superficial. Estudar. Recuperado de: estudo.com
- O garoto deveria ver isso. (2020). Sete Experiências de tensão superficial - Girl de física. Recuperado de: thekidswouldseethis.com

