História do silício, propriedades, estrutura, obtenção, usa

- 3331
- 162
- Alfred Kub
Ele silício É um elemento não -metálico e ao mesmo tempo metalóide que é representado pelo símbolo químico se. É um semicondutor, que é uma parte essencial de computadores, calculadoras, telefones celulares, células solares, diodos etc.; É praticamente o componente principal que permitiu a liquidação da era digital.
O silício sempre esteve presente em quartzo e silicatos, ambos os minerais que compondo cerca de 28% na massa de toda a crosta terrestre. É assim o segundo elemento mais abundante na superfície da terra, e a vastidão dos desertos e praias oferece uma perspectiva de quão abundante é.
 Desertos são uma fonte natural abundante de partículas de sílica ou granitos com outros minerais. Fonte: pxhere.
Desertos são uma fonte natural abundante de partículas de sílica ou granitos com outros minerais. Fonte: pxhere. O silício pertence ao grupo 14 da tabela periódica, o mesmo que o carbono, localizado abaixo disso. É por isso que esse elemento é considerado um metalóide tetravalente; Possui quatro elétrons de Valência e, em teoria4+.
Uma propriedade que compartilha com carvão é sua capacidade de concatenar; isto é, seus átomos estão ligados covalentemente para definir cadeias moleculares. Da mesma forma, o silício pode formar seus próprios "hidrocarbonetos", chamados Siltans.
Os compostos predominantes de silício na natureza são os silicatos famosos. Em sua forma pura, pode ocorrer como um monocristalino sólido, poliristalina ou amorfo. É um sólido relativamente inerte, por isso não representa riscos consideráveis.
[TOC]
História
A pedra de silício
O silício é talvez um dos elementos que tiveram mais influência na história da humanidade.
Este elemento é o protagonista da Idade da Pedra, e também da era digital. Suas origens datam quando as civilizações trabalharam com quartzo e fizeram seu próprio vidro; E atualmente, é o principal componente de computadores, laptops e smartphones.
Praticamente o silício tem sido a pedra de duas épocas claramente definidas em nossa história.
Isolamento
Quando a sílica era tão abundante, um nome nascido da rocha de pederneira, tinha que conter um elemento extremamente rico na crosta terrestre; Essa foi a suspeita bem -sucedida de Antoine Lavoisier, que em 1787 falhou em suas tentativas de reduzi -lo de seu óxido.
Algum tempo depois, em 1808, Humphry Davy fez suas próprias tentativas e atribuiu seu primeiro nome ao elemento: 'Silicium', que traduzido seria como 'Pedernal Metal'. Isto é, o silício até então era considerado um metal devido à sua falta de caracterização.
Então, em 1811, os químicos franceses Joseph L. Gay-Lussac e Louis Jacques Thénard conseguiram preparar o silício amorfo pela primeira vez. Para isso, eles reagiram tetrafluoreto de silício com potássio metálico. No entanto, eles não purificaram ou caracterizaram o produto obtido, então não concluíram que era o novo elemento de silício.
Não era nada além de em 1823, quando o químico sueco Jacob Berzelius obteve um silício amorfo com pureza suficiente para reconhecê -lo como silício; Nome dado em 1817 pelo químico escocês Thomas Thomson ao considerar um elemento não -metálico. Berzelius realizou a reação entre potássio e fluorossilicato de potássio fundido para produzir este silício.
Silício cristalino
O silício cristalino foi preparado pela primeira vez em 1854 pelo químico francês Henry Deville. Para conseguir isso, Deville fez uma eletrólise de uma mistura de cloretos de alumínio e sódio, obtendo assim cristais de silício cobertos por uma camada de siliciuro de alumínio, que eliminou (aparentemente) lavando -os com água com água.
Propriedades físicas e químicas
Aparência física
 Silício elementar, que tem um brilho metálico, mas na verdade é um metalóide. Fonte: imagens de alta resolução de elementos químicos [CC por 3.0 (https: // CreativeCommons.Org/licenças/por/3.0)]
Silício elementar, que tem um brilho metálico, mas na verdade é um metalóide. Fonte: imagens de alta resolução de elementos químicos [CC por 3.0 (https: // CreativeCommons.Org/licenças/por/3.0)] O silício em sua forma pura ou elementar consiste em um sólido azulado ou preto (imagem superior), que embora não seja um metal, apresenta rostos brilhantes como se realmente fosse.
É um sólido duro, mas quebradiço, que também exibe uma superfície escamosa se for formada por Polyristales. Por outro lado, o silício amorfo parece um sólido em pó marrom escuro. Graças a isso, é fácil identificar e diferenciar um tipo de silício (cristalino ou poliristalina) de outro (amorfo).
Massa molar
28.085 g/mol
Número atômico (Z)
14 (14Sim)
Ponto de fusão
1414 ºC
Ponto de ebulição
3265 ºC
Densidade
-À temperatura ambiente: 2,33 g/ml
-Bem no ponto de fusão: 2,57 g/ml
Observe que o silício líquido é mais denso que o silício sólido; o que significa que seus cristais flutuarão em uma fase líquida, como no sistema de água gelo. A explicação se deve ao fato de que o espaço interatômico entre os átomos se em seu vidro for maior (menos denso), do que o correspondente no líquido (mais denso).
Calor de fusão
50,21 kJ/mol
Calor de vaporização
383 KJ/mol
Capacidade de calor molar
19.789 J/(mol · k)
Eletro-negatividade
1,90 na escala Pauling
Energias de ionização
-Primeiro: 786,5 kJ/mol
-Segundo: 1577,1 KJ/mol
-Terceiro: 3231,6 KJ/mol
Rádio atômico
111 pm (medido em seus respectivos cristais de diamante)
Condutividade térmica
149 com (M · k)
Resistividade elétrica
2.3 · 103 Ω · m a 20 ºC
Dureza mohs
6.5
Concatenação
Os átomos de silício têm a capacidade de formar links Si-Si simples, que acabam definindo uma corrente (Si-Si-Si ...).
Esta propriedade também é manifestada por carbono e enxofre; No entanto, hibridizações SP3 do silício são mais deficientes em comparação com os dos outros dois elementos e, além disso, seus orbitais 3p são mais difusos; portanto, a sobreposição dos orbitais sp3 resultante é mais fraco.
Pode atendê -lo: reações exotérmicas e endotérmicasAs energias médias das ligações covalentes Si-Si e C-C são 226 kJ/mol e 356 kJ/mol, respectivamente. Portanto, os links Si-se são mais fracos. Por causa disso, o silício não é a pedra angular da vida (nem enxofre). De fato, a cadeia ou esqueleto mais longo que o silício pode formar é geralmente quatro membros (se4).
Números de oxidação
O silício pode ter um dos seguintes números de oxidação, assumindo em cada um deles a existência dos íons com suas respectivas cargas: -4 (sim4-), -3 (sim3-), -2 (sim2-), -1 (sim-), +1 (sim+), +2 (sim2+), +3 (sim3+) e +4 (sim4+). De todos eles, os -4 e +4 são os mais importantes.
Por exemplo, -4 é assumido em siliciuros (mg2Sim ou mg22+Sim4-); enquanto +4 corresponde ao de sílica (SIO2 ou sim4+QUALQUER22-).
Reatividade
O silício é completamente insolúvel em água, além de ácidos ou bases fortes. No entanto, ele se dissolve em uma mistura concentrada de ácidos nítricos e fluorhoréricos (HNO3-HF). Da mesma forma, se dissolve em uma solução alcalina quente, ocorrendo a seguinte reação química:
Sim (s) + 2naoh (AC) + H2Ou (l) => na2SiO3(AC) + 2h2(g)
O metassilicato de sódio, na2SiO3, Também é formado quando o silício se dissolve em carbonato de sódio fundido:
Sim (s) + na2Co3(L) => na2SiO3(L) + c (s)
À temperatura ambiente, não reage com oxigênio, nem mesmo a 900 ° C, quando uma camada vítrea protetora do SIIO começa a se formar2; E então, a 1400 ° C, o silício reage com o nitrogênio do ar para formar uma mistura de nitrilhas, sem e se3N4.
O silício também reage em altas temperaturas com metais para formar siliciuros de metal:
2mg (s) + sim (s) => mg2Sim (s)
2cu (s) + sim (s) => cu2Sim (s)
À temperatura ambiente, reage explosivo e diretamente com halogênios (não há camada sio2 que o protege disso). Por exemplo, você tem a reação de formação do SIF4:
Sim (s) + 2f2(g) => sif4(g)
E embora o silício seja insolúvel na água, o vermelho vivo reage com uma corrente de vapor:
Sim (s) + h2Ou (g) => si2(s) + 2h2(g)
Estrutura e configuração eletrônica
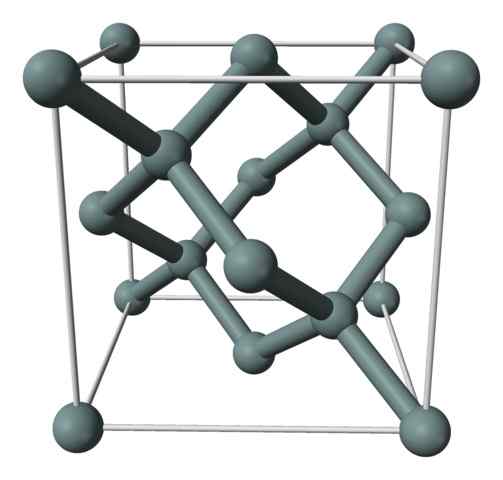 Estrutura cristalina ou a célula unitária do silício representado com um modelo de esferas e barras. Fonte: Benjah-BMM27 [Domínio Público]
Estrutura cristalina ou a célula unitária do silício representado com um modelo de esferas e barras. Fonte: Benjah-BMM27 [Domínio Público] A imagem superior mostra a estrutura cúbica centrada nas faces (FCC), a mesma do diamante, para cristal de silício. As esferas cinza correspondem aos átomos se, como apreciados, estiverem covalentemente ligados um ao outro; Além disso, eles têm ambientes tetraédricos que se reproduzem ao longo do vidro.
O cristal de silício é FCC porque um átomo é observado se localizado em cada uma das faces do cubo (6 × 1/2). Existem também oito átomos se nos vértices do cubo (8 × 1/8) e quatro localizados dentro dele (aqueles que mostram um tetraedro bem definido ao seu redor, 4 × 1).
Disse o acima, cada célula unitária possui um total de oito átomos de silício (3 + 1 + 4, números indicados no parágrafo acima); Característica que ajuda a explicar sua alta dureza e rigidez, porque o silício puro é um cristal covalente e também o diamante.
Caráter covalente
Esse caráter covalente se deve ao fato de que, como carbono, o silício tem quatro elétrons de valência de acordo com sua configuração eletrônica:
[NE] 3s2 3p2
Para vincular, os orbitais puro 3s e 2p são inúteis. É por isso que o Atom cria quatro orbitais híbridos SP3, Com o qual você pode formar quatro ligações covalentes Si-Si e, dessa maneira, completar o octeto de Valência para os dois átomos de silício.
O cristal de silício é então visualizado como uma rede covalente e tridimensional composta por tetraedra interconectada.
No entanto, essa rede não é perfeita, pois apresenta defeitos e limites de grãos, que separam e definem um cristal de outro; E quando esses cristais são muito pequenos e numerosos, se fala de um sólido poliristalino, identificado por seu brilho heterogêneo (semelhante a um mosaico enganado ou prata da superfície).
Condutividade elétrica
Os links Si-IF, com seus elétrons bem localizados,, em princípio, discordam do que é esperado de um metal: um mar de elétrons "molhando" seus átomos; Pelo menos, isso é tão à temperatura ambiente.
Quando a temperatura aumenta, no entanto, o silício começa a acionar eletricidade e, portanto, se comporta como um metal; Isto é, é um elemento metalóide semicondutor.
Silício amorfo
Os tetrahers de silício nem sempre adotam um padrão estrutural, mas podem ser organizados de maneira desordenada; E mesmo, com átomos de silício cujas hibridizações parecem ser sp3 mas sp2, o que contribui para aumentar ainda mais o grau de desordem. Portanto, se fala de um silício amorfo e não -cristalino.
No silício amorfo, há vagas eletrônicas, onde alguns de seus átomos têm um orbital com um elétron desaparecido. Graças a isso, seu próprio hidrogênio sólido lata, dando origem à formação de silício amorfo hidrogenal; Ou seja, ele tem links Si-H, com os quais os tetraedros são concluídos em posições desordenadas e arbitrárias.
Pode atendê -lo: links interatômicosEsta seção é então concluída dizendo que o silício pode ser apresentado em três tipos de sólidos (sem mencionar seu grau de pureza): cristalino, poliristalino e amorfo.
Cada um deles tem seu próprio método ou processo de produção, bem como suas aplicações e dilema ao decidir qual dos três usar, conhecendo suas vantagens e desvantagens.
Onde está e obtenha
 Cristais de quartzo (sílica) são um dos minerais principais e mais extraordinários onde o silício está localizado. Fonte: James St. John (https: // www.Flickr.com/fotos/jsjgeology/22437758830)
Cristais de quartzo (sílica) são um dos minerais principais e mais extraordinários onde o silício está localizado. Fonte: James St. John (https: // www.Flickr.com/fotos/jsjgeology/22437758830) O silício é o sétimo elemento mais abundante do universo, e o segundo na crosta terrestre, também enriquecendo o manto da terra com sua vasta família de minerais. Esse elemento é associado extraordinariamente bem ao oxigênio, formando uma ampla gama de óxidos; Entre eles, sílica, então2, e silicatos (composição química diversificada).
Sílica pode ser vista a olho nu nos desertos e praias, porque a areia é composta principalmente por Sio2. Por sua vez, esse óxido pode se manifestar em alguns polimorfos, sendo os mais comuns: quartzo, ametista, ágata, christobalita, tripoli, coesita, stishovita e thundimita. Além disso, pode ser encontrado em sólidos amorfos, como opalas e terras de diatomea.
Os silicatos, enquanto isso, são ainda mais ricos e quimicamente. Entre alguns dos silicatos, os minerais podem ser mencionados: amianto (branco, café e azul), feldspato, argilas, micies, azeitona, aluminossilicatos, zeólitos, anfibe e piroxenos.
Praticamente, todas as rochas são compostas de silício e oxigênio, com suas ligações estáveis de Si-O, e seus silicatos e silicatos misturados com óxidos metálicos e espécies inorgânicas.
-Redução de sílica
O problema que representa a obtenção de silício é quebrar esse link SI-O, para o qual são necessários fornos especiais e uma boa estratégia de redução. A matéria -prima para esse processo é sílica em forma de quartzo, que se move anteriormente até que seja um pó fino.
A partir desta sílica de solo, pode ser preparada por silício amorfo ou poliristalina.
Silício amorfo
Em pequena escala, feita em laboratório e com as medidas relevantes, a sílica é misturada com poeira de magnésio em um caldeirão e é incinerada na ausência de ar. A próxima reação ocorre então:
SiO2(s) + mg (s) => 2mGo (s) + sim (s) (s) (s)
Magnésio e óxido são eliminados com uma solução diluída de ácido clorídrico. Então, o sólido restante é tratado com ácido fluorhorréico, para que termine de reagir o SIO2 em excesso; Caso contrário, o excesso de magnésio favorece a formação de seu respectivo siliciuro, mg2Sim, composto indesejável para o processo.
O SiO2 Ele se transforma em gás volátil SIF4, que é recuperado para outra síntese química. Finalmente, a massa amorfa de silício é seca sob uma corrente de hidrogênio a gás.
Outro método semelhante para obter o silício amorfo é usar o mesmo SF4 Produzido anteriormente, ou o SICL4 (adquirido anteriormente). Os vapores desses halogenuros de silício são passados sobre sódio líquido em uma atmosfera inerte, de modo que a redução do gás possa ser dada sem a presença de oxigênio:
Sicl4(g) + 4na (l) => Sim (s) + 4nAcl (l)
Curiosamente, com silício amorfo, os painéis solares de alta energia são fabricados.
Silício cristalino
Começando de novo a partir da sílica ou quartzo em pó, eles são levados para um forno de arco elétrico, onde reage com a Coca -Cola. Dessa forma, o agente redutor não é mais um metal, mas um material carbonáceo de alta pureza:
SiO2(s) + 2c (s) => Sim (s) + 2co (g)
Na reação, o carboneto de silício também é produzido, o SIC, que é neutralizado com um excesso de Sio2 (Novamente, o quartzo é excessivamente):
2SIC (s) + sio2(S) => 3SI (S) + 2CO (G)
Outro método para preparar o silício cristalino é usar o alumínio como um agente redutor:
3SIO2(s) + 4al (l) => 3si (s) + 2al2QUALQUER3(S)
E começando do hexafluorurosilicato de potássio, k2[Sif6], também é reagido com alumínio de metal ou potássio para causar o mesmo produto:
K2[Sif6] (l) + 4al (l) => 3si (s) + 6kf (l) + 4fl3(g)
Imediatamente o silício se dissolve no alumínio fundido e, quando o sistema está esfriando, o primeiro cristaliza e se separa do segundo; Ou seja, os cristais de silício são formados, que parecem cores acinzentadas.
Silício poliristalino
Ao contrário da outra síntese ou produções, para obter o silício poliristalino, começa com uma fase gasosa de Silano, SIH4. Esse gás passa por uma pirólise acima de 500 ° C, de forma que ocorra uma decomposição térmica e, portanto, seus vapores iniciais, eles acabam depositando poliristals de silício em uma superfície de semicondutores.
A equação química a seguir exemplifica a reação que ocorre:
Se H4(g) => sim (s) + h2(g)
Obviamente, não deve haver oxigênio na câmara, pois reagiria com o SIH4:
Se H4(g) + 2º2(g) => sio2(s) + 2h2O (G)
E a espontaneidade da reação de combustão é tal, que ocorre rapidamente à temperatura ambiente no rosto.
Outra via sintética para produzir esse tipo de parte do silício do silício cristalino como matéria -prima. Eles o fazem reagir com cloreto de hidrogênio a uma temperatura em torno de 300 ° C, de modo que o triclorosilano seja formado:
Pode atendê -lo: ferro (elemento): características, estrutura química, usosSim (s) + 3hcl (g) => sicl3H (g) + h2(g)
E o sicl3H reage a 1100 ºC para regenerar o silício, mas agora poliristalina:
4sicl3H (g) => sim (s) + 3sicl4(g) + 2h2(g)
Basta ver as equações para dar uma idéia de trabalho e parâmetros de produção rigorosos que devem ser considerados.
Isótopos
O silício é natural e principalmente como o isótopo 28Sim, com uma abundância de 92,23%.
Além disso, existem outros dois isótopos que são estáveis e, portanto, não sofrem decaimento radioativo: o 29Sim, com uma abundância de 4,67%; e 30Sim, com uma abundância de 3,10%. Sendo tão abundante 28Sim, não é de surpreender que o peso atômico do silício seja 28.084 u.
O silício também pode estar em vários radioisótopos, entre os quais o 31Sim (t1/2= 2,62 horas) e 32Sim (t1/2= 153 anos). Os demais (22Sim - 44Sim têm t1/2 muito curto ou breve (menos de centésimos de segundos).
Riscos
O silício puro é uma substância relativamente inerte, por isso geralmente não se acumula em nenhum órgão ou tecido, desde que a exposição a ela seja baixa. Na forma de poeira, pode causar irritações para os olhos, causando lágrimas ou vermelhidão, enquanto tocá -la pode causar desconforto na pele, coceira e descascamento.
Quando a exposição é muito alta, o silício pode prejudicar os pulmões; Mas sem efeitos subsequentes, a menos que a quantidade seja suficiente para causar asfixia. No entanto, isso não acontece com o quartzo, que está associado a câncer de pulmão e doenças como bronquite e enfisema.
Da mesma forma, o silício puro é muito raro de natureza, e seus compostos, tão abundantes na crosta terrestre, não representam nenhum risco para o meio ambiente.
Agora, com relação aos órgãos, estes podem ser tóxicos; Mas ter muitos deles depende de qual deles está sendo considerado, assim como outros fatores (reatividade, pH, mecanismo de ação, etc.).
Formulários
Indústria de construção
Os minerais de silício integram a "pedra" com os quais edifícios, casas ou monumentos são construídos. Por exemplo, cimentos, concreto, estuque e tijolos refratários, consistem em misturas sólidas com base em silicatos. A partir dessa abordagem, pode -se parecer o utilitário que esse elemento tem nas cidades e arquitetura.
Vidro e cerâmica
Da sílica, os cristais usados em dispositivos ópticos podem ser fabricados, seja como isoladores, células para amostras de espectrofotômetros, cristais piezoelétricos ou meros óculos.
Além disso, quando o material é preparado com múltiplos aditivos, acaba se transformando em um sólido amorfo, bem conhecido como vidro; e montanhas de areia são geralmente a fonte de sílica ou quartzo necessários para sua produção. Por outro lado, com os silicatos de cerâmica e porcelana são fabricados.
Idéias entrelaçadas, Silicon também está presente em artesanato e ornamentações.
Ligas
Os átomos de silício podem coesos e ser miscíveis com uma matriz de metal, por isso é um aditivo para inúmeras ligas ou metais; Por exemplo, aço, para fabricar núcleos magnéticos; bronzes, para a fabricação de cabos telefônicos; e alumínio, na produção de liga de alumínio-solicio para peças automotivas leves.
Portanto, não apenas pode ser encontrado na "pedra" dos edifícios, mas também nos metais de suas colunas.
Desiclantes
 Bolas de sílica gelatinosa, usadas como dessecantes. Fonte: Desiclantes [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]
Bolas de sílica gelatinosa, usadas como dessecantes. Fonte: Desiclantes [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)] A sílica, na forma de gel ou amorfa, permite fabricar sólidos que atuam como dessecantes ao capturar as moléculas de água que entram no recipiente e mantêm seu interior seco.
Indústria eletrônica
 Silício poliristal e amorfo são usados para a fabricação de painéis solares. Fonte: pxhere.
Silício poliristal e amorfo são usados para a fabricação de painéis solares. Fonte: pxhere. Camadas de silício de diferentes espessuras e cores fazem parte dos chips de computador, bem como com seus sólidos (cristalinos ou amorfos), circuitos integrados e células solares foram projetadas.
Sendo um semicondutor, os átomos são incorporados com menos (Al, B, GA) ou mais elétrons (P, como, SB) para transformá -lo em semicondutores de tipo p qualquer n, respectivamente. Com dois sindicatos de silicios, um n e o outro p, Diodos de emissores de luz são fabricados.
Polímeros de silicone
A famosa cola de silicone consiste em um polímero orgânico apoiado pela estabilidade das correntes dos links Si-O-Si ... se essas cadeias forem muito longas, curtas ou reticuladas, as propriedades da mudança de polímero de silicone, bem como seus Aplicações finais.
Entre seus usos, o seguinte pode ser mencionado abaixo:
-Cola ou adesivos, não apenas para ingressar em papéis, mas blocos de construção, borrachas, painéis de vidro, pedras, etc.
-Lubrificantes em sistemas de frenagem hidráulica
-Reforça as pinturas e melhora o brilho e a intensidade de suas cores, ao mesmo tempo que permite resistir às mudanças de temperatura sem rachaduras ou carrosse
-Eles são usados como sprays repelentes de água, que permanecem secos algumas superfícies ou objetos
-Eles fornecem produtos de higiene pessoal (massas dentárias, shampoo, géis, cremes de barbear, etc.) A sensação de ser sedoso
-Seus revestimentos protegem os componentes eletrônicos de dispositivos delicados de calor e umidade, como microprocessadores
-Com polímeros de silicone, várias das bolas de borracha que saltam mal são derrubadas no chão.
Referências
- Shiver & Atkins. (2008). Química Inorgânica. (Quarta edição). Mc Graw Hill.
- Wikipedia. (2019). Silício. Recuperado de: em.Wikipedia.org
- Microquímicos. (s.F.). Cristalografia do silício. Recuperado de: microcímicos.com
- Lentech b.V. (2019). Tabela de período: silício. Recuperado de: lentech.com
- Marques Miguel. (s.F.). Silício ocorre. Recuperado de: Nautilus.Fis.Uc.Pt
- Mais hemant. (5 de novembro de 2017). Silício. Recuperado de: Hemantmore.org.em
- Pilgaard Michael. (22 de agosto de 2018). Silício: ocorrência, isolamento e síntese. Recuperado de: pilgaardelegs.com
- Dr. Doug Stewart. (2019). Fatos do elemento de silício. Chemicool. Recuperado de: Chemicool.com
- Christiana Honsberg e Stuart Bowden. (2019). Uma coleção de recursos para o educador fotovoltaico. Pveducation. Recuperado de: Pveducation.org
- American Chemistry Council, Inc. (2019). Silicones na vida cotidiana. Recuperado de: SEHSC.AmeriCachemistry.com
- « Estratégias de distribuição Tipos e exemplos
- Tipos de estratégia de produto, como é feito e exemplo »

