Renio Discovery, Propriedades, Estrutura, Usos

- 2860
- 246
- Pete Wuckert
Ele Renio É um elemento metálico cujo símbolo químico está e está localizado no grupo 7 da tabela periódica, duas posições abaixo do manganês. Compartilhe com isso e a propriedade da Techecio de vários números ou estados de oxidação, de +1 a +7. Além disso, forma um ânion chamado Perrenato, preso4-, Análogo ao permanganato, MNO4-.
Este metal é um dos mais raros e escassos de natureza, então seu preço é alto. É extraído como um subproduto de molibdênio e mineração de cobre. Uma das propriedades mais relevantes do Renio é o seu alto ponto de fusão, mal superado por carbono e tungstênio, e sua grande densidade, sendo o dobro da de chumbo.
 Esfera de metal Renio. Fonte: imagens de alta resolução de elementos químicos/cc por (https: // criativecommons.Org/licenças/por/3.0)
Esfera de metal Renio. Fonte: imagens de alta resolução de elementos químicos/cc por (https: // criativecommons.Org/licenças/por/3.0) Sua descoberta tem nuances controversas e infelizes. O nome de 'Renio' deriva da palavra latina 'Rhenus', que significa Rin, o famoso rio alemão perto do local onde os químicos alemães que isolaram e identificaram esse novo elemento funcionou.
Renio tem numerosos usos, entre os quais o refinamento da octana de gasolina está.
[TOC]
Descoberta
A existência de dois elementos pesados com características químicas semelhantes às do manganês já estavam prevendo desde o 1869, através da tabela periódica do químico russo Dmitri Mendeleev. No entanto, não se sabia como seus números atômicos deveriam ser; E foi aqui em 1913 quando a previsão do físico inglês Henry Moseley foi introduzido.
Segundo Moseley, esses dois elementos pertencentes ao grupo de manganês devem ter números atômicos 43 e 75.
Alguns anos antes, no entanto, o químico japonês Masataka Ogawa havia descoberto o suposto elemento 43 em uma amostra de mineral torianita. Depois de anunciar seus resultados em 1908, ele queria batizar esse elemento com o nome de 'Niponio'. Infelizmente, os químicos da época mostraram que Ogawa não havia descoberto o elemento 43.
Pode servir a você: Cycloalques: estrutura química, propriedades, nomenclaturaE assim, outros anos se passaram quando, em 1925, três químicos alemães: Walter Noddack, Ida Noddack e Otto Berg, encontraram elemento 75 em Amostras de Mineral de Columbita, Gadolinita e Molibdenita. Isso deu a ele o nome de Renio, em homenagem ao Rin Rin da Alemanha ('Rhenus', em latim).
O erro de Masataka Ogawa foi ter dispensado a identificação do elemento: ele descobriu Renio, não o elemento 43, chamado Tecnecio hoje.
Renio Properties
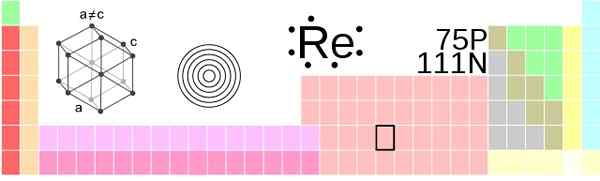 Situação de Renio na tabela periódica. !Original: Ahoteseiervector: Sushant Savla/CC BY-S (https: // criativeCommons.Org/licenças/BY-SA/3.0)
Situação de Renio na tabela periódica. !Original: Ahoteseiervector: Sushant Savla/CC BY-S (https: // criativeCommons.Org/licenças/BY-SA/3.0) Aparência física
Renio geralmente é comercializado na forma de pó cinzento. Suas peças de metal, geralmente gotas esféricas, são cinza prateado, que também são altamente brilhantes.
Massa molar
186.207 g/mol
Número atômico
75
Ponto de fusão
3186 ºC
Ponto de ebulição
5630 ºC
Densidade
-À temperatura ambiente: 21.02 g/cm3
-Bem no ponto de fusão: 18,9 g/cm3
Renio é um metal quase duas vezes mais denso do que o mesmo líder. Assim, uma esfera de Renio que pesa 1 grama pode ser equiparada a um cristal de chumbo robusto da mesma massa.
Eletro-negatividade
1.9 na escala Pauling
Energias de ionização
Primeiro: 760 kJ/mol
Segundo: 1260 kJ/mol
Terceiro: 2510 KJ/mol/mol
Capacidade de calor molar
25.48 J/(mol · k)
Condutividade térmica
48,0 W/(M · K)
Resistividade elétrica
193 Nω · M
Dureza mohs
7
Isótopos
Os átomos de Renio são apresentados na natureza como dois isótopos: 185Re, com uma abundância de 37,4%; e 187Re, com uma abundância de 62,6%. Renio é um daqueles elementos cujo isótopo mais abundante é radioativo; No entanto, o tempo de meia -vida de 187Re é muito grande (4,12 · 1010 anos), então é praticamente considerado estável.
Pode atendê -lo: níquel: história, propriedades, estrutura, usos, riscosReatividade
Renio metálico é um material resistente a oxidar. Quando ele faz, seu óxido, re2QUALQUER7, É volatilizado em altas temperaturas e queimaduras com uma chama verde amarelada. As peças de Renio resistem ao ataque de Hno3 concentrado; Mas quente, dissolve -se para gerar ácido rênico e dióxido de nitrogênio, que coloram a solução:
Re + 7hno3 → Hreo4 + 7 não2 + 3h2QUALQUER
A química de Renio é vasta, porque é capaz de formar compostos com um amplo espectro de números de oxidação, além de estabelecer uma ligação quadrupolo entre dois átomos de Renio (quatro ligações covalentes).
Estrutura e configuração eletrônica
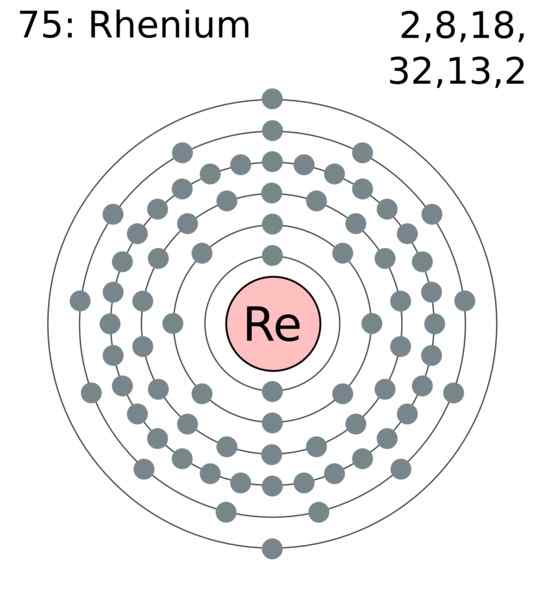 Camada de elétrons Renio. Autor: Usuário: Gregrobson (Greg Robson). Wikimedia Commons
Camada de elétrons Renio. Autor: Usuário: Gregrobson (Greg Robson). Wikimedia Commons Os átomos de Renio são agrupados em seus cristais para causar uma estrutura hexagonal compacta, HCP, que é caracterizada por ser muito densa. Isso concorda com o fato de ser um metal de grande densidade. O link metálico, produto da sobreposição de seus orbitais externos, mantém os átomos fortemente coesos.
Neste link metálico, re-re-re, os elétrons de Valência participam, que estão de acordo com a configuração eletrônica:
[Xe] 4f14 5 d5 6s2
Em princípio, são os orbitais 5d e 6s que se sobrepõem para compactar os átomos de ReS na estrutura do HCP. Observe que seus elétrons adicionam um total de 7, correspondendo ao número do seu grupo na tabela periódica.
Números de oxidação
A configuração eletrônica da Renio, uma vez vislumbres, que seu átomo é capaz de perder até 7 elétrons, para se tornar o cátion hipotético re7+. Quando a existência do Re é assumida7+ Em qualquer composto Renio, por exemplo, no re2QUALQUER7 (Ré27+QUALQUER72-), Diz -se que possui um número de oxidação de +7, re (vii).
Outros números de oxidação positiva para Renio são: +1 (re+), +2 (re2+), +3 (re3+) E assim por diante para +7. Da mesma forma, Renio pode ganhar elétrons se tornando um ânion. Nesses casos, diz -se que ele tem um número de oxidação negativo: -3 (re3-), -2 (re2-) e -1 (re-).
Pode servir a você: hidrólise: o que é e exemplos de reaçõesFormulários
Gasolina
Renio, juntamente com a platina, é usado para criar catalisadores que aumentam o grau de octana da gasolina, enquanto diminuem seu conteúdo de chumbo. Por outro lado, os catalisadores da Renio são destinados a múltiplas reações de hidrogenação, devido à sua resistência ao envenenamento por nitrogênio, fósforo e enxofre.
Superleações refratárias
Renio é um produto de metal refratário de seu alto ponto de fusão. É por isso que as ligas de níquel são adicionadas para transformá -las refratárias e resistentes a grandes pressões e temperaturas. Essas superleações são usadas principalmente para o design de turbinas e motores para navios aeroespaciais.
Filamentos de tungstênio
Renio também pode formar ligas com tungstênio, o que melhora sua ductilidade e, portanto, facilita a fabricação de filamentos. Esses filamentos de Renio-Tungstênio são usados como fontes de raios-X e para o design de termos de termos capazes de medir as temperaturas de até 2200 ° C.
Da mesma forma, esses filamentos de Renio foram usados uma vez para câmeras arcaicas e atualmente para lâmpadas sofisticadas de equipamentos; como espectrofotômetro de massa.
Referências
- Shiver & Atkins. (2008). Química Inorgânica. (Quarta edição). Mc Graw Hill.
- Sarah Pierce. (2020). Rhenium: Uso, História, Fatos e Isotopos. Estudar. Recuperado de: estudo.com
- Centro Nacional de Informações sobre Biotecnologia. (2020). Rhenium. Banco de dados PubChem., CID = 23947. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Wikipedia. (2020). Rhenium. Recuperado de: em.Wikipedia.org
- Dr. Doug Stewart. (2020). Fatos do elemento do Rhenium. Recuperado de: Chemicool.com
- Eric Scerri. (18 de novembro de 2008). Rhenium. Química em seus elementos. Recuperado de: químicaworld.com

