Modelo Atômico de Heisenberg
- 1857
- 528
- Melvin Mueller
O que é o modelo atômico de Heisenberg?
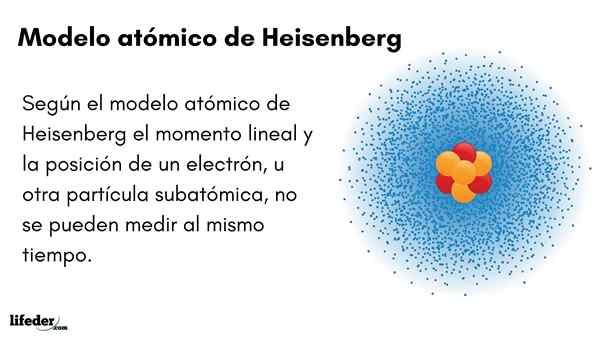
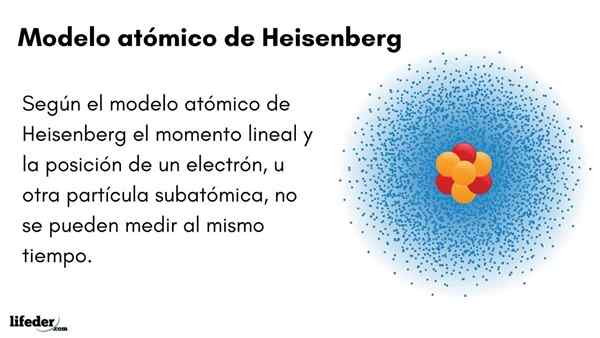
Ele Modelo Atômico de Heisenberg (1927) apresenta o princípio da incerteza em orbitais de elétrons em torno do núcleo atômico. O excelente físico alemão estabeleceu os fundamentos da mecânica quântica para estimar o comportamento de partículas subatômicas que compõem um átomo.
O princípio da incerteza de Werner Heisenberg indica que não é possível saber com certeza a posição linear de um elétron ao mesmo tempo. O mesmo princípio se aplica às variáveis de tempo e energia; Ou seja, se tivermos uma indicação sobre a posição do elétron, ignoraremos o momento linear do elétron e vice -versa.
Em resumo, não é possível prever simultaneamente o valor de ambas as variáveis. O exposto acima não implica que nenhuma das magnitudes mencionadas anteriormente não possa ser conhecida com precisão. Sempre que é separadamente, não há impedimento para obter o valor do interesse.
No entanto, a incerteza ocorre quando se trata de conhecer simultaneamente duas magnitudes conjugadas, como é o caso da posição linear e do momento.
Esse princípio surge devido ao raciocínio estritamente teórico, como a única explicação viável para dar motivos sobre observações científicas.
Características do modelo atômico de Heisenberg
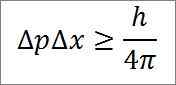 Werner Heisenberg
Werner Heisenberg Em março de 1927, Heisenberg publicou seu trabalho Sobre o conteúdo perceptivo da cinemática e mecânica quântica, onde ele detalhou o princípio da incerteza ou indeterminação.
Esse princípio, fundamental no modelo atômico proposto por Heisenberg, é caracterizado pelo seguinte:
- O princípio da incerteza surge como uma explicação que complementa as novas teorias atômicas sobre o comportamento dos elétrons. Apesar de usar instrumentos de medição com alta precisão e sensibilidade, a indeterminação ainda está presente em qualquer estudo experimental.
- Devido ao princípio da incerteza, ao analisar duas variáveis relacionadas, se você tiver um conhecimento preciso de um deles, a indeterminação sobre o valor da outra variável estará aumentando.
- O momento linear e a posição de um elétron, ou outra partícula subatômica, não podem ser medidos ao mesmo tempo.
- A relação entre ambas as variáveis é dada por uma desigualdade. De acordo com Heisenberg, o produto das variações do momento linear -3. 4 Jules x segundos) e 4π, conforme detalhado na seguinte expressão matemática:
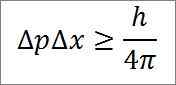
A lenda correspondente a esta expressão é a seguinte:
∆P: indeterminação do momento linear.
∆x: indeterminação da posição.
H: Plank Constant.
π: PI 3.14 Número.
- Em vista do exposto, o produto das incertezas tem como menor parada do relacionamento h/4π, que é um valor constante. Portanto, se uma das magnitudes tende a zero, o outro deve aumentar na mesma proporção.
- Esse relacionamento é válido para todos os pares de magnitudes canônicas conjugadas. Por exemplo: o princípio da incerteza de Heisenberg é perfeitamente aplicável à dupla de tempo de energia, conforme detalhado abaixo:
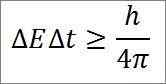
Nesta expressão:
∆E: indeterminação de energia.
∆t: indeterminação do tempo.
H: Plank Constant.
π: PI 3.14 Número.
- A partir deste modelo, segue -se que o determinismo causal absoluto em variáveis canônicas conjugadas é impossível, uma vez que estabeleça essa relação, o conhecimento dos valores iniciais das variáveis do estudo deve ser estabelecido.
- Consequentemente, o modelo Heisenberg é baseado em formulações probabilísticas, devido à aleatoriedade que existe entre as variáveis para os níveis subatômicos.
Testes experimentais
Heisenberg's uncertainty principle arises as the only possible explanation to the experimental tests that took place during the first three decades of the 21st century.
Antes de Heisenberg enunciar o princípio da incerteza, os preceitos em vigor sugeriram que as variáveis de momento linear, momento angular, tempo, energia, entre outros, para as partículas subatômicas, elas foram definidas operacionalmente.
Isso significava que eles eram tratados como se fossem física clássica; Ou seja, um valor inicial foi medido e o valor final foi estimado de acordo com o procedimento pré -estabelecido.
Pode atendê -lo: magnitude do vetorO exposto acima significava definir um sistema de referência para medições, o instrumento de medição e a forma de uso do referido instrumento, de acordo com o método científico.
De acordo com isso, as variáveis descritas por partículas subatômicas tiveram que se comportar determinísticas. Isto é, seu comportamento deve ser previsto exato e precisamente.
No entanto, toda vez que um ensaio dessa natureza era realizado, era impossível obter na medição o valor estimado teoricamente.
As medidas foram deturpadas devido às condições naturais do experimento, e o resultado obtido não foi útil para enriquecer a teoria atômica.
Exemplo
Por exemplo: se se trata de medir a velocidade e a posição de um elétron, a montagem do experimento deve contemplar o choque de um fóton de luz com o elétron.
Esta colisão induz uma variação na velocidade e posição intrínsecas do elétron, para que o objeto da medição seja alterado por condições experimentais.
Portanto, o pesquisador incentiva a ocorrência de um erro experimental inevitável, apesar da precisão e precisão dos instrumentos utilizados.
Mecânica quântica diferente de mecânica clássica
Além disso, o princípio da indeterminação de Heisenberg afirma que, por definição, a mecânica quântica funciona de maneira diferente em relação à mecânica clássica.
Consequentemente, supõe -se que o conhecimento preciso das medidas subatômicas seja limitado pela linha fina que separa a mecânica clássica e quântica.
Limitações do modelo de Heisenberg
Apesar de explicar a indeterminação de partículas subatômicas e sentar as diferenças entre a mecânica clássica e quântica, o modelo atômico de Heisenberg não estabelece uma equação única para explicar a aleatoriedade desse tipo de fenômeno.
Pode servir a você: energia gravitacional: fórmulas, características, aplicações, exercíciosAlém disso, o fato de o relacionamento ser estabelecido através de uma desigualdade implica que a gama de possibilidades para o produto de duas variáveis canônicas conjugadas é indeterminada. Consequentemente, a incerteza inerente aos processos subatômicos é significativa.
Artigos de interesse
Modelo Atômico de Schrödinger.
Modelo Atômico de Broglie.
Modelo Atômico de Chadwick.
Modelo atômico de perrina.
Modelo Atômico de Thomson.
Modelo atômico de Dalton.
Modelo Atômico Dirac Jordan.
Modelo Atômico do Demócrito.
Modelo Atômico de Leucipo.
Modelo atômico Bohr.
Modelo Atômico Sommerfeld.
Modelo atômico atual.
Referências
- Beyler, r. (1998). Werner Heisenberg. Encyclopædia Britannica, Inc. Recuperado de: Britannica.com
- Princípio da incerteza de Heisenberg (S.F.). Recuperado de: hiru.EUS
- Garcia, J. (2012). Princípio da incerteza de Heisenberg. Recuperado de: hiberus.com
- Modelos atômicos (S.F.). Universidade Nacional Autônoma do México. Cidade do México, México. Recuperado de: Advisory.Cuautitlan2.Unam.mx
- Werner Heisenberg (S.F.).Recuperado de: o History-Off-tom.Wikispaces.com
- Wikipedia, Enciclopédia Livre (2018). Prancha constante. Recuperado de: é.Wikipedia.org
- Wikipedia, Enciclopédia Livre (2018). Relacionamento da indeterminação de Heisenberg. Recuperado de: é.Wikipedia.org

