Definição de massa atômica, tipos, como calculá -la, exemplos
- 4809
- 683
- Melvin Mueller
O massa atômica É a quantidade de matéria presente em um átomo, que pode ser expresso em unidades físicas comuns ou em unidades de massa atômica (Uma ou U). Um átomo está vazio em quase toda a sua estrutura; elétrons que são borrados em regiões chamadas orbital, onde há uma certa probabilidade de encontrá -las e seu núcleo.
No núcleo do átomo, há prótons e nêutrons; O primeiro com cargas positivas, enquanto os segundos com carga neutra. Essas duas partículas subatômicas têm uma massa muito maior que a do elétron; Portanto, a massa de um átomo é governada por seu núcleo e não pelo vazio ou por elétrons.
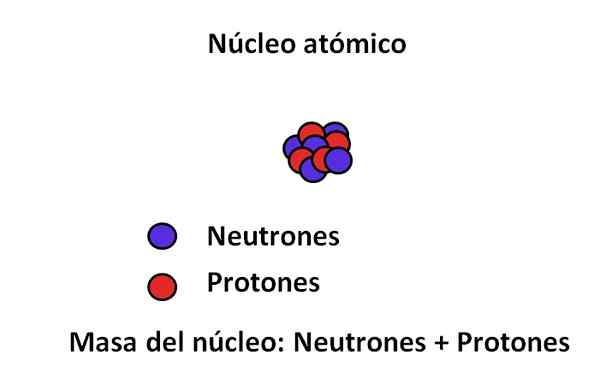
 As principais partículas subatômicas e a massa do núcleo. Fonte: Gabriel Bolívar.
As principais partículas subatômicas e a massa do núcleo. Fonte: Gabriel Bolívar. A massa de um elétron é de aproximadamente 9,1,10-31 kg, enquanto o próton 1.67 · 10-27 kg, sendo a proporção de massa de 1.800; isto é, um próton "pesa" 1.800 vezes mais do que um elétron. Da mesma forma, o mesmo acontece com as massas de nêutrons e elétrons. É por isso que a contribuição em massa do elétron para fins comuns é considerada insignificante.
Por esse motivo, geralmente se supõe que a massa do átomo, ou massa atômica, depende apenas da massa do núcleo; que, por sua vez, consiste na soma do assunto de nêutrons e prótons. A partir desse raciocínio, dois conceitos surgem: número de massa e massa atômica, ambos intimamente relacionados.
Tendo tanta "vazia" em átomos e, como sua massa é quase inteiramente o núcleo, espera -se que este último seja extraordinariamente denso.
Se levássemos esse vazio a qualquer corpo ou objeto, suas dimensões seriam drasticamente. Além disso, se pudéssemos construir um pequeno objeto baseado em núcleos atômicos (sem elétrons), isso teria uma massa de milhões de toneladas.
Por outro lado, as massas atômicas ajudam a distinguir diferentes átomos do mesmo elemento; Estes são, os isótopos. Tendo isótopos mais abundantes do que outros, uma média das massas átomos para um determinado elemento deve ser estimada; média que pode variar de planeta no planeta, ou de uma região espacial para outra.
[TOC]
Definição e conceito

Por definição, a massa atômica é a soma das massas de seus prótons e nêutrons expressos com uma ou u. O número resultante (também chamado número de massa) é colocado sem dimensão no canto superior esquerdo na notação usada para nucleids. Por exemplo, para o elemento quinzeX sua massa atômica é 15um ou 15u.
A massa atômica não pode dizer muito sobre a verdadeira identidade deste elemento x. Em vez disso, o número atômico é usado, o que corresponde aos prótons que abriga o núcleo de x. Se esse número for 7, a diferença (15-7) será igual a 8; isto é, x tem 7 prótons e 8 nêutrons, cuja soma é 15.
Voltando à imagem, o núcleo possui 5 nêutrons e 4 prótons; portanto, seu número de massa é 9; E por sua vez 9 Uma é a massa de seu átomo. Tendo 4 prótons e consultando a tabela periódica, pode -se observar que esse núcleo corresponde ao elemento do berílio, seja (ou 9SER).
Unidade de massa atômica
Os átomos são pequenos demais para medir suas massas através de métodos convencionais ou escalas comuns. É por esse motivo que o Uma, ou o da (daltón) foi inventado. Essas unidades criadas para átomos permitem que você tenha uma idéia de quão enormes os átomos de um elemento são em relação um ao outro.
Pode atendê -lo: cobalto: estrutura, propriedades, aplicaçõesMas o que exatamente um Uma representa? Deve haver uma referência que permita que você estabeleça relacionamentos em massa. Para fazer isso, o átomo foi usado como referência 12C, que é o isótopo mais abundante e estável para carbono. Tendo 6 prótons (seu número atômico Z) e 6 nêutrons, sua massa atômica, portanto, é 12.
Supõe -se que prótons e nêutrons tenham as mesmas massas, para que cada contribuição 1 Uma. A unidade de massa atômica é então definida como a parte doze (1/12) da massa um átomo de carbono-12; Isto é, a massa de um próton ou nêutron.
Equivalência em gramas
E agora surge a seguinte pergunta: quantos gramas são equivalentes a 1 uma? Como a princípio não havia técnicas avançadas o suficiente para medi -lo, os produtos químicos tiveram que se contentar em expressar todas as massas com uma; No entanto, isso foi uma vantagem e não uma desvantagem.
Porque? Por ser as pequenas partículas subatômicas, assim quando criança, deve ser a massa deles expressa em gramas. De fato, 1 Uma é equivalente a 1.6605 · 10-24 gramas. Além disso, com o uso do conceito de mol, não foi um problema trabalhar as massas dos elementos e seus isótopos com uma, sabendo que essas unidades poderiam ser modificadas para g/mol.
Por exemplo, retornando para quinzex e 9Ser, temos que suas massas atômicas são 15 Uma e 9 Uma, respectivamente. Como essas unidades são tão pequenas e não dizem quanto é a matéria que se deve "pesar" para manipulá -las, elas se transformam em suas respectivas massas molares: 15 g/mol e 9 g/mol (introduzindo os conceitos de moles e número Avogadro).
Massa atômica média
Nem todos os átomos do mesmo elemento têm a mesma massa. Isso significa que eles devem ter mais partículas subatômicas no núcleo. Sendo o mesmo elemento, o número atômico ou o número de prótons deve permanecer constante; Portanto, há apenas variação nas quantidades de nêutrons que possuem.
Assim, parece da definição de isótopos: átomos do mesmo elemento, mas com diferentes massas atômicas. Por exemplo, o berílio consiste quase inteiramente no isótopo 9Estar, com traços de traços 10Ser. No entanto, este exemplo não ajuda muito a entender o conceito de massa atômica média; Precisamos de um com mais isótopos.
Exemplo
Suponha que o elemento exista 88J, sendo este o principal isótopo de j com uma abundância de 60%. J Além disso, tem outros dois isótopos: 86J, com uma abundância de 20%, e 90J, com uma abundância também 20%. Isso significa que, de 100 J átomos que coletamos na Terra, 60 deles são 88J e os 40 restantes uma mistura de 86J e 90J.
Cada um dos três isótopos de J tem sua própria massa atômica; isto é, sua soma de nêutrons e prótons. No entanto, essas massas devem ser calculadas para poder ter um átomo uma massa atômica para J; Aqui na terra, já que pode haver outras regiões do universo onde a abundância de 86J é 56% e não 60%.
Pode atendê -lo: sódio: história, estrutura, propriedades, riscos e usosPara calcular a massa atômica média de J, a média ponderada das massas de seus isótopos deve ser obtida; isto é, levando em consideração a porcentagem de abundância para cada um deles. Assim temos:
Massa média (j) = (86 Uma) (0,60) + (88 Uma) (0,20) + (90 Uma) (0,20)
= 87.2 Uma
Isto é, a massa atômica média (também conhecida como j é 87,2 Uma. Enquanto isso, sua massa molar é 87,2 g/mol. Observe que 87,2 está mais próximo que 88 que 86 e também está distante de 90.
Massa atômica absoluta
A massa atômica absoluta é a massa atômica expressa em gramas. A partir do exemplo do elemento hipotético, podemos calcular sua massa atômica absoluta (a média), sabendo que cada Uma é equivalente a 1.6605,10-24 gramas:
Massa atômica absoluta (j) = 87,2 Uma * (1.6605 · 10-24 g/ Uma)
= 1.447956 · 10-22 g/átomo j
Isso significa que, em média, J átomos têm uma massa absoluta de 1.447956 · 10-22 g.
Massa atômica relativa
A massa atômica relativa é idêntica à massa atômica média para um determinado elemento; No entanto, ao contrário do segundo, o primeiro carece de unidade. Portanto, não tem dimensão. Por exemplo, a massa atômica média de berílio é 9.012182 U; enquanto sua massa atômica relativa é simplesmente 9.012182.
É por isso que às vezes esses conceitos geralmente entendem mal como sinônimos, pois são muito semelhantes e as diferenças entre eles são sutis. Mas quais são essas massas relativas? Em relação à parte doze da massa do 12C.
Assim, um elemento com uma massa atômica relativa de 77 significa que possui uma massa 77 vezes maior que 1/12 parte do 12C.
Aqueles que ganharam os elementos na tabela periódica podem ver que suas massas são expressas relativamente. Eles não têm unidades Uma e é interpretada como: o ferro tem uma massa atômica de 55.846, o que significa que é 55.846 vezes mais maciço que a massa de 1/12 parte do 12C, e isso também pode ser expresso como 55.846 Uma ou 55.846 g/mol.
Como calcular a massa atômica
Matematicamente um exemplo de como calculá -lo com o exemplo do elemento j. Em termos gerais, a fórmula média ponderada deve ser aplicada, que seria:
P = σ (massa atômica isótopo) (abundância em decimais)
Em outras palavras, ter as massas atômicas (nêutrons + prótons) de cada isótopo (natural comum) para um determinado elemento, bem como suas respectivas abundâncias terrestres (ou qualquer que a região considerada), então a média ponderada pode ser calculada.
E por que não simplesmente a média aritmética? Por exemplo, a massa atômica média de J é 87,2 Uma. Se calcularmos essa massa novamente, mas de uma maneira aritmética, teremos:
Massa média (j) = (88 Uma + 86 Uma + 90 Uma)/3
= 88 Uma
Observe que há uma diferença importante entre 88 e 87,2. Isso ocorre porque na média aritmética supõe -se que a abundância de todos os isótopos seja a mesma; Quando há três isótopos J, cada um deve ter uma abundância de 100/3 (33,33%). Mas não é realmente: existem isótopos muito mais abundantes do que outro.
Pode atendê -lo: uretano: estrutura, propriedades, obtenção, usosÉ por isso que a média ponderada é calculada, pois é levada em consideração o quão abundante é um isótopo em relação a outro.
Exemplos
Carbono
Para calcular a massa atômica média de carbono, precisamos de seus isótopos naturais com suas respectivas abundâncias. No caso de carbono, estes são: 12C (98,89%) e 13C (1,11%). As massas atômicas relativas deles são 12 e 13, respectivamente, que por sua vez são iguais a 12 Uma e 13 Uma. Resolução:
Massa atômica média (c) = (12 um) (0,9889) + (13 Uma) (0,0111)
= 12.0111 Uma
Portanto, a massa de um átomo de carbono é em média 12,01 uma. Tendo quantidades de traços de 14C, quase não tem influência nessa média.
Sódio
Todos os átomos de sódio terrestre consistem no isótopo 23Na, então sua abundância é 100%. Por isso, em cálculos comuns, pode -se supor que sua massa é simplesmente 23 Uma ou 23 g/mol. No entanto, sua massa exata é 22.98976928 Uma.
Oxigênio
Os três isótopos de oxigênio com suas respectivas abundâncias são: 16O (99.762%), 17Ou (0,038%) e 18O (0,2%). Temos tudo para calcular sua massa atômica média:
Massa atômica média (o) = (16 Uma) (0,99762) + (17 Uma) (0,00038) + (18 Uma) (0,002)
= 16.00438 Uma
Embora sua massa exata relatada seja realmente 15.9994 Uma.
Azoto
Repetindo os mesmos passos com oxigênio que temos: 14N (99.634%) e quinzeN (0,366%). Então:
Massa atômica média (n) = (14 Uma) (0,99634) + (15 Uma) (0,00366)
= 14.00366 Uma
Observe que a massa relatada para o nitrogênio é de 14.0067 uma, um pouco maior do que o que calculamos.
Cloro
Os isótopos de cloro com suas respectivas abundâncias são: 35Cl (75,77%) e 37Cl (24,23%). Calculando sua massa atômica média que temos:
Massa atômica média (cl) = (35 Uma) (0,7577) + (37 Uma) (0,2423)
= 35.4846 Uma
Muito semelhante ao relatório (35.453 Uma).
Disposio
E, finalmente, a massa média de um elemento com muitos isótopos naturais será calculada: Disposio. Estes e com suas respectivas abundâncias são: 156DY (0,06%), 158DY (0,10%), 160DY (2,34%), 161Dy (18,91%), 162DY (25,51%), 163DY (24,90%) e 164DY (28,18%).
Procedemos como os exemplos anteriores para calcular a massa atômica deste metal:
Massa atômica média (DY) = (156 Uma) (0,0006%) + (158 Uma) (0,0010) + (160 UMA) (0,0234) + (161 UMA) (0,1891) + (162 AMA) (0,2551) + (163 Uma) (0,2490) + (164 Uma) (0,2818)
= 162.5691 Uma
A massa relatada é 162.500 Uma. Observe que essa média é entre 162 e 163, já que os isótopos 156Dy, 158Dy e 160Dy são poucos abundantes; enquanto aqueles que predominam são 162Dy, 163Dy e 164Dy.
Referências
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- Wikipedia. (2019). Massa atômica. Recuperado de: em.Wikipedia.org
- Christopher Masi. (s.F.). Massa atômica. Recuperado de: WSC.Massa.Edu
- Natalie Wolchover. (12 de setembro de 2017). Como você pesa um átomo? Ciência viva. Recuperado de: LiveScience.com
- Química Librettexts. (5 de junho de 2019). Calcular massas atômicas. Recuperado de: química.Librettexts.orks
- Edward Wichers e H. Steffen Peiser. (15 de dezembro de 2017). Peso atômico. Encyclopædia britannica. Recuperado de: Britannica.com
- « Características, efeitos e aplicações da terapia eletroconvulsiva
- História da embriologia, campo de estudo e filiais »

