Propriedades de hidrocarbonetos aromáticos, exemplos, aplicações
- 3088
- 206
- Terrell Stokes
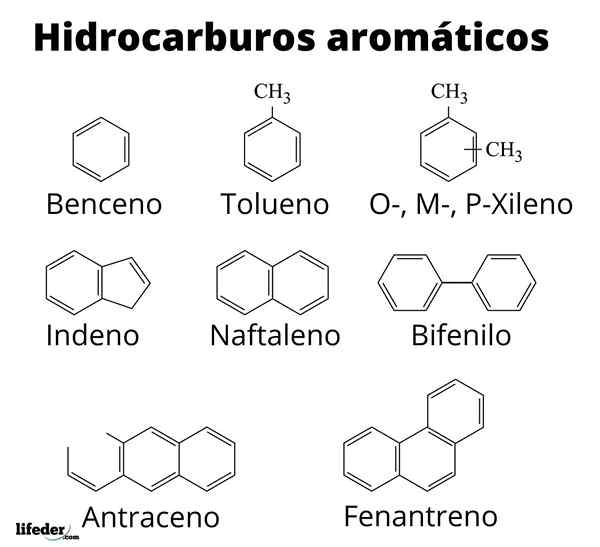
O hidrocarbonetos aromáticos ou de areia Eles são um conjunto de compostos orgânicos compostos apenas de carbonos e hidrogênios, e que são caracterizados por ter unidades de anéis de benzeno em suas estruturas moleculares.
Alguns, como seu nome enfatiza, disparam odores doces e agradáveis; razão pela qual os primeiros produtos químicos orgânicos se referiam a eles como aromáticos. O gás metano, por exemplo, é um hidrocarboneto de banheiro; Enquanto tolueno, líquido volátil, apresenta um cheiro bastante peculiar e forte.
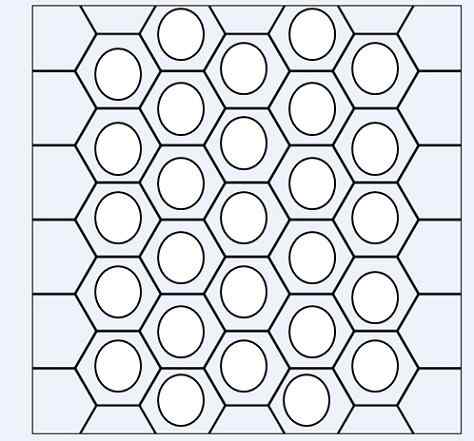 Os hidrocarbonetos aromáticos são reconhecidos por unidades de anéis benncênicos
Os hidrocarbonetos aromáticos são reconhecidos por unidades de anéis benncênicos Na imagem superior, temos um tipo de rede ou malha composta por anéis benzenos. Observe suas geometrias hexagonais e o círculo dentro. Este círculo representa o que é conhecido como aromaticidade, que é uma propriedade totalmente química e não -física, independente dos odores desses hidrocarbonetos.
Os hidrocarbonetos aromáticos estão entre os mais importantes, extraídos ou produzidos, minerais de petróleo e carbono. O benzeno é a pedra angular desses hidrocarbonetos e suas aplicações, pois deriva sinfinas de compostos que são usados como matéria -prima para a produção de fertilizantes, plásticos, adesivos, detergentes, perfumes, medicamentos, etc.
[TOC]
Como os hidrocarbonetos aromáticos são nomeados?
Um único anel de benzeno
Para hidrocarbonetos aromáticos, temos a peculiaridade de que seus nomes tradicionais ou comuns geralmente prevalecem sobre os governados pela nomenclatura da IUPAC.
Todos contêm o anel benzeno, ou um anel que encontra a propriedade de aromaticidade. O mais simples pode ser nomeado de acordo com o benzeno e as posições relativas de seus substituintes.
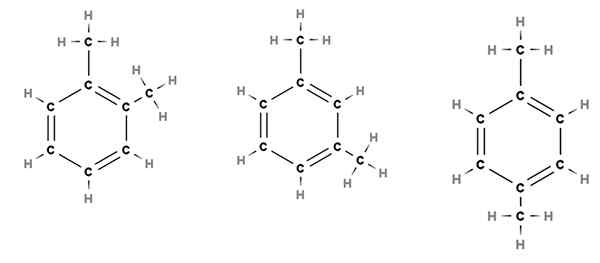 Posições relativas dos substituintes em um anel benzênico para a molécula de dimetilbenzeno. Fonte: Gabriel Bolívar via Molview.
Posições relativas dos substituintes em um anel benzênico para a molécula de dimetilbenzeno. Fonte: Gabriel Bolívar via Molview. Por exemplo, considere a imagem superior. Nas três estruturas, vemos o anel hexagonal do benzeno, que tem dois substituintes metilo, Cho3. Assim, este composto é chamado de dimetilbenzeno, porque consiste em um benzeno com dois metilos.
Pode servir a você: sulfato de potássio (K2SO4): estrutura, propriedades, usos, sínteseDa esquerda para a direita, vemos que a separação entre os dois3 Torna -se maior, o que não afeta apenas as propriedades físicas da molécula, mas também modifica seus respectivos nomes. Para diferenciá-los, uma vez que todos são chamados dimetilbenzeno, os prefixos de Ortho (O-), o objetivo (M-) e para (P-) são usados (P-).
Portanto, e novamente, da esquerda para a direita, temos: Ortho-dimetilbenzeno, Meta-Dimetilbenzeno e Parameterbenzeno. No entanto, o nome tradicional para este composto é o xileno, então os nomes se tornam: orto-xileno, meta-xileno e para-xileno.
Se houver mais de dois substituintes diferentes, é usado para enumerar carbonos seguindo as mesmas regras de nomenclatura que para todos os hidrocarbonetos.
Vários anéis
Para hidrocarbonetos aromáticos com mais de um anel benzênico, os nomes tradicionais se tornam ainda mais importantes. Isso ocorre porque os nomes sistemáticos que descrevem suas estruturas são pesados e difíceis de memorizar. Considere o exemplo de naftaleno:
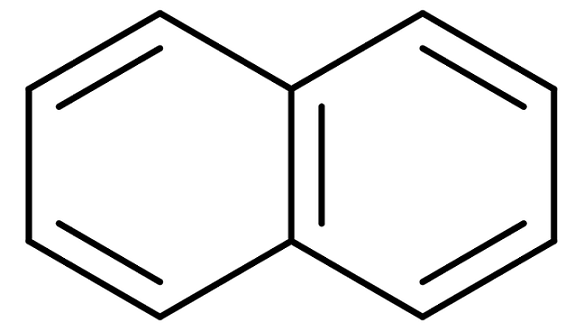 Estrutura de naftaleno
Estrutura de naftaleno O naftaleno também é conhecido comercialmente como naftalina ou cânfora branca. No entanto, seu nome sistemático é: biciclo [4,4,0] dezembro-1,3,5,7,9 pentano. E isso apenas para um composto com dois anéis benzênicos mesclados; A nomenclatura se torna muito mais complicada para compostos com três ou mais anéis.
Propriedades de hidrocarbonetos aromáticos
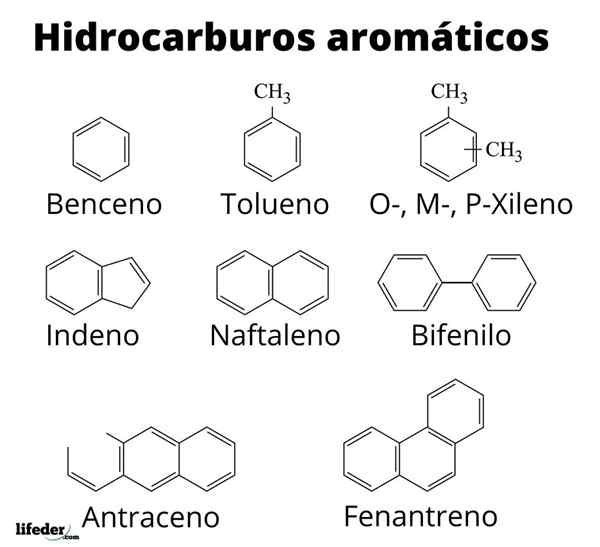 Estrutura de alguns hidrocarbonetos aromáticos
Estrutura de alguns hidrocarbonetos aromáticos Aromaticidade
Os hidrocarbonetos aromáticos contêm anéis que obedecem às regras de Huckel. Isto é, seus anéis devem ter átomos com hibridizações de SP2, Seja o mais plano possível e tenha vários elétrons π elocados iguais a 4n + 2. Por exemplo, o benzeno é aromático porque possui 6 elétrons democados para n= 1 (4 · 1 + 2 = 6).
Altas relações C/H
As relações C/H para hidrocarbonetos aromáticos são altos ou maiores que 1. Por exemplo, para benzeno, c6H6, Seu C/H é igual a 6/6 ou 1. Enquanto isso, para naftaleno, c10H8, Seu C/H é igual a 10/8 ou 1.25. O que significa isto? Que esses hidrocarbonetos são muito "carbonatados" em comparação com outros compostos.
Pode atendê -lo: ácido sulfônico: estrutura, nomenclatura, propriedades, usosChamas amarelas
Precisamente por causa de suas altas relações C/H, quando hidrocarbonetos aromáticos são queimados de chamas amarelas de fogo, o produto das partículas de carvão formadas (fuligem).
Reações de reposição
Hidrocarbonetos aromáticos podem substituir seus átomos de hidrogênio por qualquer outro substituinte. Isso é alcançado através de dois tipos de reações orgânicas: substituição eletrofílica aromática (SEAR) ou substituição nucleofílica aromática (SNAR).
Fragrâncias
Hidrocarbonetos aromáticos, como sugere o nome, são caracterizados por ter cheiros doces ou fortes. Essa propriedade lhes permitiu diferenciá -los, em princípio, de hidrocarbonetos gasosos e algumas parafinas de besouro.
Exemplos de hidrocarbonetos aromáticos
Hidrocarbonetos aromáticos, estritamente falando, preocupam apenas aqueles que são compostos de carbono e hidrogênio. Não deve haver heteroátomos (ou, p, n, s, etc.). Portanto, os seguintes exemplos que serão mencionados deixam de fora para compostos como piridina, furano ou fenol.
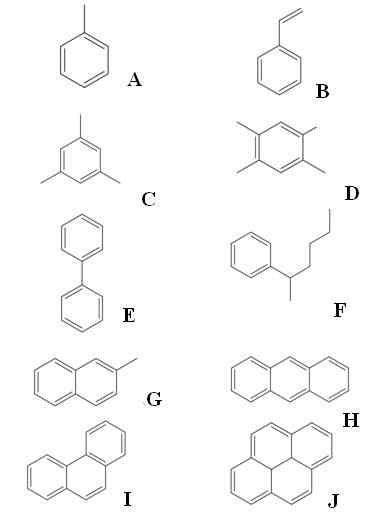 Exemplos de hidrocarbonetos aromáticos. Fonte: Gabriel Bolívar via Molview.
Exemplos de hidrocarbonetos aromáticos. Fonte: Gabriel Bolívar via Molview. Up, temos dez exemplos de hidrocarbonetos aromáticos. Observe que todo mundo tem pelo menos um anel benzênico. Seus nomes são:
A: tolueno
B: Alongamento
C: Mesitileno
D: tarde
E: Bifenil
F: 2-fenilhexan
G: 2-metilnaftaleno
H: Antraceno
I: Fenantreno
J: Pireno
De todos eles, Tolueno é o maior valor industrial.
Aplicações/usos
A maioria das aplicações de hidrocarbonetos aromáticos consiste em servir como matéria -prima para síntese, ou produção, produtos com alto valor comercial. Quase todos eles começam do benzeno, que é submetido a várias reações orgânicas para obter derivados funcionais.
Fibras e plásticos
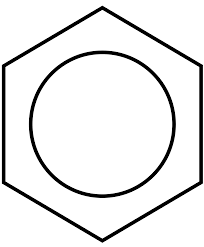 Benzeno
Benzeno Do benzeno, há ciclo -hexano, que é posteriormente transformado em outros compostos para sintetizar o nylon 6 ou o nylon 66. Por outro lado, o trecho também pode ser obtido do benzeno, que consiste no monômero de poliestireno. Assim, temos polímeros necessários para a produção de fibras e plásticos.
Pode atendê -lo: energia de ativaçãoResinas epóxi
Do benzeno, também, o bisfenol A pode ser sintetizado, com o qual, seguindo várias rotas de síntese, resinas epóxi, cola, adesivos e até pinturas ocorrem.
Detergentes
Alcybentes com cadeias laterais longas servem para a produção de detergentes; Entre eles, Alkybenzeosulfonates.
Tnt
Do tolueno, você pode produzir TNT: Trinitrotolueno, um dos explosivos mais conhecidos.
Ácido benzóico
Do tolueno, o ácido benzóico é obtido como derivado, composto essencial para as formulações de muitos perfumes, medicamentos e alimentos.
Solventes
Benzeno, tolueno e xileno (BTX), são os solventes orgânicos mais usados na pesquisa de petróleo.
Gasolina
Os hidrocarbonetos aromáticos também fazem parte da composição da gasolina, com o papel principal de aumentar seu Índice de octanas ou octanas.
Referências
- Graham Solomons t.C., Craig b. Fryhle. (2011). Química orgânica. (10º Edição.). Wiley Plus.
- Carey f. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Morrison e Boyd. (1987). Quimica Organica. (Quinta edição). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Composto aromático. Recuperado de: em.Wikipedia.org
- Ed Vitz et al. (8 de setembro de 2020). Hidrocarbonetos aromáticos. Química Librettexts. Recuperado de: química.Librettexts.org
- Wyman Elizabeth. (2020). Hidrocarbonetos aromáticos: definição, exemplo e uso. Estudar. Recuperado de: estudo.com
- Boluda, c. J., Macías, m., & González Marrero, J. (2019). A complexidade química da gasolina automotiva. Ciência, Engenharia e Aplicações,2(2), 51-79. Doi: doi.org/10.22206/cyap.2019.V2i2.Pp51-79
- « Conservação do Princípio, Exemplos, Exemplos, Exercícios Lineares.
- Orações com exemplos e regras de uso »

