Háfnio

- 2738
- 431
- Mr. Reginald Lindgren
 Amostra metálica de hafnio. Fonte: imagens de alta resolução de elementos químicos [CC por (https: // criativeCommons.Org/licenças/por/3.0)]
Amostra metálica de hafnio. Fonte: imagens de alta resolução de elementos químicos [CC por (https: // criativeCommons.Org/licenças/por/3.0)] O que é hafnio?
Ele háfnio É um metal de transição cujo produto químico é HF e tem um número atômico de 72. É o terceiro elemento do Grupo 4 da tabela periódica, sendo congene no titânio e no circum. Com o último, ele compartilha muitas propriedades químicas, sendo localizadas juntas em minerais da crosta da Terra.
Procurando o hafnio está olhando onde o zircônio, porque é um subproduto de sua extração. O nome deste metal vem da palavra latina 'Hafnia', cujo significado é o nome de Copenhague, uma cidade onde foi descoberta em minerais de zircão e a controvérsia terminou em relação à sua verdadeira natureza química.
Este metal assume a distinção de ser o último dos elementos mais estáveis descobertos aqui da Terra; Ou seja, as outras descobertas constituíram uma série de ultrapesados, isótopos radioativos e/ou artificiais.
Os compostos de hafnio são análogos ao titânio e circulium, predominantemente o número de oxidação +4, como o HFCL4, HFO2, Hfi4 e hfbr4. Alguns deles lideram a lista dos materiais mais refratários já criados, bem como ligas de grande resistência térmica e também atuam como excelentes absorventes de nêutrons.
Por esse motivo, o hafnio tem muita participação na química nuclear, especialmente para os reatores de água da pressão.
Descoberta
Transição metal ou terras raras
A descoberta do Hafnio foi cercada por controvérsias, embora sua existência já tenha sido prevista desde 1869 graças à tabela periódica de Mendeleev.
O problema era que ele estava posicionado sob o zircônio, mas coincidiu no mesmo período dos elementos das terras raras: Lantanoides. Químicos na época não sabiam se era um metal de transição ou um metal de terras raras.
 99,9% da barra de hafnium. Fonte-alquimista-HP (www.PSE-Mendelejew.de), CC BY-SA 2.0, via Wikimedia Commons
99,9% da barra de hafnium. Fonte-alquimista-HP (www.PSE-Mendelejew.de), CC BY-SA 2.0, via Wikimedia Commons O químico francês Georges Urbain, descoberto de Luthacio, vizinho metal do Hafnio, disse em 1911 que descobriu o Element 72, que Celtio chamou e proclamou que era um metal das terras raras. Mas três anos depois, concluiu -se que seus resultados estavam errados e que apenas isolou uma mistura de lantanoides.
Não foi até que os elementos fossem ordenados por seus números atômicos, graças ao trabalho de Henry Moseley em 1914, que o bairro entre Luthate e elemento 72 era evidência do mesmo grupo que os metais de titânio e circuito.
Pode servir a você: floculação: reação, tipos, aplicações, exemplosDetecção em Copenhague
Em 1921, após os estudos da estrutura atômica de Niels Bohr e sua previsão do espectro de emissão de raios X para o elemento 72, esse metal foi interrompido nos minerais das terras raras; E, em vez disso, sua busca nos minerais de Circonium focou, já que os dois elementos tiveram que compartilhar várias propriedades químicas.
O químico dinamarquês Dirk Coster e o químico húngaro Georg von Hevesy em 1923 finalmente reconheceram o espectro previsto por Niels Bohr em amostras de zircão da Noruega e da Groenlândia. Tendo feito a descoberta em Copenhague, eles chamaram o elemento 72 pelo nome latino desta cidade: Hafnia, que mais tarde derivou 'Hafnio'.
Isolamento e produção
No entanto, não foi uma tarefa fácil. Embora em 1924 um método tenha sido desenvolvido pela recristalização fracionária para obter tetracloreto de hafnio, HFCL4, Era os produtos químicos holandeses Anton Eduard van Arkel e Jan Hendrik de Boer, que o reduziram ao Hafnium metálico.
Para fazer isso, o HFCL4 Foi submetido a uma redução usando magnésio metálico (processo Kroll):
Hfcl4 + 2 mg (1100 ° C) → 2 mgcl2 + HF
Por outro lado, a partir de Hafnio tetrayoduro, HFI4, Isso foi vaporizado para sofrer uma decomposição térmica em um filamento incandescente de tungstênio, no qual o hafnio metálico foi depositado para causar uma barra de aparência policristalina (processo de barra cristalina ou processo de arkel-boer):
Hfi4 (1700 ° C) → HF + 2 I2
Estrutura de hafnio
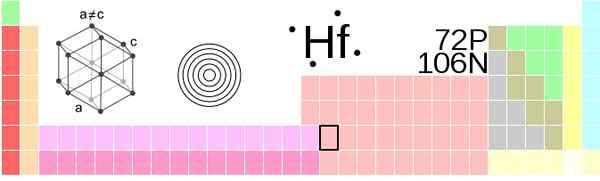 Hafnio Localização na tabela periódica. Fonte: !Original: ahoteseiervector: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons
Hafnio Localização na tabela periódica. Fonte: !Original: ahoteseiervector: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons Hafnio, átomos de HF, são agrupados em pressão ambiente em um cristal de estrutura hexagonal compacta, HCP, assim como o titânio e os metais de zircônio fazem. Este cristal de Hcnio HCP se torna sua fase α, que permanece constante até uma temperatura de 2030 K, quando sofre uma transição para a fase β, com uma estrutura cúbica centrada no corpo, BCC.
Isso é entendido se o calor "relaxa", o vidro é considerado e, portanto, os átomos de HF buscam se posicionar de tal maneira que sua compactação diminua. Essas duas fases são suficientes para considerar o polimorfismo do hafnium.
Também apresenta um polimorfismo que depende de altas pressões. As fases α e β existem a uma pressão de 1 atm; Enquanto a fase ω, hexagonal, mas ainda mais compactada que o HCP comum, aparece quando as pressões excedem 40 GPa. Curiosamente, quando as pressões continuam aumentando, a fase β reaparece, a menos densa.
Pode atendê -lo: ácido seleenenhdric (h2se): o que é, estrutura, propriedades, usaHAFNIO Propriedades
Aparência física
Sólido branco prateado, que mostra tons escuros se tiver uma camada de óxido e nitreto.
Massa molar
178,49 g/mol
Ponto de fusão
2233 ºC
Ponto de ebulição
4603 ºC
Densidade
À temperatura ambiente: 13,31 g/cm3, sendo duas vezes mais denso que o circum
Bem no ponto de fusão: 12 g/cm3
Calor de fusão
27,2 kJ/mol
Calor de vaporização
648 kJ/mol
Eletro-negatividade
1.3 na escala Pauling
Energias de ionização
Primeiro: 658,5 kJ/mol (HF+ gasoso)
Segundo: 1440 KJ/mol (HF2+ gasoso)
Terceiro: 2250 kJ/mol (HF3+ gasoso)
Condutividade térmica
23,0 W/(M · K)
Resistividade elétrica
331 nω · m
Dureza mohs
5.5
Reatividade
A menos que o metal seja pula e queima, disparando faíscas a uma temperatura de 2000 ºC, ele não tem suscetibilidade a oxidar ou correr, uma vez que uma fina camada de seu óxido o protege. Nesse sentido, é um dos metais mais estáveis. De fato, ácidos ou bases fortes podem dissolvê -lo; Com exceção do ácido fluorhorrórico, e halogênios capazes de oxidá -lo.
Configuração eletronica
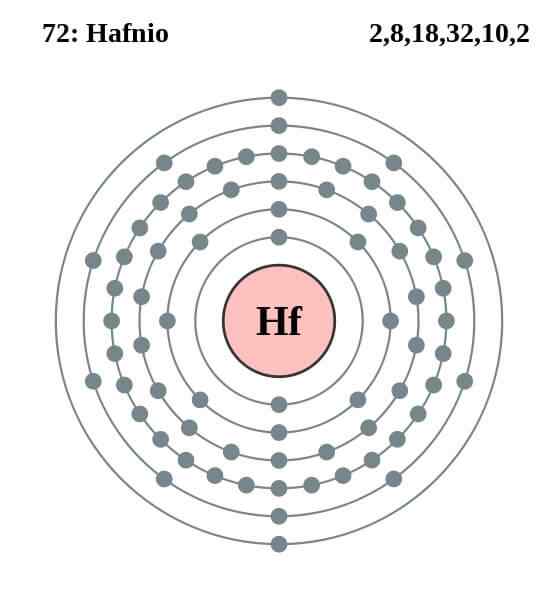 Hafnio Configuração eletrônica
Hafnio Configuração eletrônica O Atom de Hafnio tem a seguinte configuração eletrônica:
[Xe] 4f14 5 d2 6s2
Isso coincide com o fato de pertencer ao Grupo 4 da Tabela Periódica, juntamente com o titânio e o Circonium, porque possui quatro elétrons de Valência nos orbitais 5D e 6s. Observe que o hafnio não poderia ser um Lantanoide, pois possui seus orbitais 4F completamente cheios.
Números de oxidação
A mesma configuração eletrônica revela quantos elétrons são capazes de perder um átomo de hafnio ao fazer parte de um composto. Supondo que ele perde seus quatro elétrons de Valência, ele seria um cátion tetravalente HF4+ (Em analogia para você4+ e zr4+) E, portanto, teria um número de oxidação de +4.
Este é de fato o mais estável e comum de seus números de oxidação. Outros menos relevantes são: -2 (HF2-), +1 (HF+), +2 (HF2+) e +3 (HF3+).
Isótopos
Hafnio é apresentado na Terra como cinco isótopos estáveis e um radioativo com um tempo muito grande da vida:
-174HF (0,16%, com meia -vida de 2,10quinze anos, então é considerado praticamente estável)
-176HF (5,26%)
-177HF (18,60%)
Pode atendê -lo: bases fracas-178HF (27,28%)
-179HF (13,62%)
-180HF (35,08%)
Observe que não existe esse isótopo como tal que se destaca em abundância, e isso se reflete na massa atômica média do Hafnio, 178.49 Uma.
De todos os isótopos radioativos do Hafnio, que juntamente com os nativos totalizam um total de 34, o 178m2A HF é a mais controversa porque, em sua decadência radioativa libera a radiação gama, para que esses átomos possam ser usados como uma arma de guerra.
Usa/aplicações
 Hafnio coberto com uma fina camada de óxido. Fonte: Alchemist-HP (Talk) (www.PSE-Mendelejew.De), Fal, via Wikimedia Commons
Hafnio coberto com uma fina camada de óxido. Fonte: Alchemist-HP (Talk) (www.PSE-Mendelejew.De), Fal, via Wikimedia Commons Reações nucleares
Hafnio é um metal resistente à umidade e altas temperaturas, além de ser um excelente absorvente de nêutrons. Por esse motivo, é usado em reatores de água de pressão, bem como na fabricação de barras de controle para reatores nucleares, em cujos revestimentos eles são feitos de Ultrapuro Circu.
Ligas
Os átomos de hafnio podem integrar outros cristais de metal para dar origem a diferentes ligas. Estes são caracterizados por serem tenazes e resistentes termicamente, por isso são destinados a aplicações espaciais, como na construção de bicos de motor para foguetes.
Por outro lado, algumas ligas e compostos sólidos de Hafnio têm propriedades especiais; como seus carbonetos e nituros, HFC e HFN, respectivamente, que são materiais muito refratários. Tantalo e Hafnio Carbide, TA4HFC5, Com um ponto de fusão de 4215 ºC, é um dos materiais mais refratários já conhecidos.
Catálise
Os metalocenos de Hafnio são usados como catalisadores orgânicos para síntese de polimeleno, como polietileno e poliestireno.
Riscos
Não se sabe até o momento que impacto os íons HF poderiam ter em nosso corpo4+. Por outro lado, porque eles são encontrados na natureza nos minerais de zircônio, não se acredita que eles alterem o ecossistema de libertar seus sais para o meio ambiente.
Agora, é recomendável manipular os compostos de Hafnio com cuidado, como se fossem tóxicos, mesmo que não houvesse estudos médicos que provem que eles são prejudiciais à saúde.
O verdadeiro perigo do hafnio está nas partículas de seu sólido finamente moído, que pode queimar exatamente quando eles entram em contato com o oxigênio do ar.
Isso explica por que, quando é polido, ação que raspa sua superfície e emite partículas de metal puro, as faíscas queimadas são liberadas com uma temperatura de 2000 ºC; Ou seja, o Hafnio apresenta piroporicidade, a única propriedade que implica fogo ou riscos graves de queimaduras.

