Propriedades, comportamento, formulário, exemplos de gases

- 3029
- 948
- Lonnie MacGyver
O Gases São todas as substâncias ou compostos cujos estados de agregação são fracos e dispersos, enquanto dependendo muito das condições de pressão e temperatura que os governam. Talvez constitua a segunda forma de matéria mais abundante em todo o universo após o plasma.
Na terra, os gases compõem as camadas da atmosfera, da exosfera, à troposfera e ao ar que respiramos. Embora um gás seja invisível quando é divulgado por grandes espaços, como o céu, é detectado pelo movimento das nuvens, pelas curvas das lâminas de um moinho ou pelos vapores expirados de nossas bocas em climas frios.
 Os gases podem ser observados em chaminés industriais ou domésticas, bem como em torres de fumaça que emanam por vulcões. Fonte: pxhere.
Os gases podem ser observados em chaminés industriais ou domésticas, bem como em torres de fumaça que emanam por vulcões. Fonte: pxhere. Da mesma forma, indo para os aspectos negativos ambientais, é observado na fumaça negra do tubo de escape dos veículos, nas colunas de fumaça das torres localizadas nas fábricas, ou na fumaça levantada quando uma floresta queima.
Também está enfrentando fenômenos gasosos quando são vistos vapores que deixam os esgotos, nos fatídicos incêndios do pântano e dos cemitérios, no oxigênio bubb liberado pelo produto das plantas de sua fotossíntese, e mesmo nos erutos e flatulência.
Onde quer que os gases sejam observados, isso significa que houve uma reação química, a menos que sejam fixos ou assimilados diretamente do ar, a principal fonte de gases (superficialmente) do planeta. À medida que as temperaturas aumentam, toda substância (elementos químicos) será transformada em gases, incluindo metais como ferro, ouro e prata.
Independentemente da natureza química dos gases, todos compartilham em comum a grande distância que separa suas partículas (átomos, moléculas, íons etc.), que se movem caóticos e arbitrariamente por um volume ou espaço específico.
[TOC]
Propriedades de gás
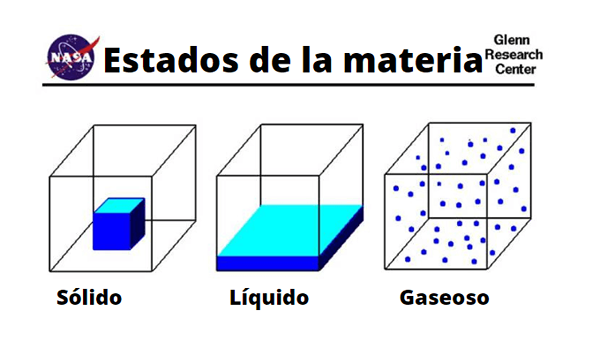 Diferenças em moléculas sólidas, líquidas e de gás
Diferenças em moléculas sólidas, líquidas e de gás Físico
As propriedades físicas dos gases variam dependendo de que substância ou composto é. Popularmente, os gases estão associados a maus odores ou podridão, devido ao seu teor de enxofre ou à presença de aminas voláteis. Da mesma forma, eles são visualizados por cores verdes, marrons ou amareladas, que intimidam e dão um mau presságio.
No entanto, a maioria dos gases, ou pelo menos os mais abundantes, são realmente incolores e inodorosos. Mesmo que não sejam atribuídos, podem ser sentidos na pele e se opõem à resistência do movimento, até criando camadas viscosas nos corpos que os atravessam (como nos aviões).
Todos os gases podem sofrer mudanças de pressão ou temperatura que acabam criando seus respectivos líquidos; isto é, eles sofrem condensação (se forem resfriados) ou liquefação (se forem "pressionados").
 Condensação; de estado gasoso para estado líquido
Condensação; de estado gasoso para estado líquido Por outro lado, os gases são capazes de se dissolver em líquidos e alguns sólidos porosos (como carbono ativado). Bolhas são o resultado de aglomerados de gás que ainda não se dissolveram no meio e escapam para a superfície líquida.
Condutividade elétrica e térmica
Sob condições normais (sem ionização de suas partículas), os gases são motivadores ruins de calor e eletricidade. No entanto, quando estão tensos com muitos elétrons, permitem a passagem da corrente através deles, como visto nos raios durante as tempestades.
Por outro lado, com baixas pressões e submetidas a um campo elétrico, alguns gases, especialmente os nobres ou perfeitos, iluminados e suas luzes são usadas para o design da vida noturna e pôsteres (luz neon), bem como no famoso choque elétrico Lâmpadas nas lanternas de rua.
Pode atendê -lo: equilíbrio de granataria: características, peças e como usá -loEm relação à condutividade térmica, muitos gases se comportam como isoladores térmicos, de modo que sua incorporação no preenchimento de fibras, tecidos ou painéis de vidro ajude a impedir que o calor os fabrica e mantenha a temperatura constante.
No entanto, existem gases que são bons condutores de calor e podem causar queimaduras piores causadas por líquidos ou sólidos; Por exemplo, como no vapor quente de bolos assados (ou empanadas), ou com jatos a vapor que escapam das caldeiras.
Reatividade
Geralmente as reações envolvendo gases, ou onde ocorrem, são descritas como perigosas e pesadas.
Sua reatividade depende, novamente, de sua natureza química; No entanto, ao expandir e mobilizar bastante, mais cuidado e controle devem ser tomados, porque eles podem desencadear aumentos drásticos de pressão que colocam em risco a estrutura do reator; Sem mencionar o quão inflamável ou não são gases felizes.
Comportamento Gase
Macroscopicamente, pode -se dar uma idéia do comportamento dos gases testemunhando como fumaça, anéis ou "idiomas" literários de cigarros evoluem no ar. Além disso, quando uma granada de fumaça explode, é interessante detalhar o movimento dessas nuvens de cores diferentes.

No entanto, essas observações estão sujeitas à ação aérea e também ao fato de que existem partículas sólidas muito finas suspensas em fumaça. Portanto, esses exemplos não são suficientes para chegar a uma conclusão sobre o verdadeiro comportamento de um gás. Em vez disso, experimentos foram realizados e desenvolveram a teoria cinética dos gases.
Molecular e, idealmente, partículas gasosas colidem elasticamente entre si, tendo deslocamentos lineares, rotacionais e vibracionais. Eles têm uma energia associada média, o que permite viajar livremente por qualquer espaço sem quase interagir ou colidir com outra partícula à medida que o volume aumenta ao seu redor.
Seu comportamento seria uma mistura do movimento errático browniano e o de colisões de bolas de bilhar que saltam incessantemente entre si e as paredes da mesa; Se não houver paredes, elas se espalharão em direção ao infinito, a menos que as mantenham: gravidade.
Forma de gase
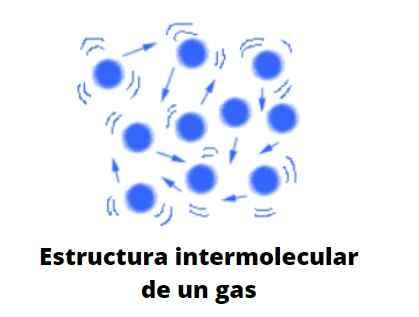
Os gases, ao contrário de líquidos e sólidos, não estão sujeitos ao tipo condensado; isto é, a agregação ou coesão de suas partículas nunca consegue definir uma forma. Eles compartilham com líquidos o fato de ocuparem completamente o volume do recipiente que os contém; No entanto, eles não têm tensão superficial e superficial.
Se a concentração de gás for alta, seus "idiomas" ou formulários macroscópicos já descritos podem ser visualizados a olho nu. Estes, mais cedo ou mais tarde, acabarão desaparecendo devido à ação do vento ou pela mera expansão do gás. Os gases, portanto, cobrem todos os cantos do espaço limitado, causando sistemas altamente homogêneos.
Agora, a teoria considera convenientemente gases como esferas que mal colidem consigo mesmas; Mas quando o fazem, eles saltam elasticamente.
Essas esferas são muito separadas uma da outra, então os gases são praticamente "cheios" de vácuo; A partir daí, você deve sua versatilidade para atravessar a menor fenda ou fissura, e a facilidade de poder comprimi -las significativamente.
Pode atendê -lo: óxidos não -metálicosÉ por isso que, no entanto, fechou a instalação de uma padaria, se caminhar ao lado, é certo que o aroma do pão recém -assado será apreciado.
Pressão do gás
Pode -se acreditar que, sendo tão disperso e separado as esferas ou partículas de gás, elas são incapazes de gerar qualquer pressão sobre corpos ou objetos. No entanto, a atmosfera demonstra que essa crença é falsa: tem uma massa, pesa e impede que líquidos evaporam ou fervendo de nada. Os pontos de ebulição são medidos à pressão atmosférica.
As pressões gastronômicas se tornam mais quantificáveis se os manômetros estiverem disponíveis ou se estiverem trancados de recipientes de parede não -deformáveis. Assim, quanto mais partículas de gás estiverem dentro do recipiente, maior o número de colisões entre elas e as paredes do mesmo.
Essas partículas ao colidir com as paredes as pressionam, pois exercem em sua superfície uma força proporcional à sua energia cinética. É como se as bolas ideais de bilhar para uma parede estivessem sobrecarregadas; Se houver muitos que os afetam em alta velocidade, pode conseguir quebrar.
Unidades
Existem muitas unidades que acompanham as medidas de pressão de um gás. Alguns dos mais conhecidos são os milímetros de Mercúrio (MMHG), bem como o Torr. São os do sistema internacional de unidades (SI) que definem o Pascal (PA) em termos de N/M2; E dele, o quilo (kpa), mega (mpa) e giga (gpa) Pascal.
Volume de gás
Um gás ocupa e se expande durante todo o volume do recipiente. Quanto maior o recipiente, o volume de gás também será; Mas tanto a pressão quanto a densidade diminuirão pela mesma quantidade de partículas.
O próprio gás, por outro lado, possui um volume associado que não depende tanto de sua natureza ou estrutura molecular (idealmente), mas das condições de pressão e temperatura que o governam; Este é, seu volume molar.
Na realidade, o volume molar varia de um gás para outro, embora as variações sejam pequenas se não forem de moléculas heterogêneas e grandes. Por exemplo, o volume molar de amônia (NH3, 22.079 l/mol) a 0 ºC e 1 atm, difere do hélio (He, 22.435 l/mol).
Todos os gases têm um volume molar que muda dependendo de P e T, e independentemente do tamanho de suas partículas, o número delas é sempre o mesmo. A partir daqui, ele derivou o que é conhecido pelo número Avogadro (nPARA).
Principais leis de gases
O comportamento da Gase tem estudado desde os séculos passados por meio de experimentos, observações profundas e interpretação dos resultados.
Tais experimentos permitiram uma série de leis que, reunidas na mesma equação (a dos gases ideais), ajudam a prever as respostas de um gás a diferentes condições de pressão e temperatura. Dessa maneira, há uma relação entre seu volume, temperatura e pressão, bem como o número de suas toupeiras em um determinado sistema.
Entre essas leis estão as quatro seguintes: Boyle, Charles, Gay-Lussac e Avogadro.
Lei de Boyle
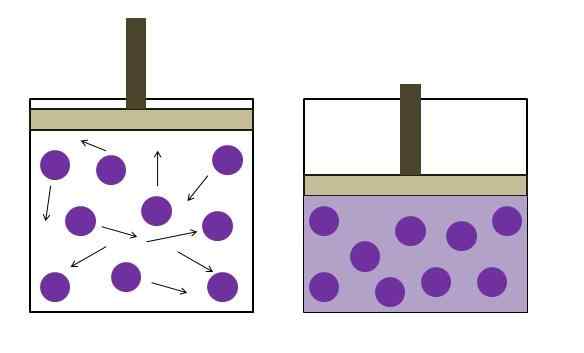 Aumento da pressão de redução de pressão. Fonte: Gabriel Bolívar
Aumento da pressão de redução de pressão. Fonte: Gabriel Bolívar A lei de Boyle estabelece que, a temperatura constante, o volume de um gás ideal é inversamente proporcional à sua pressão; Isto é, quanto maior o contêiner, menor a pressão que suas paredes experimentarão pela mesma quantidade de gás experimentará.
Pode servir a você: Charles Law: Fórmulas e Unidades, Experimento, ExercíciosCharles Law
 Lanternas ou desejos chineses. Fonte: pxhere.
Lanternas ou desejos chineses. Fonte: pxhere. A lei de Charles estabelece que a pressão constante, o volume de um gás ideal é diretamente proporcional à sua temperatura. Os balões demonstram Charles '.
Lei Gay-Lussac
A lei de Gay-Lussac estabelece que, em volume constante, a pressão de um gás ideal é diretamente proporcional à sua temperatura. Em um caldeirão bem fechado, se um gás esquentar progressivamente, cada vez que a pressão interna será maior, porque as paredes do caldeirão não são deformadas ou dilatadas; Isto é, seu volume não muda, é constante.
Lei Avogadro
Finalmente, a lei de Avogadro estabelece que o volume ocupado por um gás ideal é diretamente proporcional ao número de suas partículas. É assim, se você tem um mol de partículas (6,02,1023), então o volume molar de gás será.
Tipos de gases
Gases combustíveis
São gases cujos componentes funcionam como combustíveis, porque são usados para produção de energia térmica. Alguns deles são gás natural, petróleo liquefeito e gás hidrogênio.
Gases industriais
Estes são gases fabricados, que são comercializados ao público para diferentes usos e aplicações, como setores de saúde, alimentos, proteção ambiental, metalurgia, indústria química, segurança, entre outros. Alguns desses gases são oxigênio, nitrogênio, hélio, cloro, hidrogênio, monóxido de carbono, propano, metano, óxido nitroso, entre outros.
Gases inertes
São aqueles gases que, sob condições específicas de temperatura e pressão, não geram nenhuma reação química ou muito baixa. Eles são o neon, argônio, hélio, kripton e xenônio. Eles são usados em processos químicos nos quais os elementos não reativos são necessários.
Exemplos de elementos e compostos gasosos
Quais são os elementos gasosos da tabela periódica em condições terrestres?
Primeiro temos hidrogênio (H), que forma moléculas H2. É seguido por hélio (ele), o gás nobre mais claro; e então nitrogênio (n), oxigênio (o) e fluoreto (f). Estes últimos três também formam moléculas diatômicas: n2, QUALQUER2 e f2.
Depois que o fluoreto vem o neon (NE), o gás nobre que segue o hélio. Sob fluorino, temos cloro (CL), na forma de moléculas de Cl2.
Então temos o resto dos gases nobres: Argônio (AR), Kripton (KR), Xenón (Xe), Radon (RN) e Oganeson (OG).
Portanto, eles são um total de doze elementos gasosos; onze se excluirmos o altamente radioativo e instável oganeson.
Compostos gasosos
Além dos elementos gasosos, alguns compostos gasosos comuns serão listados:
-H2S, sulfeto de hidrogênio, responsável pelo cheiro de ovos podres
-NH3, amônia, aquele aroma penetrante que é percebido em sabonetes usados
-Co2, Dióxido de carbono, um gás de efeito estufa
-NÃO2, dióxido de nitrogênio
-Não, monóxido de nitrogênio, um gás que se acreditava extremamente tóxico, mas desempenha um papel importante no sistema circulatório
-SW3, Trióxido de enxofre
-C4H10, butano
-HCL, cloreto de hidrogênio
-QUALQUER3, ozônio
-Sf6, Hexafluoruro do enxofre
Referências
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- As propriedades dos gases. Recuperado de: Chemed.Chem.Purdue.Edu
- Wikipedia. (2019). Gás. Recuperado de: em.Wikipedia.org
- Helmestine, Anne Marie, Ph.D. (5 de dezembro de 2018). Gases - Propriedades gerais de gases. Recuperado de: pensamento.com
- Relógio de saúde masculina de Harvard. (2019). O estado de gás. Recuperado de: saúde.Harvard.Edu
- Editores de resfriamento eletrônicos. (1 de setembro de 1998). A condutividade térmica dos gases. Recuperado de: resfriamento eletrônico.com
- « História Demonologia, que estudo e demonologistas famosos
- Características gráficas, elementos, exemplos »

