Características, treinamento, exemplos
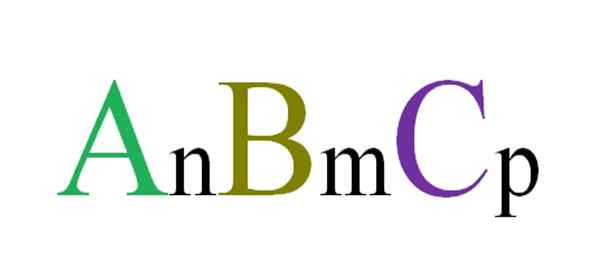
- 1158
- 81
- Orlando MacGyver
O Compostos ternários Eles são todos aqueles que são compostos por três átomos ou íons diferentes. Eles podem ser muito diversos, de substâncias ácidas ou básicas, a ligas de metal, minerais ou materiais modernos. Os três átomos podem pertencer ao mesmo grupo da tabela periódica ou prosseguir com locais arbitrários.
No entanto, para que o composto ternário ocorra, deve haver uma afinidade química entre seus átomos. Nem todos são compatíveis entre si e, portanto, você não pode simplesmente escolher aleatoriamente quais três integrarão e definirão o composto ou a mistura (assumindo a falta de ligações covalentes).
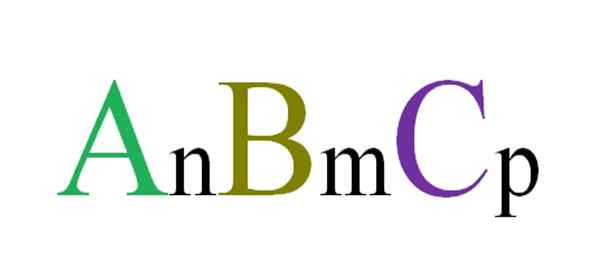 Fórmula geral e aleatória para compostos ternários. Fonte: Gabriel Bolívar.
Fórmula geral e aleatória para compostos ternários. Fonte: Gabriel Bolívar. Por exemplo, três letras são escolhidas aleatoriamente que governarão um composto ternário ABC (imagem superior). Os subscritos N, M e P indicam relações estequiométricas entre átomos ou íons A, B e C. Variando os valores de tais subscritos e as identidades das letras, compostos ternários sem fim são obtidos.
No entanto, a fórmula AnBmCp Só será válido se atender à eletroneutralidade; isto é, a soma de suas cobranças deve ser igual a zero. Com isso em mente, existem limitações físicas (e químicas) que orientam se a formação do referido composto ternário é ou não possível.
[TOC]
Características de compostos ternários
Suas características não são gerais, mas variam dependendo da natureza química deles. Por exemplo, oxoácidos e bases são compostos ternários, e cada um deles compartilha ou não uma série de características representativas.
Agora, antes de um composto hipotético ABC, isso pode ser iônico, se as diferenças de eletronegatividade entre A, B e C não forem grandes; ou covalente, com links a-b-c. Estes últimos são dados em exemplos infinitos na química orgânica, como em álcoois, fenóis, éteres, carboidratos, etc., cujas fórmulas podem ser descritas com CnHm QUALQUERp.
Pode atendê -lo: propriedades mecânicas de metaisAssim, as características são muito variadas e oscilam no alto grau de um composto ternário para outro. O composto cnHmQUALQUERp Dizem que é oxigenado; enquanto cnHmNp, Por outro lado, é nitrogênio (é uma amina). Outros compostos podem ser enxofre, fosforados, fluorizados ou têm um caráter metálico acentuado.
Bases e ácidos
Avançando no campo da química inorgânica, você tem bases de metal, MnQUALQUERmHp. Dar.
Por exemplo, a base Naoh, considerando tais subscritos, deve ser escrita como NA1QUALQUER1H1 (que seria caótico). Além disso, seria assumido que H é como um cátion h+, E não como realmente parece: fazer parte do ânion oh-. Devido à ação de OH- Na pele, essas bases são sabonetes e cáusticos.
As bases de metal são substâncias iônicas e, embora consistam em dois íons, Mn+ e oh- (N / D+ e oh- Para o Naoh), eles são compostos ternários por ter três átomos diferentes.
Os ácidos, por outro lado, são covalentes e sua fórmula geral é Hao, onde um átomo não metálico é geralmente. No entanto, dada a facilidade de ionizado em hidrogênios de liberação de água, seus íons h+ Corroen e machucar a pele.
Nomenclatura
Como as características, a nomenclatura dos compostos ternários é muito variada. Por esse motivo, apenas apenas as bases, oxoácidos e oxiss serão considerados superficiais.
Bases
As bases de metal são mencionadas primeiro com a palavra 'hidróxido' seguida pelo nome do metal e sua valência em números romanos entre parênteses. Assim, NaOH é hidróxido de sódio (I); Mas como o sódio tem valência única de +1, permanece simplesmente como hidróxido de sódio.
Pode servir você: alceansO al (oh)3, Por exemplo, é hidróxido de alumínio (III); e Cu (OH)2, Hidróxido de cobre (II). Claro, tudo de acordo com a nomenclatura sistemática.
Oxoácidos
Oxóácidos tem uma fórmula bastante geral do tipo HAO; Mas, na realidade, eles são melhor descritos como aoh. O link de Ha-H emerge o H é liberado+.
A nomenclatura tradicional é a seguinte: a palavra 'ácido' começa, seguida pelo nome do átomo central, precedido ou precedido por seus respectivos prefixos (hypo, por) ou sufixos (urso, OIC) de acordo com se ele trabalha com seus menores ou valências mais antigas.
Por exemplo, oxoácidos de bromo são hbro, hbro2, Hbro3 e hbro4. Estes são ácidos: hipobromo, brômico, brômico e perbrômico, respectivamente. Observe que em todos eles existem três átomos com valores diferentes para seus subscritos.
Oxisals
Também chamados de sais nullion, eles são os mais representativos dos compostos ternários. A única diferença para mencioná -los é que o urso e os sufijos mudam para Ito e Ato, respectivamente. Além disso, H é substituído por um cátion metal, produto da neutralização ácido-base.
Continuando com bromo, seus oxisals de sódio seriam: Nabro, Nabro2, Nabro3 e Nabro4. Seus nomes se tornariam: Hipobromito, Bromito, Bromato e Perbromato de Sódio. Sem dúvida, o número de oxisals possíveis excede o dos oxoácidos.
Treinamento
Novamente, cada tipo de composto ternário tem sua própria origem ou processo de treinamento. No entanto, é justo mencionar que estes só podem ser formados se houver uma afinidade suficiente entre os três membros do átomo. Por exemplo, existem bases de metal graças às interações eletrostáticas entre cátions e OH-.
Pode atendê -lo: ácido cítricoAlgo semelhante acontece com os ácidos, o que não pôde ser formado se não houvesse uma ligação covalente a-o-h.
Com base na pergunta, como os principais compostos são formados? A resposta direta é a seguinte:
- As bases de metal são formadas por dissolução de óxidos de metal na água ou em uma solução alcalina (geralmente fornecida por NaOH ou amônia).
- Os oxoácidos são o produto da dissolução de óxidos não -metálicos na água; Entre eles, o CO2, Clo2, NÃO2, SW3, P4QUALQUER10, etc.
- E então, o oxisal surge quando os oxoacídeos são alcalados ou neutralizados com uma base de metal; A partir dele vêm os cátions de metal que supõem H+.
Outros compostos ternários são formados após um processo mais complicado, como em certas ligas ou minerais.
Exemplos
Finalmente, uma série de fórmulas para diferentes compostos ternários será mostrada como uma lista:
- Mg (oh)2
- Cr (oh)3
- Kmno4
- N / D3Bo3
- CD (OH)2
- Irmão mais velho3
- FEASO4
- Bacr2QUALQUER7
- H2SW4
- H2Teo4
- Hcn
- Agohh
Outros exemplos menos comuns (e até hipotéticos) são:
- COFECU
- Algasn
- Ucapb
- BEMGO2
Os subscritos N, M e P foram omitidos para não complicar as fórmulas; Embora na realidade, seus coeficientes estequiométricos (exceto o melhor para o bem2), pode até ter valores decimais.
Referências
- Shiver & Atkins. (2008). Química Inorgânica. (Quarta edição). Mc Graw Hill.
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- SRA. Hilfstein. (s.F.). Comunões ternários. Recuperado de: tenafly.K12.NJ.nós
- Wikipedia. (2019). Ternário comund. Recuperado de: em.Wikipedia.org
- Carmen Bello, Arantxa Isasi, Ana Puerto, Germán Tomás e Ruth Vicente. (s.F.). Compostos ternários. Recuperado de: iesdmjac.EducA.Aragão.é
- « Características de compostos quaternários, treinamento, exemplos
- Características de compostos especiais, treinamento, usos »

