Características de compostos quaternários, treinamento, exemplos
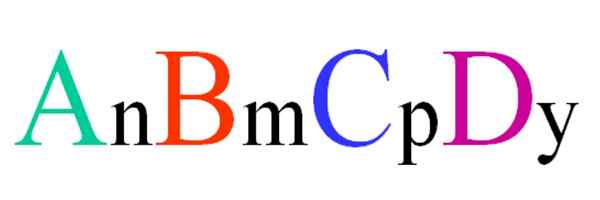
- 4860
- 1192
- Ernesto Bruen
O Compostos quaternários Eles são todos aqueles que têm quatro átomos ou íons diferentes. Portanto, eles podem ser espécies moleculares ou iônicas. Suas diversidades cobrem química orgânica e inorgânica, sendo um grupo muito volumoso; Embora talvez não tanto comparado aos compostos binários ou ternários.
A razão pela qual seu número é menor é porque os quatro átomos ou íons devem ser mantidos unidos por suas afinidades químicas. Nem todos os elementos são compatíveis entre si, e menos quando considerados um quarteto; De repente, alguns deles estão mais relacionados um do outro do que com o outro par.
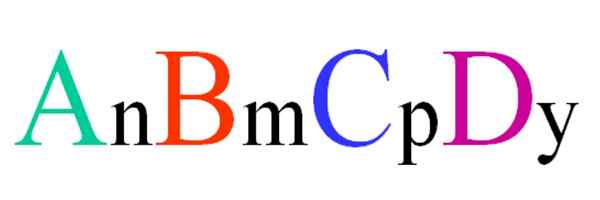 Fórmula geral e aleatória para um composto quaternário. Fonte: Gabriel Bolívar.
Fórmula geral e aleatória para um composto quaternário. Fonte: Gabriel Bolívar. Considere um composto quaternário de fórmula aleatória ABCD. Os subscritos n, m, p e y são os coeficientes estequiométricos, que por sua vez indicam qual proporção de cada átomo existe em relação aos outros.
Assim, Fórmula AnBmCpDe Será válido se atender à eletroneutralidade. Além disso, esse composto será possível se seus quatro átomos estiverem próximos um com o outro. Veremos que essa fórmula não se aplica a muitos compostos, mas especialmente para ligas ou minerais.
[TOC]
Características dos compostos quaternários
Produtos químicos
Um composto quaternário pode ser iônico ou covalente, exibindo as características esperadas para sua natureza. Espera -se que os compostos iônicos ABCD sejam solúveis em água, álcoois ou em outros solventes polares; Eles devem ter pontos de ebulição e fusão altos e ser bons motoristas de eletricidade quando se fundirem.
Em relação aos compostos covalentes ABCD, a maioria consiste em compostos orgânicos nitrogênio, oxigenado ou halogenado; isto é, sua fórmula se tornaria CnHmQUALQUERpNe ou cnHmQUALQUERpXe, X sendo um átomo de halogênio. Destas moléculas, seria lógico pensar que eram polares, dadas as altas eletronegatividades de O, N e X.
Pode atendê -lo: cloreto de sódio (NaCl)Um composto ABCD puramente covalente pode ter muitas possibilidades de link: A-B, B-C, D-A, etc., Dependendo das afinidades e capacidades eletrônicas dos átomos. Enquanto em um composto abcd puramente iônico, suas interações são eletrostáticas: um+B-C+D-, por exemplo.
No caso de uma liga, considerada mais uma mistura sólida do que um composto corretamente, o ABCD consiste em átomos neutros nos estados basais (em teoria).
Do resto, um composto ABCD pode ser neutro, ácido ou básico, dependendo da identidade de seus átomos.
Físico
Fisicamente falando, é provável que o ABCD não se torne um gás, porque quatro átomos diferentes sempre envolvem uma massa molecular maior ou formulam. Se não for um líquido com um ponto de ebulição alto, espera -se que seja sólido, cuja decomposição deve gerar muitos produtos.
Novamente, suas cores, cheiro, textura, cristais, etc., Eles estarão sujeitos à maneira como coexistem A, B, C e D no complexo e dependerão de sua sinergia e estruturas.
Nomenclatura
Até agora, a questão dos compostos quaternários foi abordada de maneira global e imprecisa. Deixando de lado a química orgânica (Amidas, cloretos de Benchilo, sais de amônio quaternário, etc.), Na química inorgânica, existem exemplos bem definidos chamados oxisals ácidos e básicos.
Oxisals ácidos
Oxisals ácidos são aqueles que derivam da neutralização parcial de um oxoácido polipótico. Assim, um ou mais de seus hidrogênios são substituídos por cátions metálicos, e o hidrogênio menos remanescente possui, menos ácido será.
Por exemplo, ácido fosfórico, h3Po4, Até dois sais ácidos podem ser obtidos, para dizer o sódio. Estes são: Nah2Po4 (N / D+ substitui um hidrogênio equivalente a h+) e na2HPO4.
Pode atendê -lo: selênio: história, propriedades, estrutura, obtenção, usosDe acordo com a nomenclatura tradicional, esses sais são nomeados, assim como os oxisais (totalmente desprotegidos), mas precedem a palavra 'ácido' ao nome do metal. Assim, o NAH2Po4 Seria fosfato de doase de sódio, e o NA2HPO4 Fosfato de ácido de sódio (porque tem um h tem.
Por outro lado, a nomenclatura de ações prefere usar a palavra 'hidrogênio' que 'ácido'. O NAH2Po4 Seria para ser di -hidrogênio de sódio e o NA2HPO4 Hidrogênio fosfato de sódio. Observe que esses sais têm quatro átomos: Na, H, P e O.
Oxisals básicos
Oxisals básicos são aqueles que contêm ânion oh em sua composição-. Por exemplo, considere Salt Cano3Oh (ca2+ NÃO3- Oh-). Para nomear, seria suficiente dar a palavra 'básico' ao nome do metal. Assim, seu nome seria: nitrato básico de cálcio. E quanto a Cuio3Oh? O nome dele seria: Cupric Basic Yodato (Cu2+ Io3- Oh-).
De acordo com a nomenclatura das ações, a palavra 'básica' é substituída por hidróxido, seguida pelo uso de um script antes do nome do oxoano.
Repetir os exemplos anteriores, seus nomes seriam para cada um: hidróxido de cálcio-nitrato e hidróxido de cobre e (ii); Lembrando que o Valencia de metal deve ser indicado entre parênteses e com números romanos.
Sais duplos
Em sais duplos, existem dois cátions diferentes interagindo com o mesmo tipo de ânion. Suponha que o sal duplo: Cu3Fé (Po4)3 (Cu2+ Fé3+ Po43-). É um fosfato de ferro e cobre, mas o nome mais apropriado para se referir a isso é: Triplo cobre (ii) e ferro (iii) fosfato.
Sais hidratados
Estes são hidratos, e a única diferença é que, no final de seus nomes, o número de formulações de água é especificado. Por exemplo, o MNCL2 É cloreto de manganês (ii).
Pode atendê -lo: benzoina: estrutura, propriedades, usos e riscosSeu hidrato, mnCl2· 4h2O é chamado cloreto de manganês (ii) tetra -hidrato. Observe que existem quatro átomos diferentes: Mn, Cl, H e O.
Um famoso sal duplo e hidratado é Mohr's, Faith (NH4)2(SW4)2· 6h2QUALQUER. Seu nome é: sulfato de ferro duplo (II) e hexa -hidrato amônio.
Treinamento
Novamente, focando em compostos quaternários inorgânicos, temos principalmente um produto de neutralizações parciais. Se isso ocorrer na presença de vários óxidos metálicos, são prováveis sais duplos; E se o meio for muito básico, os oxisals básicos precipitarão.
E se, além disso, por outro lado, as moléculas de água têm uma afinidade pelo metal, elas coordenarão diretamente com ele ou com os íons circundantes, formando os hidratos.
No lado das ligas, quatro metais ou metalóides diferentes devem ser soldados para a fabricação de capacitores, semicondutores ou transistores.
Exemplos
Finalmente, uma lista com diferentes exemplos de compostos quaternários é mostrada abaixo. O leitor pode usá -lo para testar seu conhecimento da nomenclatura:
- PBCO3(OH)2
- Cr (HSO4)3
- Nahco3
- Znioh
- Cu2(OH)2SW3
- Li2Kaso4
- CUSO4· 5h2QUALQUER
- Agau (então4)2
- Caso4· 2h2QUALQUER
- FECL3· 6h2QUALQUER
Referências
- Shiver & Atkins. (2008). Química Inorgânica. (Quarta edição). Mc Graw Hill.
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- Nomenclatura e formulação inorgânicas. [PDF]. Recuperado de: Recursos.Educação.é
- Erika thalîa bom. (2019). Sais duplos. Academia. Recuperado de: Academia.Edu
- Wikipedia. (2019). Cátion de amônio quaternário. Recuperado de: em.Wikipedia.org

