Citrato de sódio (C6H5O7NA3) Estrutura, uso, propriedades
- 1281
- 245
- Ralph Kohler
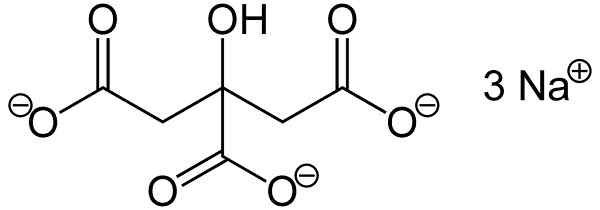
Ele citrato de sódio É o sal de sódio do ácido cítrico. É formado por um citrato de ânion c6H5QUALQUER73- e três cátions de sódio na+. Sua fórmula molecular é C6H5QUALQUER7N / D3 ou em sua forma expandida: Naooc-ch2-C (Agone) (OH) -CH2-Caminho. O citrato de sódio é a base conjugada de ácido cítrico, ou seja, o último é obtido a partir deste último substituindo cada próton h+ de -cooh para um aceno de sódio+.
Pode ser preparado em Anhydra (sem água em sua composição) ou em sua forma hidratada com 2 ou 5 moléculas de água. É um composto que quando o anidro (sem água) tende a absorver a água do meio ambiente.
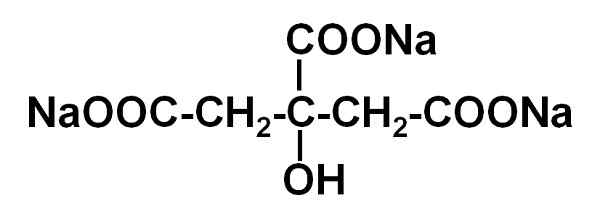 Molécula de citrato de trisódio. Autor: Marilú Stea.
Molécula de citrato de trisódio. Autor: Marilú Stea. O citrato de sódio atua como um tampão, isso significa que o pH se estabiliza, o que é uma medida da acidez ou basicidade de uma solução aquosa. Ele também tem a propriedade de formar um composto estável com os íons CA cálcio2+, Citrato de cálcio.
É usado na indústria de alimentos, por exemplo, para evitar que o leite de vaca forma os nódulos difíceis de digerir por bebês.
Nos laboratórios de bioanálise, é usado para evitar coagular o sangue de que os pacientes são extraídos para determinados testes. Também impede que ele coague o sangue usado em transfusões. É amplamente utilizado em detergentes sem fosfato porque não é poluente.
[TOC]
Estrutura
Trisodio citrato é composto de três íons de ná de sódio+ e um íon citrato.
O íon citrato é composto por uma cadeia de três átomos de carbono aos quais 3 carboxilatos estão unidos- (um para cada átomo de carbono) e um hidroxil -OH no carbono central.
Cada um dos 3 íons Na+ está ligado a um grupo -COO-.
 Estrutura de citrato de trissódio. Jü [domínio público]. Fonte: Wikimedia Commons.
Estrutura de citrato de trissódio. Jü [domínio público]. Fonte: Wikimedia Commons. Nomenclatura
- Citrato de sódio
- Trisodio citrato
- 2-hidroxipropano-1,2,3-tricarboxilato trissodium
Propriedades
Estado físico
Sólido cristalino branco ou incolor.
Peso molecular
258,07 g/mol
Ponto de fusão
300 ºC
Solubilidade
É muito solúvel em água: 42,5 g/100 ml a 25 ºC. É praticamente insolúvel em álcool.
ph
Uma solução aquosa para o citrato de sódio a 5% tem um pH entre 7,5 e 9,0, ou seja, é ligeiramente alcalino.
Propriedades quimicas
O citrato de sódio é um tampão, o que significa que estabiliza o pH, que é uma medida da acidez ou alcalinidade de uma solução aquosa. Citrato ao estabilizar o pH não permite que a solução seja acidificada ou alcalinizada acima de certos valores.
Pode atendê -lo: Configuração eletrônica do kernel: construção, exemplosQuando há excesso de prótons h+ Eu os levo para converter seus grupos -COO- Em grupos -coh. Vice -versa, se houver muitos grupos OH- produz os prótons de seus grupos -Coh e os torna -COO-.
Quando transformado pelo corpo, ele fornece 3 moléculas de HCO3- Para cada molécula de citrato.
Outras propriedades
Seus cristais são deliciosos, ou seja, eles absorvem o ar do ar. O citrato de sódio di -hidratado é mais estável no ar.
Se o di -hidrato for aquecido, quando atingir 150 ºC, ele se torna anidro (sem água).
Como o ácido cítrico, o citrato de sódio tem sabor azedo.
Obtenção
O citrato de sódio é geralmente obtido adicionando carbonato de sódio a uma solução de ácido cítrico até que a efervescência cessasse. EferveScence é devido ao destacamento de dióxido de carbono2:
N / D2Co3 + Ácido cítrico → citrato de sódio + CO2↑
Então a água da solução evapora para cristalizar o produto.
Também pode ser preparado tratando uma solução de sulfato de sódio com citrato de cálcio:
N / D2SW4 + Citrato de cálcio → citrato de sódio + caixa4↓
A solução é filtrada para remover o estojo4 Sólido que precipitou. Então a solução é concentrada e, portanto, cristaliza o citrato de sódio.
Localização na natureza
O citrato de sódio é a base conjugada de ácido cítrico, que é um composto natural encontrado em todos os organismos vivos porque faz parte de seu metabolismo, que é o mecanismo para desenvolver energia nas células.
Formulários
Na indústria de alimentos
O citrato de sódio tem vários usos na indústria de alimentos, por exemplo, como regulador de acidez, seqüestro, estabilizador, agente de surfactante ou emulsificante.
É usado em bebidas, sobremesas congeladas e queijos especiais, entre outros produtos.
Ele permite evitar a coagulação do leite, por isso é adicionado ao leite da vaca usado para a alimentação de bebês. Dessa forma, sem coagis ou cachos mais difíceis são criados pelo estômago dos mais pequenos.
 Você pode adicionar citrato de sódio ao leite para que os caroços não sejam formados no estômago. Autor: Couleur. Fonte: Pixabay.
Você pode adicionar citrato de sódio ao leite para que os caroços não sejam formados no estômago. Autor: Couleur. Fonte: Pixabay. É usado para acelerar a fixação de cores em carnes de porco ou vacinas curadas, ou seja, carne tratada para evitar sua decomposição. Até 50% de ácido ascórbico é substituído nestes.
Pode atendê -lo: ácido silícico Carne curada de porco que provavelmente contém citrato de sódio. Autor: Ben Kerckx. Fonte: Pixabay.
Carne curada de porco que provavelmente contém citrato de sódio. Autor: Ben Kerckx. Fonte: Pixabay. Também serve para evitar a coagulação sanguínea em carne de vacina fresca (como bifes).
Em medicina
É usado como um agente alcalinista, uma vez que neutraliza o excesso de ácido no sangue e na urina. É indicado para tratar a acidose metabólica que ocorre quando o corpo produz muito ácido.
Uma vez que o íon citrato é ingerido, torna -se um íon bicarbonato que é um agente alcalingo sistêmico (ou seja, todo o corpo) e, como conseqüência, os íons h neutralizam+, Aumenta o pH do sangue e reverte ou elimina a acidose.
O citrato de sódio serve como um agente neutralizante para desconforto estomacal.
É usado como expectorante e suor. Tem ação diurética. Aumentar a excreção urinária de cálcio, que é usada na hipercalcemia, que é quando há excesso de cálcio no sangue.
Também serve para facilitar a eliminação de chumbo ao envenenar com este metal ocorre.
Se o excesso for administrado, a alcalose pode ser produzida, espasmos musculares devido.
Citrato de sódio é usado em transfusões. É adicionado ao sangue junto com dextrose para evitar sua coagulação.
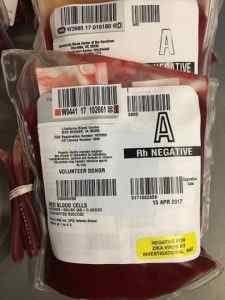 Sangue armazenado para transfusões. Provavelmente contém citrato de sódio. Autor: Kshirl02. Fonte: Pixabay.
Sangue armazenado para transfusões. Provavelmente contém citrato de sódio. Autor: Kshirl02. Fonte: Pixabay. Normalmente, o fígado metaboliza rapidamente o citrato obtido na transfusão, no entanto, durante transfusões de grandes quantidades, a capacidade do fígado pode ser excedida.
Nesses casos, uma vez que o citrato forma um complexo com cálcio, é uma diminuição no íon de cálcio da CA2+ No Sangue. Isso pode gerar atordoamento, tremores, formigamento, etc. Portanto, as transfusões devem ser realizadas lentamente.
Na indústria farmacêutica
Entre muitos outros usos, é usado para evitar o escurecimento dos medicamentos nos quais existem ferro e taninos.
Em análise de sangue
É usado como um anticoagulante na coleta de sangue ou quando deve ser armazenado, pois atua como um peito de cálcio CA CA2+, isto é, ele se liga a íons de cálcio que formam citrato de cálcio que não é ionizado.
Pode servir a você: link iônico: características, como é formado e exemplosÉ usado em testes de coagulação e na determinação da velocidade de sedimentação dos glóbulos vermelhos.
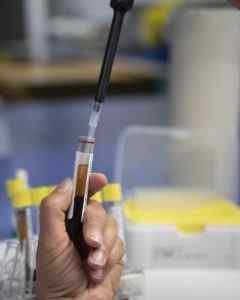 Análise de sangue. Autor: Bokskopet. Fonte: Pixabay.
Análise de sangue. Autor: Bokskopet. Fonte: Pixabay. É usado como um anticoagulante durante a plasmaférese, procedimento para extrair do excesso de sangue de substâncias prejudiciais ao corpo.
Na síntese de nanopartículas
É usado como um estabilizador na síntese de nanopartículas de ouro. É adicionado o citrato de trisodio di -hidratado ao ácido cloroárico, formando uma suspensão de vinho tinto.
O citrato de sódio serve como um agente redutor e como um agente anti -regência, pois é adsorvido em nanopartículas.
Devido à carga negativa de citrato, as partículas repelirem uma com a outra, evitando e formando uma dispersão estável. Quanto maior, a menor concentração de citrato é as partículas.
Essas nanopartículas servem para preparar biossensores médicos.
Em detergentes amigáveis
O citrato de sódio é amplamente utilizado em detergentes líquidos sem fosfato. Isso ocorre porque seu comportamento ambiental é inofensivo porque é um metabolito encontrado em todos os organismos vivos.
É facilmente biodegradável e fracamente tóxico para a vida aquática. Por esse motivo, considera -se que é um agente de limpeza com características ecologicamente favoráveis.
Ao melhorar a exploração de areias betuminosas
Areias betuminosas são formações arenosas ricas em betume ou alcatrão, um material semelhante ao óleo.
O citrato de sódio foi testado com sucesso junto com o hidróxido de sódio Naoh para extrair óleo de areias betuminosas.
Pensa -se que quando o citrato com o arenito, os íons -coo- de citrato formam um grande número de cargas negativas em partículas de sílica. Isso produz uma melhor separação da areia do betume pela simples repelência das cargas negativas do cascalho das cargas negativas do betume.
Em outras aplicações
É usado na fotografia, para remover metais de rastreamento, em eletrodeposição e remover2 de gases residuais.
Referências
- OU.S. Biblioteca Nacional de Medicina. (2019). Citrato de sódio. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov.
- McNamara, c. (2017). Coleção e manuseio de sangue. Em Dacie e Lewis Hematologia Prática (décima segunda edição). Recuperado de cientedirect.com.
- Sede, J. (2007). A ecotoxicidade da limpeza dos ingredientes do produto. No manual para limpeza/descontaminação de superfícies. Recuperado de cientedirect.com.
- Xiang, b. et al. (2019). Estudo do papel do citrato de sódio na libertação de betume. Energy Fuels 2019, 33, 8271-8278. Recuperado de bares.ACS.org.
- Heddle, n. e Webert, k.E. (2007). Transfusão de medicina. Em Blood Banking e Medicine. Recuperado de cientedirect.com.
- Sudhakar, s. e Santhosh, P.B. (2017). Nanomateriais de ouro. Nos avanços nas biomembranas e lipídios auto-asssamente. Recuperado de cientedirect.com.
- Elsevier (Editorial) (2018). Capítulo 8. Nanometal. Em fundos e aplicações de nano silício em plasmônicos e fullines. Tendências atuais e futuras Micro e Nano Technologies. Páginas 169-203. Recuperado de cientedirect.com.
- « Schi -Source, receitas, refeições na América Latina
- História e significado da bandeira da Sérvia »

