Estrutura do ácido tricloroacético, propriedades, síntese, usos, efeitos

- 3053
- 744
- Gilbert Franecki
Ele Ácido tricloroacético É um composto orgânico sólido cuja fórmula química é c2Hcl3QUALQUER2 ou ccl3-COOH. Também é conhecido como ácido tricloroetanóico e como TCA. É um ácido monocarboxílico no qual os hidrogênios do segundo átomo de carbono foram substituídos por cloro. Seus cristais são incolores para os brancos.
O TCA é muito solúvel em água, gerando soluções muito ácidas. Pode precipitar as proteínas de uma solução aquosa. O contato prolongado com o ácido tricloroacético pode gerar queimaduras na pele.
 Cristais de ácido tricloroacético CCL3COOH. Lem [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikipedia Commons.
Cristais de ácido tricloroacético CCL3COOH. Lem [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikipedia Commons. No entanto, isso tem sido usado vantajosamente para tratar os distúrbios da pele, como é usado em solução diluída e muito bem controlada. O TCA também é frequentemente usado no So -chamado DESCAMAÇÃO Químico para rejuvenescimento da pele.
Por outro lado, sendo um composto organizado encontrado no ambiente em pequenas proporções, foi responsável como uma possível causa de dano às florestas.
Apesar de seu conteúdo de elementos de cloro, não há dados que confirmam se o ácido tricloroacético é um carcinogênio.
[TOC]
Estrutura
O ácido tricloroacético é um ácido monocarboxílico, ou seja, que contém um único grupo de Coh. Seu esqueleto contém apenas 2 átomos de carbono. É semelhante ao ácido acético CH3-COOH, mas em vez do grupo metil -chap3, Tem um grupo -cl3, isto é, sua fórmula é CCL3-COOH.
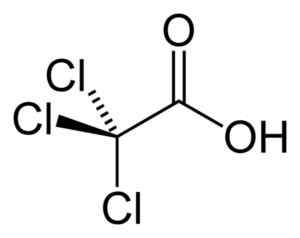 Estrutura da molécula de ácido tricloroacético CCL3-COOH. Benjah-BMM27 [domínio público]. Fonte: Wikipedia Commons.
Estrutura da molécula de ácido tricloroacético CCL3-COOH. Benjah-BMM27 [domínio público]. Fonte: Wikipedia Commons. Nomenclatura
- Ácido tricloroacético
- Ácido tricloroetanóico
- Ácido 2,2,2-crítico
- TCA (sigla para inglês Ácido tricloroacético)
Propriedades
Estado físico
Sólido cristalino Solid Color to White. Seus cristais são Rhomboédica
Peso molecular
163,38 g/mol
Ponto de fusão
57,5 ºC
Ponto de ebulição
195.5 ºC
Densidade
1,6 g/cm3
Solubilidade
Solubilidade de água muito boa: 120 g/100 ml a 25 ° C.
Solúvel em etanol Cho3CH2Oh e em dietyl éter3CH2OCH2CH3. Ligeiramente solúvel em tetracloreto de carbono CCL4.
Pode servir você: óxido beril (Beeo)ph
O pH de uma solução aquosa com 0,1 moles/L é 1,2.
Constante de dissociação
Pkpara = 0,51 (significa que é um ácido mais forte que o ácido acético)
Propriedades quimicas
O ácido tricloroacético é um sólido higroscópico, absorve a umidade do ar formando um líquido viscoso. Tem um acre ou cheiro picante.
Ao se dissolver na água, a liberação de calor ocorre. É corrosivo em relação a metais como ferro, zinco e alumínio e para tecidos biológicos. É extremamente corrosivo para a pele humana em contato prolongado.
Tem a propriedade de precipitar proteínas em solução.
Quando aquecido com álcalis para decomposição emite fumaça tóxica de clorofórmio ch CH3Cl, ácido clorídrico HCl, dióxido de carbono2 e monóxido de carbono.
Nas fontes consultadas, não há consenso sobre se é ou não carcinogênico.
Síntese
É preparado no nível industrial por cloração de ácido acético CH3-COOH, com cloro cl2 na presença ou não em catalisadores.
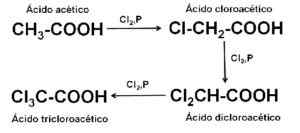 Síntese de ácido tricloroacético CCL3COOH. Autor: Marilú Stea.
Síntese de ácido tricloroacético CCL3COOH. Autor: Marilú Stea. Uso na análise de proteínas
O ácido tricloroacético é amplamente utilizado para determinação de proteínas, como albumina. É um agente muito eficaz para sua precipitação, especialmente de soluções de proteínas diluídas.
A precipitação ocorre especificamente e quantitativamente, permitindo que eles os separem de outras substâncias não proteínas, como polissacarídeos, cátions unidos a proteínas e sais e permite desnaturalizar proteases (enzimas que permitem quebrar proteínas).
De acordo com a literatura consultada, muito não se sabe sobre o que é o mecanismo de precipitação. Foi sugerido que a forma dominante poderia ser agregação hidrofóbica, pois há um intervalo, cerca de 15% do ácido trifluoroacético, no qual ocorre a precipitação ideal.
Usos terapêuticos
As soluções diluídas do TCA foram usadas com sucesso no tratamento de otite aguda externa (dor na orelha na área antes do tímpano ou canal auditivo externo).
O TCA desativa as células inflamatórias, mudando suas propriedades, secando a região inflamada, reduzindo o edema e rapidamente aliviado a dor. Também é tolerado muito bem por pacientes, crianças e adultos.
Pode atendê -lo: hidróxido de bário (BA (OH) 2)Além disso, restaura o estado ácido da área, inibindo a proliferação de bactérias e fungos na fase aguda da doença. Seu mecanismo de ação impede a recorrência e progressão da doença em fase crônica.
Uso em tratamentos dermatológicos
Para distúrbios da pele
Ele tem sido usado no tratamento da queratose actínica, que é uma doença da pele que é caracterizada por uma área escamosa que é formada em áreas de pele crônica por anos para radiação UV, como face, couro cabeludo ou antebraços.
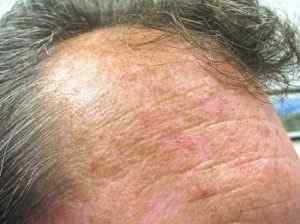 Queratose actínica. FUTURO FAMDOC [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikipedia Commons.
Queratose actínica. FUTURO FAMDOC [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikipedia Commons. Uma pequena porcentagem dessa doença leva ao câncer de pele, daí a importância de tratá -la no tempo.
Também é usado para rosácea, dermatite seborréica, acne, xantelass (pequenos inchaços de gordura benigna), verrugas, toupeiras e hiperpigmentação.
O procedimento é chamado queima ou DESCAMAÇÃO O ácido químico e tricoloacético é preferido em outros compostos químicos devido à sua segurança, eficácia e não toxicidade sistêmica.
O TCA destrói quimicamente a epiderme e a derme superior da área tratada. A nova epiderme migra dos anexos cutâneos sob o tecido destruído, após o que os córtexos sobrejacentes surgem em alguns dias.
A regeneração dérmica é evidente em 2 a 3 semanas. Alterações histológicas na pele são a homogeneização da arquitetura de colágeno e um aumento no tecido elástico na derme.
Essas mudanças são permanentes. Além disso, as células anômalas são removidas e substituídas por células normais epidérmicas.
Para tratamentos cosméticos
Queima ou esfoliação ou DESCAMAÇÃO Com o ácido tricloroacético, também é usado no tratamento cosmético de pele envelhecida e enrugada, cicatrizes de acne e tatuagens.
 Rugas. Autor: Kelsey Vere. Fonte: Pixabay.
Rugas. Autor: Kelsey Vere. Fonte: Pixabay. Pode produzir uma pele relativamente profunda queimada sem produzir toxicidade sistêmica. Os tratamentos devem sempre ser realizados por pessoal treinado e experiente.
As variáveis a levar em consideração para o sucesso da técnica são a concentração adequada de ácido de acordo com o tipo e a espessura da pele, a técnica de aplicação, a eficácia da preparação, densidade e atividade da pele anteriores das glândulas sebáceas e aplicação de agentes queratolíticos antes do tratamento.
Pode servir você: hidróxido de zinco (Zn (OH) 2)Cada paciente deve ser avaliado para selecionar a concentração adequada e evitar resultados desastrosos.
Efeito da poluição do TCA
O ácido tricloroacético é um composto químico presente no ar, chuva, vegetação e solo. Por esse motivo, ele foi envolvido como responsável por efeitos adversos em algumas florestas e selvas.
 floresta de pinheiros. Autor: Paul Gilmore. Fonte: UNSPASH
floresta de pinheiros. Autor: Paul Gilmore. Fonte: UNSPASH Há incerteza em relação às fontes do TCA no ambiente. Embora exista um consenso que possa vir da oxidação de solventes clorados presentes na atmosfera, as concentrações de TCA encontradas nas chuvas são muito maiores do que se esperaria se fosse esses solventes.
O TCA também pode ocorrer no chão e se degradar neste. As plantas podem pegar o TCA do ar e do solo e ser transportado das folhas para a raiz e vice -versa. Estima -se que seja metabolizado na folhagem.
Nos testes realizados por alguns pesquisadores em mudas de um tipo de pinheiro tratado com níveis de ácido tricloroacético semelhantes aos encontrados no ar em algumas áreas da Europa, EUA e Canadá, verificou -se que não há danos visíveis às plantas ou alterações nas mudanças no crescimento delas devido ao TCA.
Apenas uma certa diminuição no teor de proteínas das plantas tratadas com TCA foi encontrada, possivelmente devido à propriedade do ácido tricloroacético de proteínas precipitantes.
Referências
- Novák, p. e Havlícek, V. (2016). Proteína de extração e precipitação. Em perfil proteômico e química analítica (segunda edição). Recuperado de cientedirect.com.
- OU.S. Biblioteca Nacional de Medicina. (2019). Ácido tricloroacético. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Cape, n.J. et al. (2003). Exposição a longo prazo de mudas de abeto sitka ao ácido tricloroacético. Ambiente. Sci. Technol. 2003, 37, 2953-2957. Recuperado de bares.ACS.org.
- Brodland, d.G. et al. (1988). Chemexfoliação de ácido tricloroacético (casca química) para um amplo dano actínico pré -saligno da face e do couro cabeludo. Maio Clin Proc 63: 887-896, 1988. NCBI se recuperou.Nlm.NIH.Gov.
- Collins, p.S. (1989). Revisão do ácido tricloroacético. Dermatol. Surg. Oncol. 1989; 15: 933-940. Recuperado da biblioteca online.Wiley.com.
- Kantas, i. et al. (2007). O uso de ácido tricloroacético no tratamento da otite externa acotte. Eur Arch Irhinolaryngol (2007) 264: 9-14. NCBI se recuperou.Clm.NIH.Gov.
- « Terceira Lei de Fórmulas, Equações, Exemplos de Termodinâmica
- Que papel as pessoas desempenham na eficiência energética? »

