Ácido acético (CH3cooh)
- 631
- 61
- Conrad Schmidt
 O ácido acético é responsável pelo sabor característico e cheiro de vinagre
O ácido acético é responsável pelo sabor característico e cheiro de vinagre O que é ácido acético?
Ele ácido acético, o ácido estanóico, é um líquido orgânico incolor cuja fórmula química é CHO3COOH. Está presente em vinagre, o que dá seu cheiro e sabor característicos. O vinagre é uma solução aquosa de ácido acético com uma concentração de 5%, aproximadamente.
Como o nome indica, é um composto ácido e, portanto, o vinagre tem valores de pH inferiores a 7. Na presença de seu sal de acetato, constitui um sistema de amortecimento eficaz na regulação do pH entre 2,76 e 6,76, ou seja, mantém o pH dentro desse intervalo contra adições moderadas de uma base ou ácido.
Após o ácido fórmico, Hcooh, é um dos ácidos orgânicos mais simples, que também representa o ponto final de muitos processos de fermentação. É comumente usado para vestir alimentos e também para eliminar impurezas e microorganismos de vegetais.
História
O humano usou a fermentação de inúmeras frutas, legumes, cereais etc., Para obter bebidas alcoólicas, o produto da transformação de açúcares, como glicose, em etanol, CH3CH2Oh.
Provavelmente porque o método inicial para a produção de álcool e vinagre é a fermentação, talvez tentando produzir álcool em um momento indeterminado, muitos séculos atrás, o vinagre foi obtido por engano.
Já no terceiro século para.C., O filósofo grego Theophofastus descreveu a ação do vinagre em metais para a produção de pigmentos, como o chumbo branco.
1800
Em 1823, um equipamento em forma de torre foi projetado na Alemanha para fermentação aeróbica de diferentes produtos, a fim de obter ácido acético na forma de vinagre.
Em 1846, Herman Foelbe alcançou pela primeira vez a síntese do ácido acético através do uso de compostos inorgânicos. A síntese começou com a cloração de dissulfeto de carbono e concluiu, após duas reações, com uma redução eletrolítica ao ácido acético.
No final do século XIX e início do século XX, devido a J J. Weizmann começou a usar as bactérias Clostridium acetobutylicum Para a produção de ácido acético, através da fermentação anaeróbica.
Pode atendê -lo: relacionamento de química e tecnologia com ser humano, saúde e meio ambiente1900
No início do século XX, a tecnologia dominante foi a produção de ácido acético por oxidação de acetaldeído.
Em 1925, Henry Dreyfus, da Companhia Britânica Celanese, projetou uma planta piloto para carbonilação de metanol. Posteriormente, em 1963, a empresa alemã BASF introduziu o uso de cobalto como catalisador.
Otto Hromatka e Heinrich Ebner (1949), projetaram um tanque com um sistema de agitação e suprimento de ar para fermentação aeróbica, destinada à produção de vinagre. Este implemento, com algumas adaptações, permanece em uso.
Em 1970, a empresa norte -americana Monsanto usou um sistema de catalisadores baseados no ródio para carbonilação de metanol.
Posteriormente, a empresa BP em 1990, apresenta o procedimento Cativa com o uso do catalisador de iridium para o mesmo objetivo. Este método acabou sendo mais eficiente e menos ambientalmente agressivo do que o método Monsanto.
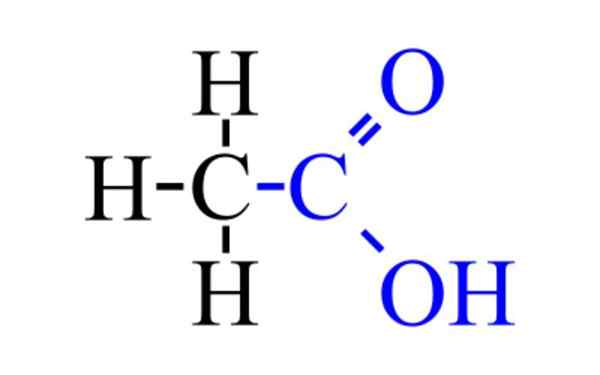
Estrutura do ácido acético
 Estrutura de ácido acético químico
Estrutura de ácido acético químico A imagem superior mostra a estrutura do ácido acético representado com um modelo de esferas e barras. As esferas vermelhas correspondem aos átomos de oxigênio, que por sua vez pertencem ao grupo carboxil, -cooh. Portanto, é um ácido carboxílico. No lado direito da estrutura, você tem o grupo metil, -ch3.
Como pode ser visto, é uma molécula muito pequena e simples. Tem um momento de dipolo permanente devido ao grupo -Cooh, que também permite que o ácido acético forme duas pontes consecutivamente de hidrogênio.
São essas pontes que guiam espacialmente as moléculas de CH3COOH para formar cenas no estado líquido (e gás).
 Duas pontes de hidrogênio
Duas pontes de hidrogênio Na imagem, observa-se como as duas moléculas são organizadas para formar as duas pontes de hidrogênio: O-H-O e O-H-O.
Para evaporar o ácido acético, a energia suficiente deve ser fornecida para quebrar essas interações, e é por isso que é um líquido com um ponto de ebulição maior que a água (aproximadamente 118 ° C).
Propriedades físicas e químicas do ácido acético
Nomes químicos
Ácido:
Pode atendê -lo: brometo de alumínio- Acético
- Etanóico
- Etilo
Fórmula molecular
C2H4QUALQUER2 ou cap3COOH.
Aspecto físico
Líquido incolor.
Cheiro
Acre característico.
Sabor
Queimar.
Ponto de ebulição
244 ºF a 760 mmHg (117,9 ºC).
Ponto de fusão
61,9 ºF (16,6 ºC).
ponto de ignição
112 ºF (vidro aberto) 104 ºF (vidro fechado).
Solubilidade em água
106 mg/ml a 25 ºC (é miscível em todas as proporções).
Solubilidade em solventes orgânicos
É solúvel em etanol, éter etílico, acetona e benzeno. Também é solúvel em tetracloreto de carbono.
Densidade
1.051 g/cm3 a 68 ºf (1.044 g/cm3 a 25 ºC).
Densidade de vapor
2.07 (com relação aérea = 1).
Pressão de vapor
15,7 mmHg a 25 ºC.
Decomposição
Quando é aquecido a mais de 440 ºC, se decompõe para produzir dióxido de carbono e metano.
Gosma
1.056 mPascal a 25 ° C.
Corrosividade
O ácido acético glacial é altamente corrosivo e sua ingestão pode causar lesões graves de esôfago e piloro em humanos.
Calor de combustão
874,2 kJ/mol/mol.
Calor de vaporização
23,70 kJ/mol a 117,9 ºC.
23,36 kJ/mol a 25,0 ºC.
ph
- Uma solução de concentração de 1 m tem um pH de 2,4.
- Para uma solução de 0,1M, seu pH é 2,9.
- E 3,4 se a solução for 0,01m.
Tensão superficial
27,10 mn/m a 25 ºC.
Pka
4,76 a 25 ºC.
Reações químicas
O ácido acético é corrosivo para muitos metais, liberando o gás h2 e formando sais de metal chamados acetatos. Com exceção do acetato de cromo (II), os acetatos são solúveis em água.
Sua reação com magnésio é representada com a seguinte equação química:
Mg (s) +2 CHO3COOH (AG) => (CH3COO)2Mg (ag) +h2 (g)
Por redução, o ácido acético forma etanol. Você também pode formar anidrido acético devido à perda de água de duas moléculas de água.
Usos de ácido acético
Industriais
- O ácido acético reage com o etileno na presença de oxigênio para formar o monômero de acetato de vinil, usando paládio como um catalisador para a reação. Acetato de vinil polimeriza em acetato de polivinil, que é usado como um componente de pinturas e material adesivo.
- Reage com diferentes álcoois para a produção de ésteres, incluindo acetato de etila e acetato de propila. Os ésteres de acetato são usados como solventes de tinta, nitrocelulose, revestimentos, vernizes e lacas acrílicos.
Pode atendê -lo: liga- Ao condensar duas moléculas de ácido acético, o anidrido acético é formado, CH3Co-O-Coch3. Este composto intervém na síntese de acetato de celulose, um polímero que constitui um tecido sintético e é usado na elaboração de filmes fotográficos.
Como um solvente
- É um solvente polar capaz de dissolver compostos polares, como sais inorgânicos e açúcares, mas também dissolve compostos não polares, como óleos e gorduras. Além disso, o ácido acético é miscível com solventes polares e não polares.
- A miscibilidade do ácido acético nos alcanos depende da extensão da cadeia delas: à medida que o comprimento da corda dos alcaneos aumenta, sua miscibilidade com ácido acético diminui.
Médicos
- O ácido acético diluído é usado como um anti -séptico, aplicado topicamente, com a capacidade de atacar bactérias como estreptococos, estafilococos e Pseudomonas. Devido a esta ação, é usada no tratamento de infecções de pele.
- É usado na endoscopia do esôfago Barrett, uma condição na qual o revestimento de esôfago é modificado, tornando -se semelhante à fenda do intestino delgado.
- Um gel de ácido acético a 3% parece ser um adjuvante eficaz para o tratamento com o medicamento vaginal no misoprostol, induzindo aborto médico no trimestre médio, especialmente em mulheres com pH vaginal de 5 ou mais.
- É usado como substituto para esfoliação química. No entanto, surgiram complicações com esse uso, pois foi relatado, pelo menos, um caso de queimaduras sofridas por um paciente.
- É usado como corante para detectar papilomavírus humano (HPV).
Na comida
O vinagre tem sido usado como condimento e sabor de alimentos há séculos, então esta é a aplicação mais conhecida do ácido acético.
Referências
- O que é ácido etanóico? Recuperado de Byjus.com
- ÁCIDO ACÉTICO. Recuperado de PubChem.NCBI.Nlm.NIH.Gov
- Ácido acético glacial. Recuperado do ChemicalBook.com

