Cetogênese tipos de corpos, síntese e degradação
- 1261
- 67
- Ernesto Bruen
O cetogênese É o processo pelo qual o acetoacetato, β-hidroxibutirato e acetona são obtidos, que juntos são chamados corpos de cetona. Este mecanismo complexo e finamente regulado é realizado em mitocôndrias, do catabolismo dos ácidos graxos.
Obtenção dos corpos cetona ocorre quando o corpo está sujeito a períodos exaustivos de jejum. Embora esses metabólitos sejam sintetizados principalmente nas células hepáticas, elas são encontradas como uma importante fonte de energia em tecidos variados, como músculo esquelético e no coração e tecidos cerebrais.
 Fonte: SAV VAS [CC0]
Fonte: SAV VAS [CC0] Β-hidroxibutirato e acetoacetato são metabólitos usados como substratos no músculo cardíaco e na casca de rim. No cérebro, os corpos de cetona se tornam importantes fontes de energia quando o corpo esgotou sua reserva de glicose.
[TOC]
Características gerais
A cetogênese é considerada uma rota fisiológica ou metabólica muito importante. Geralmente, esse mecanismo é realizado no fígado, embora tenha sido demonstrado que pode ser realizado em outros tecidos capazes de metabolizar ácidos graxos.
A formação de corpos de cetona é a principal derivação metabólica de acetil-CoA. Este metabólito é obtido a partir da rota metabólica conhecida como oxidação β, que é a degradação dos ácidos graxos.
A disponibilidade de glicose nos tecidos onde a β-oxidação ocorre determina o destino metabólico do acetil-CoA. Em situações particulares, os ácidos graxos oxidados são direcionados quase inteiramente à síntese de corpos de cetona.
Tipos e propriedades de corpos de cetona
O principal corpo cetônico é o acetoacetato ou o ácido acetoacético, que é sintetizado principalmente em células hepáticas. Do acetoacetato, as outras moléculas que compõem os corpos cetona são derivados.
A redução do ácido acetoacético dá origem a D-β-hidroxibutirato, o segundo corpo cetônico. A acetona é um composto difícil de se degradar e é produzida por uma reação espontânea de descarboxilação do acetoacetato (portanto, não requer intervenção de nenhuma enzima), quando está presente em altas concentrações no sangue.
A denominação dos corpos de cetona foi organizada por convenção, pois estritamente falando β-hidroxibutirato não tem uma função de cetona. Essas três moléculas são solúveis em água, o que facilita o transporte de sangue. Sua principal função é fornecer energia a certos tecidos como músculo esquelético e cardíaco.
As enzimas envolvidas na formação de corpos de cetona estão principalmente no fígado e nos rins, o que explica que esses dois locais são os principais produtores desses metabólitos. Sua síntese ocorre apenas e exclusivamente na matriz mitocondrial das células.
Pode atendê -lo: esporulação: em plantas, em fungos e em bactériasDepois que essas moléculas foram sintetizadas, elas vão para a corrente sanguínea que aborda os tecidos que os exigem, onde se degradam até acetil-coa.
Síntese de corpos de cetona
Condições para cetogênese
O destino metabólico do acetil-CoA da β-oxidação depende dos requisitos metabólicos do organismo. Isso é oxidado para CO2 e h2Ou por meio do ciclo do ácido cítrico ou a síntese de ácidos graxos, se o metabolismo de lipídios e carboidratos estiver estável no corpo.
Quando o corpo precisa de carboidratos, o oxalacetato é usado para fabricação de glicose (gliconeogênese) em vez de iniciar o ciclo do ácido cítrico. Isso acontece, como mencionado, quando o corpo tem alguma incapacidade de obter glicose, em casos como o jejum prolongado ou a presença de diabetes.
Devido a isso, o acetil-CoA resultante da oxidação de ácidos graxos é usado para a produção de corpos de cetona.
Mecanismo
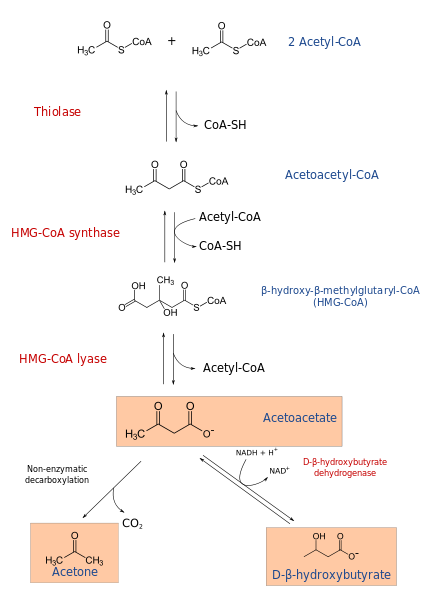
O processo de cetogênese começa a partir dos produtos da β-oxidação: acetacetil-CoA ou acetil-CoA. Quando o substrato é acetil-CoA, o primeiro passo consiste na condensação de duas moléculas, a reação de acetil-coa transferase, para produzir acetacetil-CoA.
O acetacetil-CoA é condensado com um terceiro acetil-CoA pela ação da HMG-CoA sintase, para produzir hmg-coa (β-hidroxi-β-metilglutaril-coa). O HMG-CoA é degradado para acetoacetato e acetil-CoA por ação hmg-coa liasa. Dessa maneira, o primeiro corpo cetônico é obtido.
O acetoacetato é reduzido a β-hidroxibutirato pela intervenção da β-hidroxibutirato desidrogenase. Esta reação depende do NADH.
O principal corpo de acetoacetato cetônico é um β-cetóácido, que experimenta descarboxilação não enzimática. Este processo é simples e produz acetona e CO2.
Esta série de reações resulta em corpos de cetona. Estes sendo solúveis em água podem ser transportados de maneira simples através da circulação sanguínea, sem a necessidade de ancorar em uma estrutura de albumina, como é o caso de ácidos graxos que são insolúveis em meio aquoso.
Β-oxidação e cetogênese estão relacionados
O metabolismo de ácidos graxos produz substratos para cetogênese, portanto essas duas maneiras são funcionalmente relacionadas.
O acetoacetil-CoA é um inibidor do metabolismo dos ácidos graxos, pois interrompe a atividade da acila-coa desidrogenase que é a primeira enzima de β-oxidação. Além disso, também exerce inibição na transferência de acetil-CoA e hmg-coa sintase.
A enzima HMG-CoA sintase, sujeita à CPT-I (enzima envolvida na produção de acil carnitina na β-oxidação), representa um importante papel regulatório na formação de ácidos graxos.
Pode atendê -lo: flora e fauna de Zacatecas: espécies mais representativasRegulação da β-oxidação e seu efeito na cetogênese
A alimentação do organismo regula um conjunto complexo de sinais hormonais. Carboidratos, aminoácidos e lipídios consumidos na dieta são depositados na forma de triacilgliceroles no tecido adiposo. Insulina, um hormônio anabólico, intervém na síntese de lipídios e na formação de triacilgliceroles.
No nível mitocondrial, a oxidação da β é controlada pela entrada e participação de alguns substratos nas mitocôndrias. A enzima CPT I sintetiza carnitina acil da ACIL citosólica ACIL.
Quando o corpo é alimentado, o acetil-coa carboxilase e o citrato aumentam os níveis de CPT I, enquanto diminui sua fosforilação (reação dependente da AMP cíclica).
Isso causa um acúmulo de Malonil CoA, que estimula a síntese de ácidos graxos e bloqueia sua oxidação, impedindo que um ciclo fútil seja gerado.
No caso do jejum, a atividade da carboxilase é muito baixa porque os níveis da enzima CPT eu foi reduzida e também fosforilados, ativando e promovendo a oxidação de lipídios, que subsequentemente permitirão a formação dos corpos de cetona através de acetil -Coa.
Degradação
Os corpos de cetona espalhados para fora das células onde foram sintetizados e são transportados para os tecidos periféricos pela corrente sanguínea. Nestes tecidos, eles podem ser oxidados através do ciclo de ácidos tricarboxílicos.
Nos tecidos periféricos β-hidroxibutirato é oxidado para acetoacetato. Posteriormente, o presente acetoacetato é ativado pela ação da enzima 3-ZOA transferase.
Succinil-CoA atua como um doador de COA se tornando succinata. A ativação do acetoacetato ocorre para evitar succinil-coA.
O aceoacetil-CoA resultante sofre uma ruptura tiolítica produzindo duas moléculas de acetil-CoA que são incorporadas ao ciclo de ácidos tricarboxílicos, mais conhecidos como ciclo de Krebs.
As células hepáticas não têm a transferência 3-cotoacil-CoA, impedindo que esse metabolito seja ativado nessas células. Dessa maneira, é garantido que os corpos cetona não oxidam nas células onde foram produzidos, mas que podem ser transferidos para os tecidos onde sua atividade é necessária.
Relevância médica dos corpos de cetona
No corpo humano, altas concentrações de corpos de cetona no sangue podem causar condições especiais chamadas acidose e cetonemia.
Pode atendê -lo: esfingomia: o que é, estrutura, funções, sínteseA fabricação desses metabólitos corresponde ao catabolismo de ácidos graxos e carboidratos. Uma das causas mais comuns de uma condição de cetogênese patológica é a alta concentração de fragmentos dicarbonados acéticos que não se degradam na via de oxidação de ácidos tricarboxílicos.
Como conseqüência, há um aumento nos níveis de corpos de cetona de sangue acima de 2 a 4 mg/100 N e sua presença na urina. Isso se traduz na perturbação do metabolismo intermediário desses metabólitos.
Certos defeitos nos fatores hipofisários neuroglandulares que regulam a degradação e síntese dos corpos de cetona, juntamente com os distúrbios no metabolismo de hidrocarbonetos, são a causa da condição de hiperconemia.
Diabetes mellitus e acumulação de corpos cetônicos
Diabetes mellitus (tipo 1) é uma doença endócrina que causa um aumento na produção de corpos de cetona. A produção inadequada de insulina desativa a glicose dos músculos, fígado e tecido adiposo, acumulando -se no sangue.
As células na ausência de glicose começam o processo de gliconeogênese e degradação de gordura e proteínas para restaurar seu metabolismo. Como conseqüência, as concentrações de oxalacetato diminuem e aumentam a oxidação dos lipídios.
Ocorre um acúmulo de acetil-CoA, que na ausência de oxalacetato não pode seguir o caminho do ácido cítrico, causando as altas produções dos corpos de cetona, característica desta doença.
O acúmulo de acetona é detectado por sua presença na urina e no sopro de pessoas que apresentam essa condição, e é de fato um dos sintomas que indicam a manifestação desta doença.
Referências
- Blázquez Ortiz, C. (2004). Cetogênese em astrócitos: caracterização, regulação e possível papel citoprotetor (Dousertação Doutorado, Complutense University of Madri, Serviço de Publicações).
- Devlin, t. M. (1992). Livro de Bioquímica: com correlações clínicas.
- Garrett, r. H., & Grisham, C. M. (2008). Bioquímica. Thomson Brooks/Cole.
- McGry, J. D., Mannaerts, g. P., & Foster, D. C. (1977). Um possível papel para malonil-coA na regulação da oxidação e cetogênese dos ácidos graxos hepáticos. The Journal of Clinical Investigation, 60(1), 265-270.
- Melo, v., Ruiz, v. M., & Cuamatzi, ou. (2007). Bioquímica de processos metabólicos. Reverte.
- Nelson, d. eu., Lehninger, a. eu., & Cox, M. M. (2008). Lehninger Principles of Biochemistry. Macmillan.
- Pertierra, a. G., Gutiérrez, c. V., E outros, C. M. (2000). Fundamentos da bioquímica metabólica. Tébar editorial.
- Voet, d., & Voet, J. G. (2006). Bioquímica. Ed. Pan -American Medical.
- « Café da manhã continental o que é e quais alimentos inclui?
- Propriedades, riscos e usos de peróxido de cálcio (CaO2) »

