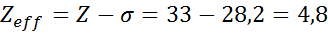Carga nuclear eficaz
- 1743
- 64
- Gilbert Franecki
O que é uma carga nuclear eficaz?
O carga nuclear eficaz (representado como zEff E em alguns casos como z*) É a carga nuclear líquida que um elétron experimenta quando está em um átomo poli -belétrico (ou seja, possui mais de um elétron).
De uma maneira mais precisa, é a carga elétrica que teria o núcleo de um átomo hipotético capaz de atrair seu único elétron com a mesma força com que o núcleo do átomo real atrai o mesmo elétron na presença de todos os outros elétrons.
É uma carga nuclear corrigida que leva em consideração o efeito da presença de outros elétrons em um átomo poliltrônico. Essa carga reduzida explica por que os elétrons mais externos em um átomo polisetrônico estão fracamente ligados ao núcleo do que os elétrons internos.
A carga nuclear eficaz é um conceito de grande importância na química, pois nos permite entender a tendência periódica de muitas propriedades, como raio atômico, raio de íons, eletronegatividade, energias de ionização e mais.
Por que a carga nuclear efetiva existe?
A carga nuclear efetiva surge de dois fenômenos:
- O efeito de blindagem dos elétrons em átomos polietrônicos.
- Repulsão eletrostática entre elétrons porque todos têm a mesma carga elétrica.
Ele efeito de blindagem Consiste em uma espécie de escudo formado pelos elétrons internos de um átomo que cobre o núcleo. Isso faz com que os elétrons mais externos "sintam" uma atração mais baixa por parte do núcleo do que eles sentiriam se os outros elétrons não estivessem presentes.
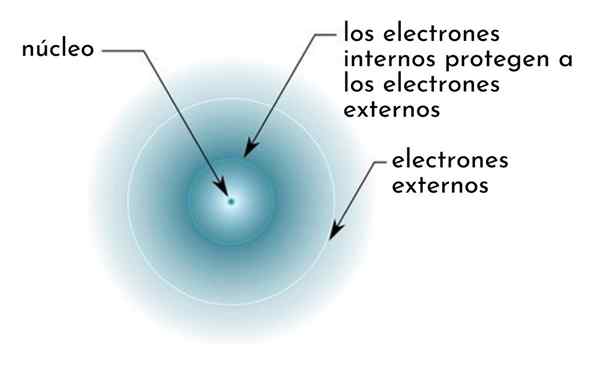 Figura mostra esquematicamente elétrons internos atuando como uma tela que protege os elétrons externos da atração do núcleo
Figura mostra esquematicamente elétrons internos atuando como uma tela que protege os elétrons externos da atração do núcleo Por exemplo, a carga nuclear do átomo de sódio é +11 (seu número atômico é z = 11), mas o único elétron de Valência que possui, na verdade sente a força de atração de uma carga de apenas +2,2.
Pode atendê -lo: benzoato de sódio: estrutura, propriedades, usos e riscosEm outras palavras, a blindagem dos outros 10 elétrons internos faz com que o elétron de Valência do sódio sinta uma força de atração nuclear do quinto do que deveria ser.
Além do efeito de blindagem, o Repulsão entre elétrons (que têm a mesma carga elétrica) também contribui para neutralizar a capacidade do núcleo de atrair elétrons externos. Isto é, essa repulsão também ajuda a reduzir a carga nuclear eficaz.
Características importantes da carga nuclear eficaz
Deve -se notar que o efeito de blindagem responsável por reduzir a carga nuclear eficaz afeta apenas os elétrons que estão no mesmo nível de energia ou nas camadas superiores, mas não nos elétrons mais internos. Além disso, o efeito não é o mesmo para elétrons encontrados em orbitais atômicos S e P do que os encontrados em orbitais D e F.
Por esse motivo, cada conjunto de elétrons de cada camada ou nível de energia parece uma carga nuclear eficaz diferente. Isso tem implicações importantes em relação às propriedades químicas dos diferentes elementos.
Tendência periódica de carga nuclear eficaz
Por um período
Os elétrons localizados no mesmo nível de energia são menos blindados do que os encontrados em níveis mais baixos de energia.
Por causa disso, o efeito de blindagem não aumenta consideravelmente à medida que avançamos durante um período, mas a verdadeira carga nuclear. Por esse motivo, a carga nuclear efetiva aumenta da esquerda para a direita na tabela periódica.
Em todo um grupo
Por outro lado, ao passar de um período para outro no mesmo grupo (ou seja, quando descemos ao longo de um grupo), camadas inteiras de elétrons internos muito protegidos são adicionados. Isso faz com que a carga nuclear eficaz diminua de cima para baixo ou o mesmo, Aumentar de baixo para cima.
Pode servir você: ayaroínaFórmula de carga nuclear eficaz
A carga nuclear eficaz pode ser calculada por meio de uma equação semi -horário muito simples que leva em consideração o valor real da carga nuclear (dada pelo número atômico, z) e um termo chamado de blindagem constante. Este último abrange os efeitos da presença de outros elétrons em um.
A equação é dada por:
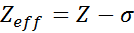
onde z é o número atômico e σ (letra grega sigma) representa a constante de blindagem, que depende da configuração eletrônica.
Regras de Slater
A constante de blindagem pode ser estimada em um sistema conhecido como Regras de Slater. Essas regras permitem calcular a constante de escudo de um elétron, adicionando as contribuições dos outros elétrons à referida constante de blindagem. Essas regras podem ser resumidas da seguinte forma:
- Qualquer elétron que esteja no mesmo nível de energia (nível n0) Fornece uma quantidade de 0,35 para a constante de blindagem, a menos que ambos estejam no nível 1, caso em que fornece 0,30 0,30.
- Cada elétron que está no nível imediatamente anterior (no nível n0-1) em um orbital S ou p, ele traz 0,85; Por outro lado, se estiver em um orbital d ou f, contribui 1.
- Todos os outros elétrons que estão em níveis mais baixos de energia (n0-2, n0-3, etc.), contribua 1 para a constante de blindagem.
Exemplo de cálculo eficaz de carga nuclear
Valencia Electron do átomo de sódio
A configuração eletrônica do átomo de sódio é 1s22s22 p63s1. Ou seja, se queremos calcular a carga nuclear efetiva que o Valencia Electron sente (o Electron 3s1), devemos adicionar as contribuições dos outros 10 elétrons seguindo as regras de Slater.
Pode atendê -lo: óxido de ferro (ii): estrutura, nomenclatura, propriedades, usosComo estamos calculando a constante de blindagem de elétrons 3s1 (n0= 3) e isso está sozinho na camada de Valência, não há outros elétrons no mesmo nível de energia.
O nível imediatamente anterior é n0-1 = 2, onde existem 8 elétrons em orbital s ou p que contribuem 0,85 cada, e não há elétrons em orbitais d ou f.
Finalmente, o único nível inferior a 2 é n = 1, no qual existem apenas 2 elétrons. Tudo isso está resumido na tabela a seguir:
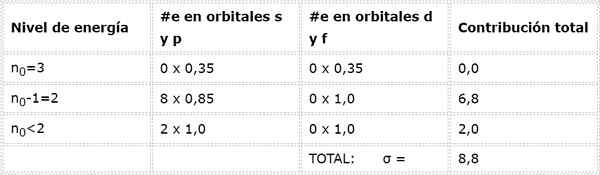
Como pode ser visto, os elétrons internos do sódio fornecem uma constante de escudo de 8,8, de modo que a carga nuclear eficaz que o elétron parece 3s1 é:
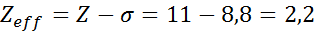
Arsênico Valencia Electrons
A configuração eletrônica de arsênico é 1s22s22 p63s23p63d104s24p3. A camada de Valência é a camada 4 (n0= 4) que possui 5 elétrons: (4s24p3). Nesse caso, cada um desses 5 elétrons sentirá o efeito dos outros 4 que estão na mesma camada e dos outros 28 elétrons internos, como mostrado na tabela:
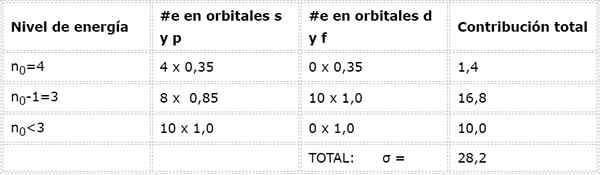
Portanto, a carga nuclear efetiva que os elétrons de Valencia sentem é: