Estrutura de brometo de lítio, propriedades, usos, riscos
- 2540
- 390
- Conrad Schmidt
Ele Brometo de lítio É um sal neutro de um metal alcalino cuja fórmula química é Libr. A fórmula expressa que seu sólido cristalino é composto de íons li+ e br- Em uma proporção de 1: 1. Seus cristais são bege brancos ou leves. É muito solúvel na água e também, é um sal bastante higroscópico.
Esta última propriedade permite seu uso como dessecante em sistemas de ar condicionado e refrigeração. Da mesma forma, o brometo de lítio foi usado desde o início do século XX no tratamento de certos distúrbios da saúde mental, abandonando seu uso devido ao uso inadequado de sal.
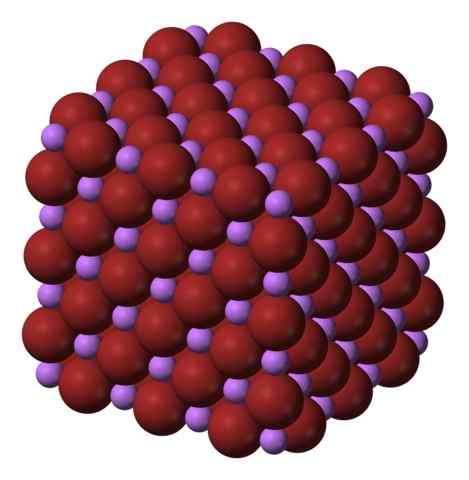
 Estrutura cristalina cúbica do Libr. Fonte: Benjah-BMM27 via Wikipedia.
Estrutura cristalina cúbica do Libr. Fonte: Benjah-BMM27 via Wikipedia. O Libr é produzido pelo tratamento de carbonato de lítio, Li2Co3, com ácido bromidérico. Após o aquecimento do meio, precipita na solução aquosa como um hidrato.
Este sal irrita a pele e os olhos por contato, enquanto produz a irritação dos ductos respiratórios por inalação. A ingestão de sais de lítio pode causar náusea, vômito, diarréia e tontura.
[TOC]
Estrutura de brometo de lítio
A fórmula de Libr deixa claro que a proporção li/Br é igual a 1; Para cada cátion li+ Deve haver um ânion br- de contraparte. Portanto, essa proporção deve ser mantida constante em todos os cantos do cristal de Libr.
Os íons li+ e br- Eles se atraem, reduzindo as repulsões entre cargas iguais, a fim de causar um tipo de jóia de cristal cúbico; Isso é isomórfico para NaCl (imagem superior). Observe que todo o conjunto tem uma geometria cúbica.
Neste cristal, o li+ Eles são menores e têm uma cor violeta leve; enquanto o Br- Eles são mais volumosos e uma cor marrom intensa. Observa -se que cada íon tem seis vizinhos, o mesmo que dizem que eles apresentam uma coordenação octaédrica: Libr6 ou li6Br; No entanto, se a célula unitária for considerada, a proporção li/Br permanece 1.
Pode atendê -lo: estrutura cristalinaEsta é a estrutura cristalina adotada de preferência pelo Libr. No entanto, também pode formar outros tipos de cristais: Wurzita, se cristaliza em baixas temperaturas (-50 ° C) em um substrato; o cúbico centrado no corpo, ou tipo de cSCL, se o sal de vidro cúbico for submetido sob alta pressão.
Hidratos e vidro
O acima é aplicável ao Libr Anhidrous. Este sal é higroscópico e, portanto, pode absorver a umidade do meio ambiente, intercalando moléculas de água em seus próprios cristais. Assim, surgem os hidratos de NH2Ou (n = 1, 2, 3 ..., 10). Para cada hidrato, a estrutura cristalina é diferente.
Por exemplo, estudos cristalográficos determinaram que o Libr · H2Ou adotar uma estrutura do tipo perovskita.
Quando esses hidratos estão em solução aquosa, eles podem transbordar e se vitrificar; Isto é, eles adotam uma estrutura cristalina, mas molecularmente desordenada. Sob tais condições, as pontes de hidrogênio da água se tornam bastante importantes.
Propriedades
Peso molecular
88.845 g/mol.
Aparência
BEIGE sólido ou leve cristalino branco.
Cheiro
Lavatório.
Ponto de fusão
552 ºC (1.026 ºF, 825 K).
Ponto de ebulição
1.256 ºC (2.309 ºF, 1.538 K).
Solubilidade em água
166,7 g/100 ml a 20 ° C. Observe sua alta solubilidade.
Solubilidade em solventes orgânicos
Solúvel em metanol, etanol, éter e acetona. Ligeiramente solúvel em piridina, composto aromático e menos polares do que os anteriores.
Índice de refração (ηd)
1.784.
Capacidade calórica
51,88 J/mol · k.
Entropia molar padrão (Sθ 298)
66,9 J/mol · k.
ponto de ignição
1.265 ºC. É considerado não -inflamável.
Estabilidade
Estábulo. A forma de Anhydra, no entanto, é extremamente higroscópica.
Decomposição
Quando se decompõe por aquecimento, causa óxido de lítio.
Pode atendê -lo: ácido clorogênicoph
Entre pH 6 e 7 em solução aquosa (100 g/L, 20 ºC).
Reatividade
O brometo de lítio não é reativo sob condições ambientais normais. No entanto, você pode experimentar reações intensas com ácidos fortes quando a temperatura aumenta.
Ao se dissolver na água, há um aumento de temperatura, causado por uma entalpia negativa de hidratação.
Produção
Libr ocorre reagindo hidróxido de lítio ou carbonato de lítio com ácido brom -hérico em uma reação de neutralização:
Li2Co3 + HBR => Libr +Co2 + H2QUALQUER
O brometo de lítio é obtido como um hidrato. Para obter uma forma anidro, é necessário aquecer o sal hidratado sob o vácuo.
Nomenclatura
O nome 'brometo de lítio' deriva de ser uma halogenidade metálica, nomeada de acordo com a nomenclatura da ação. Outros nomes, igualmente válidos, mas menos utilizados, são o monobromure de lítio, de acordo com a nomenclatura sistemática; e o brometo lítico (a valência única de +1 para lítio), de acordo com a nomenclatura tradicional.
Formulários
Dessecante
O Libr é um sal higroscópico, formando uma salmoura concentrada capaz de absorver a umidade do ar em uma ampla gama de temperaturas. Esta salmoura é usada como dessecante em sistemas de ar condicionado e refrigeração.
Fibras
É usado para aumentar o volume de lã, cabelos e outras fibras orgânicas.
Adutos farmacêuticos
O Libr forma adutos com alguns compostos farmacêuticos, modulando sua ação. Um aducto é a combinação coordenando duas ou mais moléculas, sem uma alteração estrutural de nenhuma das moléculas unidas.
Sedativo
O brometo de lítio foi usado no início como um sedativo em certos transtornos mentais, pare de usar em 1940. Atualmente, o carbonato de lítio é usado; Mas, de qualquer forma, o lítio é o elemento que exerce a ação terapêutica em ambos os compostos.
Pode atendê -lo: óxido de plumbose (PBO): fórmula, propriedades, riscos e usosO lítio é usado no tratamento do transtorno bipolar, tendo sido útil no controle de episódios maníacos do distúrbio. Pensa -se que o lítio inibe a atividade dos neurotransmissores excitatórios, como dopamina e ácido glutâmico.
Por outro lado, a atividade do sistema inibidor mediado pelo neurotransmissor gama-amino-butírico (GABA) aumenta (GABA). Essas ações podem fazer parte da base da ação terapêutica do lítio.
Riscos
Entre em contato com toxicidade
Irritação e sensibilização cutânea, alergias. Lesões oculares graves ou irritação ocular, no trato respiratório, narinas e garganta.
Ingestão
Os principais sintomas devido à ingestão de brometo de lítio são: distúrbios gastrointestinais, vômitos e náuseas. Outros efeitos adversos na ingestão de sal incluem agitação, espasmos e perda de consciência.
A condição conhecida como "bromismo" pode ocorrer com dose de lítio -bromida superior a 225 mg/dia.
No bromismo, alguns dos seguintes sintomas e sinais podem ocorrer: exacerbação da acne e perda de apetite, tremores, problemas de fala, apatia, fraqueza e agitação maníaca.
Referências
- Formulação química. (2019). Brometo de lítio. Recuperado de: formulação Quimica.com
- David c. Johnson. (10 de julho de 2008). Novo pedido de brometo de lítio. Natureza. doi.org/10.1038/454174A
- Aayushi Jain & r.C. Dixit. (s.F.). Transição de fase estrutural em brometo de lítio: efeito da pressão e temperatura. [PDF]. Recuperado de: ncpcm.em
- Takamuku et al. (1997). Estudos de diffração de raios X em soluções aquosas de lítio e soluções de iodeto de lítio aquoso super-resfriadas. Departamento de Química, Faculdade de Ciências, Universidade de Fukuoka, Nanakuma, Jonan-Ku, Fukuoka 814-80, Japão.
- Centro Nacional de Informações sobre Biotecnologia. (2019). Brometo de lítio. Banco de dados PubChem, CID = 82050. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Wikipedia. (2019). Brometo de lítio. Recuperado de: em.Wikipedia.org
- Sociedade Real de Química. (2019). Brometo de lítio. Chemspider. Recuperado de: chemspider.com
- « Propriedades de alquil halogenuros, obtenção, exemplos
- México nos atos do século 18 e mudanças socioeconômicas »

