Álcoons
- 2579
- 184
- Melvin Mueller
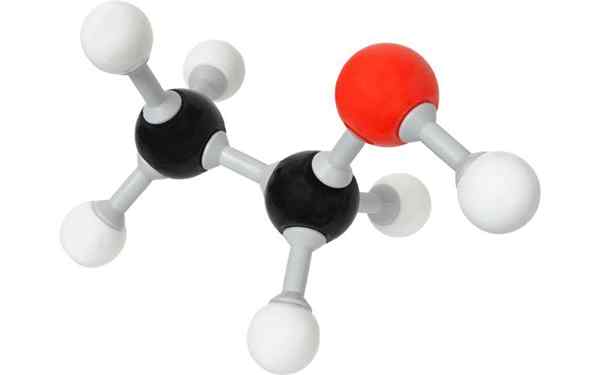
 Molécula de etanol, ou álcool etílico. Com licença
Molécula de etanol, ou álcool etílico. Com licença O que são álcoois?
O Álcoons São compostos orgânicos que são caracterizados por ter um grupo hidroxila (-OH) ligado a um carbono saturado, ou seja, um carbono que está ligado a quatro átomos por ligações simples (sem links duplos ou triplos).
A fórmula genérica para esta vasta e versátil família de compostos é ROH. Para ser considerado como álcool em um sentido estritamente químico, o grupo OH deve ser o mais reativo da estrutura molecular. Isso é importante para afirmar, entre várias moléculas com grupos de OH, qual deles é um álcool.
Um dos álcoois por excelência e o mais conhecido na cultura popular é o álcool etílico, ou etanol, ch3CH2Oh. Dependendo de sua origem natural e, portanto, de seu ambiente químico, suas misturas podem causar um espectro ilimitado de sabores, alguns, que até mostram mudanças positivas no palato com o curso dos anos.
Estrutura dos álcoois
Os álcoois têm uma fórmula general de roh. O grupo OH está ligado ao grupo R Alquilical, cuja estrutura varia de um álcool para outro. A união entre R e OH é um link covalente simples, R-OH.
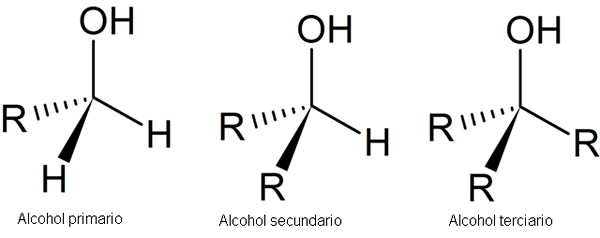
A imagem a seguir mostra três estruturas genéricas para álcoois, considerando que o átomo de carbono está saturado, ou seja, forma quatro links simples.
 Estrutura dos álcoois. Fonte: Secalinum, Wikimedia Commons
Estrutura dos álcoois. Fonte: Secalinum, Wikimedia Commons Como pode ser visto, R pode ser qualquer estrutura carbonatada, desde que não possua substituintes mais reativos do que o grupo OH.
No caso de álcool primário, 1º, o grupo OH está ligado a um carbono primário. Isso é facilmente verificado observando que o átomo no centro do tetraedro esquerdo está ligado a um r e dois h.
O álcool secundário, 2º, é verificado com o carbono do tetraedro do centro agora ligado a dois grupos R e um H.
E, finalmente, você tem álcool terciário, 3º, com carbono ligado a três grupos R.
Caráter anfifile
Dependendo do tipo de carbono ligado ao OH, você tem a classificação de álcoois primários, secundários e terciários. No tetraedro, as diferenças estruturais entre eles já foram detalhadas. Mas todos os álcoois, independentemente de sua estrutura, compartilham algo em comum: o personagem de anfifilo.
Não é necessário abordar uma estrutura para observar, mas é o suficiente com sua fórmula química ROH. O grupo de aluguel é quase totalmente constituído.
Por outro lado, o grupo OH pode formar pontes de hidrogênio com as moléculas de água, portanto, sendo hidrofila, ou seja, apresenta uma afinidade pela água. Então, os álcoois têm um esqueleto hidrofóbico, juntamente com um grupo hidrofílico. Eles são apolares e polares ao mesmo tempo, o que é o mesmo que dizer que são substâncias anfíficas.
Pode servir a você: diferenças entre misturas homogêneas e misturas heterogêneasR-OH
(Hidrofóbico) - (hidrofílico)
Como será explicado na próxima seção, o caráter anfifile dos álcoois define algumas de suas propriedades químicas.
Estrutura de r
O grupo Renta R pode ter qualquer estrutura e, no entanto, é importante, pois permite que os álcoois sejam classificados.
Por exemplo, R pode ser uma cadeia aberta, como é o caso de etanol ou propanol, ramificado, como álcool t-butílico (CH3)2Chch2Oh, pode ser cíclico, como no caso do ciclohexanol, ou pode ter um anel aromático, como no álcool benzílico (C6H5) CH2Oh, ou em 3-fenilpropanol (c6H5) CH2CH2CH2Oh.
A cadeia R pode até ter substituintes como halogênios ou ligações duplas, como para álcoois 2 células e 2-bunt-1-ol (CH3CH2= Chch2OH).
Considerando a estrutura de r, a classificação dos álcoois se torna complexa. Portanto, a classificação baseada em sua estrutura (1ª, 2ª e 3ª Álcoois) é mais fácil, mas menos específica, embora seja suficiente explicar a reatividade dos álcoois.
Propriedades físicas e químicas
- Ponto de ebulição: Uma das principais propriedades dos álcoois é que eles estão associados através de pontes de hidrogênio. Graças a isso, os álcoois geralmente são líquidos com altos pontos de ebulição.
- Capacidade de solvente: Em casas, é muito comum recorrer ao uso de álcool isopropílico para remover uma mancha difícil de remover em uma superfície. Essa capacidade de solvente, muito útil para síntese química, é devido ao seu caráter de anfropifil, anteriormente explicado. As gorduras são caracterizadas por serem hidrofóbicas: é por isso que é difícil removê -las com água. No entanto, diferentemente da água, os álcoois têm uma parte hidrofóbica em sua estrutura. Assim, seu grupo Renta r interage com as gorduras, enquanto o grupo OH forma pontes de hidrogênio com água, ajudando a movê -las.
- Anfoterismo: Os álcoois podem reagir como ácidos e bases, ou seja, são substâncias anfotentas. Isso é representado com as duas equações químicas a seguir:
Roh + h+ => Roh2+
Roh + oh- => Ro-
O ro- É a fórmula geral do que é conhecido como alcoxide.
Nomenclatura
Existem duas maneiras de nomear álcoois, cuja complexidade dependerá de sua estrutura.
Nome comum
Os álcoois podem ser chamados para seus nomes comuns. Para fazer isso, o nome do grupo R deve ser conhecido, ao qual o final -ico é adicionado e é precedido pela palavra 'álcool'. Por exemplo, Cho3CH2CH2Oh é álcool propylico.
Pode atendê -lo: sistema heterogêneoOutros exemplos são:
- CH3OH: álcool metílico.
- (CH3)2Chch2OH: Álcool isobutil.
- (CH3)3COH: Álcool terc-boutyl.
IUPAC System
Quanto a nomes comuns, você deve começar identificando R. A vantagem deste sistema é que ele é muito mais preciso do que o outro.
A, como é um esqueleto de carbono, pode ter ramificações ou várias correntes. A cadeia mais longa, isto é, com mais átomos de carbono, é a qual o nome do álcool será concedido.
O nome da cadeia mais longa é adicionado ao nome do alcano, o término 'l' é adicionado. É por isso que Cho3CH2Oh é chamado de etanol (Cho3CH2- + OH).
Geralmente, oh deve ter a menor enumeração possível. Por exemplo, o brch2CH2CH2(Oh) Cho3 É chamado 4-bromo-2-butanol, e não 1-bromo-3-butanol.
Síntese
Hidratação de alcenos
O processo de estrasagem de petróleo produz uma mistura de quatro ou cinco átomos de carbono, que podem se separar facilmente.
Esses alcenos podem se tornar álcoois pela adição direta de água ou pela reação do alceno com ácido sulfúrico, seguido pela adição da água que o ácido divide, originando o álcool.
Processo OXO
Na presença de um catalisador adequado, os alcenos reagem com carbono e monóxido de hidrogênio para gerar aldeídos. Os aldeídos podem ser facilmente reduzidos a álcoois por uma reação de hidrogenação catalítica.
Geralmente, há uma sincronização do processo OXO que a redução de aldeídos é quase simultânea com sua formação.
O catalisador mais usado é o decobalto octocarbonil, obtido pela reação entre cobalto e monóxido de carbono.
Fermentação de carboidratos
A fermentação de carboidratos para leveduras ainda é de grande importância na produção de etanol e outros álcoois. Os açúcares vêm de cana de açúcar ou amido obtido de diferentes grãos. Por esse motivo, o etanol também é chamado de "álcool de grãos"
Formulários
Bebidas
- Embora não seja a principal função dos álcoois, a presença de etanol em algumas das bebidas é um dos conhecimentos mais populares. Assim, etanol, produto da fermentação de cana -de -açúcar, uvas, maçã, etc., Está presente em inúmeras bebidas de consumo social.
Matéria -prima química
- O metanol é usado na produção de formaldeído, através de sua oxidação catalítica. O formaldeído é usado na fabricação de plásticos, pinturas, têxteis, explosivos, etc.
- Butanol é usado na produção de butanoat butano, um éster usado como um sabor na indústria de alimentos e confeitaria.
- O álcool allyic é usado na produção de ésteres, incluindo o ftalato de Dialilo e o isftalato de dialilo, que servem como monômeros.
- O fenol é usado na produção de resinas, fabricação de nylon, desodorantes, cosméticos etc.
- Os álcoois da cadeia linear de 11 a 16 átomos de carbono são usados como intermediários para obter plastificantes. Por exemplo, cloreto de polivinil.
- Os álcoois gordurosos de tão chamados são usados como intermediários na síntese de detergentes.
Solventes
- O metanol é usado como solvente de tinta, bem como 1-butanol e isobutílico álcool.
- O álcool etílico é usado como um solvente de muitos compostos insolúveis na água, usando como solvente em pinturas, cosméticos etc.
- Os álcoois gordurosos são usados como solventes na indústria têxtil, em corantes, em detergentes e em pinturas. O isobutanol é usado como solvente em material de revestimento, pinturas e adesivos.
Combustíveis
- O metanol é usado como combustível em motores a gasolina internos e aditivos para melhorar a combustão.
- O álcool etílico é usado em combinação com combustíveis fósseis em veículos a motor. Para esse fim, extensas regiões do Brasil destinam -se ao cultivo de cana -de -açúcar para produção de álcool etílico. Este álcool tem a vantagem de produzir em sua combustão apenas dióxido de carbono. Quando o álcool etílico é queimado, produz uma chama limpa e sem fumaça, e é por isso que é usado como combustível nas cozinhas de campanha.
- O álcool gelificado é produzido por combinação de metanol ou etanol com acetato de cálcio. Este álcool é usado como uma fonte de calor em fogões de campanha e, à medida que derrama, é mais seguro que os álcoois líquidos.
- O biobutanol chamado é usado como combustível de transporte, bem como álcool isopropílico, embora seu uso não seja recomendado.
Anti -sépticos
- O álcool isopropílico de concentração de 70% é usado como um anti -séptico externo para a eliminação de germes e retardo de seu crescimento, assim como o álcool etílico.
Outros usos
- Ciclohexanol e metilciclohexanol são usados no acabamento têxtil, móveis processados e chitamanchas.
Exemplos de álcoois e suas fórmulas
- Metanol (cap3OH).
- 1-propanol (c3H7OH).
- Etanol (c2H5OH).
- Isobutanol (c4H9OH).
- Isopropanol (c3H8QUALQUER).
- Álcool Allilic (C3H6QUALQUER).
- Álcool benzílico (C7H8QUALQUER).
- Térmico (c₄h₁₀o).
- Pentenol (c5HonzeOH).
- 2-butanol (cap3-CH2-Choh-ch3).
- Fenol (c6H6QUALQUER).
- 2-propanol (cap3-Choh-ch3).
- Isodecanol (c10H21OH).
- Álcool Cetil (C16H3. 4QUALQUER).
- Álcool propargílico (c3H4QUALQUER).
- Álcool tetra -hidrofurilico (C5H10QUALQUER2).
- Ciclohexanol (c6H12QUALQUER).
- 2-clorotanol (c2H5Clo).
- Heptanol (c7H16QUALQUER).
- HEXANOL (C₆H₁₄O).
Referências
- Quimica Organica. Mc Graw Hill.
- Álcoons. Recuperado de Colapret.cm.Utexas.Edu.

