Estrutura de acetato de potássio, propriedades, usos, obtenção
- 2465
- 681
- Ernesto Bruen
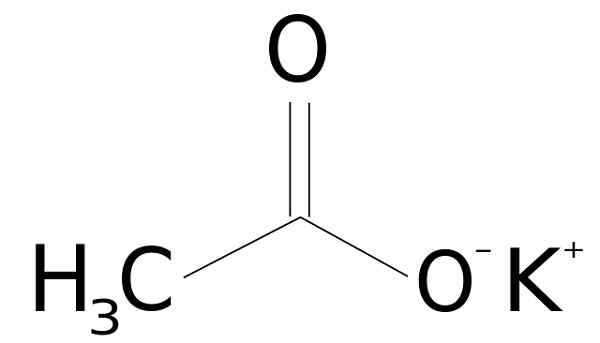
Ele acetato de potássio É um composto orgânico formado por um on potássio k+ e um acetato de íons CHO3COO-. Sua fórmula química é Cho3Cozinhe, ou KCH3COO, ou também C2H3Ko2. É um sólido cristalino incolor ou branco, muito solúvel em água.
É usado para regular a acidez de certos alimentos processados industrialmente. Devido à sua grande afinidade com a água, é usada em laboratórios ou em determinados processos para absorver a água de outros compostos, como desidratar o álcool.
 Acetato de potássio KCH3CO serve para regular a acidez de alguns alimentos processados. Autor: Ritae. Fonte: Pixabay.
Acetato de potássio KCH3CO serve para regular a acidez de alguns alimentos processados. Autor: Ritae. Fonte: Pixabay. O acetato de potássio participa de algumas reações químicas, como seu acelerador e na síntese de compostos orgânicos. Também permite aumentar a formação de anticorpos (substâncias naturais que combatem infecções) em métodos industriais para produzi -los.
Suas propriedades a temperaturas muito baixas tornam um bom candidato a ser usado em misturas para derreter o gelo em estradas de concreto em climas muito frios. De acordo com fontes consultadas, também é usado em equipamentos para combater incêndios e conjuntos para observar células em microscópios.
[TOC]
Estrutura
O acetato de potássio é formado por um cátion de potássio k+ e um acetato de ânion Cho3COO-. Este último é a base conjugada de ácido acético CH3COOH. O acetato Cho3COO- é composto de um metil -ch3 junto com um carboxilato -COO-.
A união entre os dois íons é eletrostática ou iônica, ou seja, a união entre um íon positivo e um negativo.
 Estrutura de acetato de potássio CH3Cozinhar. Sssilver [domínio público]. Fonte: Wikimedia Commons.
Estrutura de acetato de potássio CH3Cozinhar. Sssilver [domínio público]. Fonte: Wikimedia Commons. Nomenclatura
- Acetato de potássio
- Etanoato de potássio
- Sal de potássio ácido acético
- ACOK
- Koac
Propriedades
Estado físico
Branco sólido ou cristalino incolor.
Peso molecular
98,14 g/mol
Ponto de fusão
292 ºC
Densidade
1,6 g/cm3
Solubilidade
Muito solúvel em água: 256 g/100 ml a 20 ° C.
ph
Uma solução aquosa de 5% de acetato de potássio tem um pH de 7,5-9,0.
Outras propriedades
Às vezes tem um cheiro fraco de vinagre. Em solução a 10% não atacam alumínio à temperatura ambiente, mas a 60-70 ° C o metal escurece e sofre mordidas.
Em concentrações de 20% ou mais, o ataque superficial ao alumínio ocorre a qualquer temperatura.
Pode servir você: hidraceO acetato de potássio (ACOK) é altamente solúvel em água. Tem um hidrato: o kch3COO.1.5h2Ou, que é o sólido que é obtido cristalizando -o a partir das soluções ACOK aquosas.
Comportamento ao aquecer
Se o acetato de potássio (ACOK) (KCH (KCH) for submetido ao aquecimento (KCH3COO.1.5h2O) Ao atingir 40 ° C, a água de hidratação começa a perder.
Kch3COO.1.5h2O → KCH3COO + 1,5h2Ou ↑
Se o acetato de potássio anidro for aquecido (sem água: kch3COO), ao atingir 340 ° C, começa a decompor a formação de carbonato de potássio k2Co3 De acordo com a seguinte reação:
2 kch3COO + 4 O2 → k2Co3 + 3 h2O + 3 CO2↑
Obtenção
Pode ser preparado pela ação do hidróxido de koh potássio em vários compostos, como Cho Acid3COOH, anidrido acético (CH3CO)2O e acetato de amônio3Poonh4.
KOH +CH3COOH → CH3Cozinhe + h2QUALQUER
Também pode ser obtido reagindo carbonato de potássio k2Co3 Ó KHCO Bicarbonato de potássio3 Com ácido acético CH3COOH.
KHCO3 + CH3COOH → CH3Cozinhe +h2Ou + co2↑
O acetato de potássio pode ser cristalizado a partir de uma solução aquosa para obtê -lo com alta pureza.
Formulários
Em várias aplicações
O acetato de potássio é usado na indústria de alimentos processada como regulador de acidez. É usado como dessecante em métodos químicos para medir a permeabilidade ao vapor de água de alguns tecidos.
Serve como um agente desidratante do etanol na produção desse álcool baseado em lignocelulose, um material derivado da madeira.
É usado para produzir antibióticos e é amplamente utilizado em equipamentos de combate de incêndio.
Na indústria de polímeros
É usado para reciclar poliuretanos porque serve para catalisar ou acelerar as reações de hidrólise e glicólise de tais polímeros para se tornarem álcoois e aminas.
Também é usado na produção de resinas de silicone orgânico.
Em laboratórios de pesquisa científica e médica
O acetato de potássio de alta pureza é usado em laboratórios como reagente de química analítica. Também para realizar pesquisas médicas.
Pode atendê -lo: neon: história, propriedades, estrutura, riscos, usosNos laboratórios de histopatologia, ele serve para garantir um meio de pH neutro em conjuntos de microscópio.
 O acetato de potássio tem vários usos em laboratórios de pesquisa química e médica. Autor: Michal Jarmoluk. Fonte: Pixabay.
O acetato de potássio tem vários usos em laboratórios de pesquisa química e médica. Autor: Michal Jarmoluk. Fonte: Pixabay. É usado para a síntese de compostos orgânicos heterocíclicos, que são compostos com ciclos de tamanho diferente.
Certos microeletrodos que servem para estudar as propriedades elétricas das células são preenchidas com uma solução concentrada de acetato de potássio.
Na produção industrial de anticorpos
O acetato de potássio serve a produção em grande escala de anticorpos monoclonais (que são aqueles que vêm da mesma célula -tronco) em culturas de células. Permite estimular a síntese ou a formação de anticorpos.
Anticorpos são substâncias produzidas por algumas células sanguíneas para combater infecções por vírus ou bactérias.
 Imagem de anticorpos artísticos. Acetato de sódio KCH3O CO serve na produção de anticorpos em grandes quantidades. Blitzkrieg1982 [CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons.Embora o acetato de potássio (ACOK) iniba ou retarde o crescimento celular e diminua a densidade celular, a produtividade de anticorpos para cada célula aumenta.
Imagem de anticorpos artísticos. Acetato de sódio KCH3O CO serve na produção de anticorpos em grandes quantidades. Blitzkrieg1982 [CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons.Embora o acetato de potássio (ACOK) iniba ou retarde o crescimento celular e diminua a densidade celular, a produtividade de anticorpos para cada célula aumenta.
 Ataque de anticorpos atraindo algumas bactérias. SA1590 [CC BY-S (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons.
Ataque de anticorpos atraindo algumas bactérias. SA1590 [CC BY-S (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons. Em misturas antihielo
O acetato de potássio tem sido usado em misturas antihielo (tradução para o inglês Anti-gelo) para usá -los para derreter a estrada e cimento pavimentos e, assim, permitir o uso seguro destes.
 Durante a estação de inverno, as estradas estão cheias de neve e gelo. O acetato de potássio pode ser útil nesses casos. Autor: s. Hermann & F. Richter. Fonte: Pixabay.
Durante a estação de inverno, as estradas estão cheias de neve e gelo. O acetato de potássio pode ser útil nesses casos. Autor: s. Hermann & F. Richter. Fonte: Pixabay. A seleção de acetato de potássio (ACOK) para esta aplicação é devida a uma solução aquosa de 50% por peso ACOK é um euttic e possui um ponto de fusão de -62 ° C. Isso significa que, mesmo em temperaturas tão baixas quanto -62 ° C, a solução permanece derretida.
Um euttico é uma mistura homogênea de componentes que tem o menor ponto de fusão de todas as misturas possíveis, incluindo componentes puros.
Como funciona como um antihielo
O acetato de potássio (ACOK) tem uma capacidade muito boa de derreter o gelo.
A -5 ° C é capaz de derreter 11,5 kg de gelo para cada kg de ACOK. Essa propriedade diminui diminuindo a temperatura, mas mesmo para -50 ° C tem a capacidade de derreter 1,3 kg de gelo para cada kg de ACOH.
Pode servir a você: sólidos cristalinos: estrutura, propriedades, tipos, exemplosA -5 ° C Essa capacidade é comparável à do cloreto de sódio ou sal de mesa (NaCl), enquanto de -30 ° C distante.
 O acetato de potássio permite derreter o gelo em estradas congeladas. Autor: Markus Sch. Fonte: Pixabay.
O acetato de potássio permite derreter o gelo em estradas congeladas. Autor: Markus Sch. Fonte: Pixabay. No entanto, nos testes realizados com o ACOK juntamente com outros compostos, foi observado um certo grau de corrosão das superfícies de cimento, por isso foi proposto adicionar misturas anticorrosivas às misturas anti -hielo.
Por outro lado, a mistura de acetato de potássio (CH3Cozinheiro) com a formação de potássio (HCOOK) é um excelente antihielo e não requer anticorrosivo.
Referências
- Baker, f.J. et al. (1976). Procedimentos de coloração. Montantes aquosos. Em Introdução à Tecnologia do Laboratório Médico (Quinta Edição). Recuperado de cientedirect.com.
- Hassan, a.PARA. et al. (2018). Inzoles: síntese e heterociclização formadora de títulos. Em avanços na química heterocíclica. Recuperado de cientedirect.com.
- OU.S. Biblioteca Nacional de Medicina. (2019). Acetato de potássio. Recuperado de PubChem.NCBI.Nlm.NIH.Gov.
- Das, a. e alagirusamy, r. (2010). Transmissão de umidade. Método de copo invertido. Em ciência em conforto de roupas. Recuperado de cientedirect.com.
- Vargel, c. (2004). Ácidos carboxílicos e seus derivados. Acetatos. Em corrosão do alumínio. Recuperado de cientedirect.com.
- Cuevas, j. (2014). Técnicas de registro eletrofisiológico. Técnicas de gravação intracelular. Na modulação de referência em ciências biomédicas. Recuperado de cientedirect.com.
- Fink, j.K. (2018). Poli (uretano) s. Reciclando. Solvolise. Em polímeros reativos: fundamental e aplicações (terceira edição). Recuperado de cientedirect.com.
- Fong, w. et al. (1997). Otimização da produção de anticorpos monoclonais: efeitos combinados de acetato de potássio e perfusão em um tanque agitado biorreator. Citotecnologia 24: 47-54. Link recuperado.Springer.com.
- Danilov, v.P. et al. (2012). Reagentes anti-gigantes de baixa temperatura em sistemas de sal aquosos contendo acetatos e formatos. Fundamentos teóricos de engenharia química, 2012, vol 46, não. 5, pp. 528-535. Link recuperado.Springer.com.
- Falsoev, a.PARA.et al. (2012). Pesquisa e desenvolvimento de método para acetato de potássio de alta pureza. Journal of Applied Chemistry, 2012, vol. 85, não.12, pp. 1807-1813. Link recuperado.Springer.com.
- « Unidades de choque magnético, fórmulas, cálculo, exemplos
- Características Dispositivos de entrada, quais são o uso, tipos, exemplos »

