Sistemas de teoria de colisão, energia, exemplos
- 3126
- 180
- Shawn Leffler
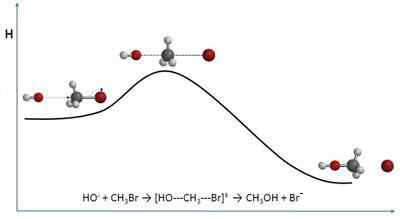
O teoria da colisão Explique as velocidades das reações químicas de uma perspectiva meramente molecular. Portanto, está intimamente próximo da cinética química. Em vez de abordar a velocidade em termos de concentrações, o faz com base nas frequências de colisão.
Ao falar sobre colisões, a imagem de algumas bolas de bilhar pode vir à mente impactando uma na outra na mesa. No entanto, moléculas, embora essa teoria assuma que suas formas são esféricas, não se comportam da mesma forma. As colisões moleculares diferem de várias maneiras, tanto espaciais quanto energia.

Essa teoria, embora possa ser matematicamente um pouco complexa e mostrar variações consideráveis em relação aos resultados experimentais, oferece uma imagem de interpretações visíveis e sem aspectos abstratos.
Embora seja aplicado a sistemas gasosos ou soluções muito diluídas, seus princípios podem se estender a qualquer reação e meio físico.
[TOC]
Condições para reações ocorrem
De acordo com a teoria das colisões, existem três condições para que ocorram reações:
- Espécies químicas (íons, moléculas, radicais, etc.) Eles devem colidir com eficiência.
- Eles devem carregar energia suficiente para o colapso de seus links.
- Além disso, a orientação de impacto deve ser muito específica.
Colisões moleculares
 Como no boliche, as reações só ocorrem quando colisões eficientes ocorrem em termos de energia e orientação
Como no boliche, as reações só ocorrem quando colisões eficientes ocorrem em termos de energia e orientação Colisões moleculares compartilham algo em comum com macroscópico: elas ocorrem predominantemente entre duas espécies ou corpos. Duas bolas de bilhar colidem entre si, bem como uma bola de futebol contra uma parede, ou dois projéteis no meio do ar. Isto é, colisões em relação à química e suas reações tendem a ser do tipo bimolecular.
Pode atendê -lo: ionização em física e química: conceito, processo e exemplosAs moléculas não estão paradas, mas elas se movem e giram pelo espaço que os cercam. Ao fazer isso, supõe -se que eles desenhem um tipo de círculo chamado seção transversal, na qual há a probabilidade de que outra molécula de Colison. Da mesma forma, a teoria considera que as moléculas são esféricas para simplificar modelos matemáticos.
Duas moléculas, hipoteticamente esféricas, podem colidir sem nenhum problema, mesmo que não haja reação química. Mas isso não acontece da mesma maneira quando se trata de três, quatro ou mais moléculas.
Quanto mais espécies elas devem colidir para originar um produto, mais improvável o fenômeno se torna. Isso é explicado visualmente tentando que três bolas ou projéteis colidem ao mesmo tempo juntos. Portanto, colisões bimoleculares são de longe as mais comuns.
Sistemas
A teoria da colisão é válida apenas para sistemas de software ou fases. Isso ocorre porque os gases mostram comportamento que pode ser bem descrito por sua cinética.
Para fases líquidas ou soluções muito diluídas, as espécies reativas são embrulhadas em uma gaiola de moléculas de solvente, com as quais também colidem. Isso modifica o panorama, pois as reações não apenas dependem das frequências das colisões, mas também da difusão das moléculas reagentes através do meio.
Energias de colisão
As moléculas podem colidir lenta ou muito rapidamente. Isso depende do tamanho de sua energia, que por sua vez varia significativamente com a temperatura. Quanto mais forte a colisão, a probabilidade de haver uma reação química aumentará, pois essa energia pode quebrar os links necessários para formar novos.
Pode atendê -lo: monômerosEsta energia é conhecida como ativação ePARA, E é característico para qualquer reação química. Quando a temperatura aumenta, a média das moléculas é capaz de corresponder ou exceder ePARA, Portanto, o número de colisões eficazes e, portanto, os produtos formados, aumentam.
Na presença de um catalisador ePARA diminui, pois fornece superfícies e eletrônicos significa que beneficiam colisões. O resultado: a taxa de reação aumenta, sem aumentar a temperatura ou adicionar outros reagentes.
Fator estérico
As espécies químicas colidem efetivamente para reagir, prevendo essa teoria qual será a velocidade de suas reações. No entanto, experimentos mostraram que quanto mais complexas forem as estruturas dos reagentes, maiores os desvios ou diferenças entre as velocidades teóricas e experimentais.
Isso ocorre porque as moléculas estão longe de ser esféricas, mas espacialmente têm todos os tipos de geometrias. É aqui que o fator estérico entra, ρ, Com o qual procura corrigir as velocidades da reação, para que as previsões da teoria com os resultados experimentais sejam melhores.
Exemplos de reações
Reação bimolecular
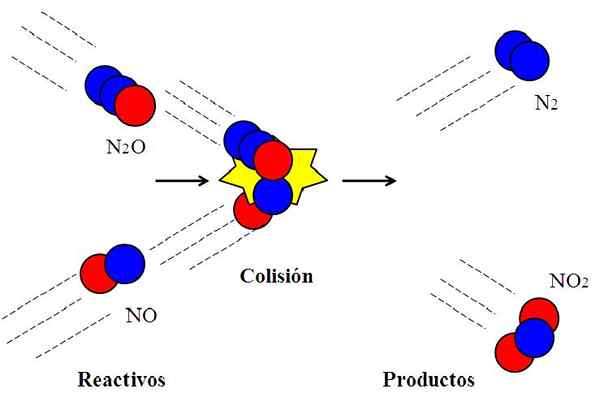 Colisão eficaz entre óxidos de nitrogênio. Fonte: Gabriel Bolívar.
Colisão eficaz entre óxidos de nitrogênio. Fonte: Gabriel Bolívar. A seguinte reação:
N2O + NO → N2 + NÃO2
É comumente usado para explicar o que a orientação eficaz significa em colisões moleculares.
A molécula n2Ou, óxido de dyitrogênio, ele não reagirá com o óxido nítrico não, a menos que durante a colisão o átomo de oxigênio (círculo vermelho) do N2Ou choque diretamente com o átomo de nitrogênio (círculo azul) do não. Somente assim os produtos n originarão2 e não2; Caso contrário, n moléculas2O e eles não vão saltar sem reagir.
Pode servir a você: Estado gasoso: características, direito geral, exemplosEste é um exemplo de uma colisão bimolecular para uma reação bimolecular elementar. Mesmo quando os reagentes têm energia suficiente para quebrar os links, se a orientação não for apropriada, não haverá reação química.
Reação unimolecular
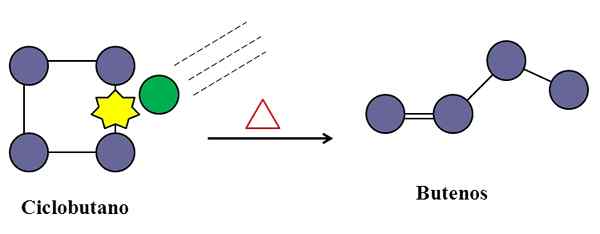 Colisões também são indispensáveis para a isomerização de ciclobutano. Fonte: Gabriel Bolívar.
Colisões também são indispensáveis para a isomerização de ciclobutano. Fonte: Gabriel Bolívar. Em uma reação elementar unimolecular, as colisões moleculares também podem intervir, mesmo que seja apenas uma espécie que sofre a transformação ou quebra de seus links.
Considere, por exemplo, a isomerização do ciclobutano para dar origem a uma mistura de butanos. Quando a temperatura aumenta, as moléculas de ciclobutano vibram em frequências mais altas e colidem com maior força. Os produtos, no entanto, mostram que duas moléculas de ciclobutano não reagem entre si porque, caso contrário, produziriam um composto com oito carbonos.
No meio, pode haver impurezas (círculo verde), que também colidem com o ciclobutano, especificamente em qualquer um de seus links C-C. Estes podem ser gases nobres, ou não moléculas muito reativas, como nitrogênio.
Chegará um momento em que a impureza colidirá com energia suficiente para quebrar um dos links C-C do ciclobutano. E então, sua molécula procurará reorganizar e originar um buuteno, reconhecível por sua ligação dupla e sua estrutura de cadeia linear.
Referências
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- Glasstone. (1970). Tratado de Physicoquímica. Aguilar s. PARA. das edições, Juan Bravo, 38, Madri (Espanha).
- Walter J. Moore. (1962). Química Física. (Quarta edição). Longmans.
- Wikipedia. (2020). Teoria da colisão. Recuperado de: em.Wikipedia.org
- Os editores da Enyclopaedia Britannica. (2020). Teoria da colisão. Enciclopédia Britannica. Recuperado de: Britannica.com
- Clark Jim. (2018). A teoria do colisão das taxas de reação. Recuperado de: Chemguide.co.Reino Unido
- Lawson p. & Inferior s. (18 de maio de 2020). A teoria do colisão. Química Librettexts. Recuperado de: química.Librettexts.org
- « Características de texto didáticas, estrutura, tipos e exemplos
- Países e características e características da América ou Antilhas »

