Características de serina, funções, metabolismo, comida
- 2028
- 22
- Alfred Kub
O Serine É um dos 22 aminoácidos básicos, embora isso não seja classificado como um aminoácido essencial para o homem e outros animais, pois é sintetizado pelo corpo humano.
De acordo com a nomenclatura de três letras, a serina é descrita na literatura como sendo (s no código de letra única). Este aminoácido participa de um grande número de rotas metabólicas e possui características polares, mas não tem carga em pH neutro.
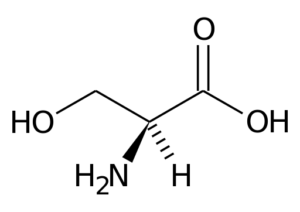 Representação da série do aminoácido serina (fonte: PageZero.Wikipedia [domínio público] via Wikimedia Commons)
Representação da série do aminoácido serina (fonte: PageZero.Wikipedia [domínio público] via Wikimedia Commons) Muitas enzimas importantes para células têm bastante.
A serina, entre muitas de suas funções, participa como precursora e molécula de andaimes na biossíntese de outros aminoácidos, como glicina e cisteína, e faz parte da estrutura dos esfingolipídios presentes nas membranas celulares em membranas celulares.
A taxa de síntese de serina varia em cada órgão e, além disso, muda de acordo com o estágio de desenvolvimento em que o indivíduo é.
Os cientistas propuseram que as concentrações de L-Serina no tecido cerebral aumentam com a idade, uma vez que a permeabilidade da barreira das células sanguíneas diminui no cérebro do adulto, sendo capaz de causar distúrbios cerebrais graves.
Sabe-se que a L-Serina é vital para a biossíntese de neurotransmissores, fosfolipídios e outras macromoléculas complexas, uma vez que fornece os precursores para essas múltiplas vias metabólicas.
Vários estudos demonstraram que o fornecimento de suplementos ou concentrados de L-Serina a certos tipos de pacientes melhoram a homeostase da glicose, a função mitocondrial e reduzem a morte neuronal.
[TOC]
Características e estrutura
Todos os aminoácidos têm como estrutura básica um grupo carboxila e um grupo amino ligado ao mesmo átomo de carbono; No entanto, eles diferem entre si por suas cadeias laterais, conhecidas como grupos R, que podem variar em seu tamanho, estrutura e até em sua carga elétrica
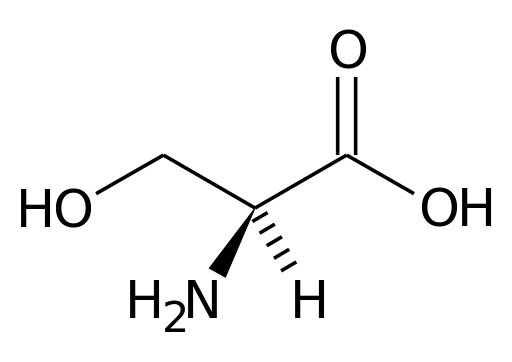
A serina contém três átomos de carbono: um carbono central unido, por um lado, para um grupo carboxil (COOH) e, por outro, um grupo amino (NH3+). As outras duas ligações de carbono central são ocupadas por um átomo de hidrogênio e um grupo CH2OH (Grupo R), característico da serina.
O carbono central ao qual os grupos amino e carboxila dos aminoácidos são conhecidos como α carbono. Os outros átomos de carbono dos grupos R são designados com as letras do alfabeto grego.
No caso da serina, por exemplo, o único átomo de carbono em seu grupo R, que está ligado ao grupo OH, é conhecido como carbono γ.
Pode servir a você: fosfatidilserina: estrutura, síntese, funções, localizaçãoClassificação
A serina é classificada dentro do grupo de aminoácidos polares sem carga. Os membros deste grupo são aminoácidos muito solúveis na água, ou seja, são compostos hidrofílicos. Na serina e na treonina, a hidrofilicidade se deve à sua capacidade de formar pontes de hidrogênio com água através de seus grupos hidroxila (OH).
Dentro do grupo de aminoácidos polares sem carga, cisteína, asparagina e glutamina também são agrupadas. Tudo isso tem um grupo polar em sua cadeia R, no entanto, esse grupo não é ionizável e o pH próximo à neutralidade cancelou suas cobranças, produzindo um composto na forma de "Zwitterion".
Estereoquímica
A assimetria geral dos aminoácidos torna a estereoquímica desses compostos de importância vital nas rotas metabólicas em que participam. No caso da serina, isso pode ser encontrado como D-O L-Serine, sendo o último sintetizado exclusivamente pelas células do sistema nervoso conhecido como astrócitos.
Os carbonos α dos aminoácidos são carbonos quirais, pois têm quatro substituintes unidos diferentes, o que gera que existem pelo menos dois estereoisômeros distinguíveis para cada aminoácido.
Um estereoisômer é uma imagem espelhada de uma molécula, ou seja, você não pode se sobrepor um no outro. As soluções desses aminoácidos giram o plano de luz polarizado em direções opostas em direções opostas são indicadas com a letra que experimentalmente.
O L-Serina que é sintetizado em células do sistema nervoso serve como substrato para sintetizar a glicina ou D-serina. O D-Serin é um dos elementos mais importantes para a troca de vesículas entre os neurônios; portanto, alguns autores propõem que ambas as isoformas de serina sejam, na realidade, aminoácidos essenciais para neurônios para neurônios.
Funções
O grupo OH da serina em sua cadeia r R torna um bom nucleófilo, por isso é essencial para a atividade de muitas enzimas com serina em seus sites ativos. Serina é um dos substratos necessários para a síntese de NADPH e nucleotídeos glutatiônicos.
L-Series é indispensável para o desenvolvimento e o funcionamento adequado do sistema nervoso central. Estudos mostraram que o suprimento exógeno de L-Serina em doses baixas para os neurônios do hipocampo e as células Purkinje Em vitro, Melhora sua sobrevivência.
Vários estudos de células cancerígenas e linfócitos descobriram que as unidades de carbono dependentes de serina são necessárias para a produção excessiva de nucleotídeos, bem como a subsequente proliferação de células cancerígenas.
Pode atendê -lo: microbiota: composição, funções e onde estáA selenocisteína faz parte dos 22 aminoácidos básicos e é obtida apenas como um derivado da serina. Este aminoácido foi observado apenas em algumas proteínas, contém selênio em vez de enxofre ligado à cisteína e é sintetizado com base em uma serina esterificada.
Biossíntese
A serina é um aminoácido não essencial, pois é sintetizado pelo corpo humano. No entanto, isso pode ser assimilado da dieta de diferentes fontes, como proteínas e fosfolipídios, principalmente.
A serina é sintetizada em sua forma pela conversão de uma molécula de glicina, uma reação mediada por uma enzima hidroximetil-transferase.
Sabe-se que o principal local de síntese de L-serina está em astrócitos e não em neurônios. São essas células, a síntese ocorre por uma rota de fosforilação na qual o 3-fosfoglicerado participa, um intermediário glicolítico.
Três enzimas agem nesta rota: a 3-fosfogliceridade desidrogenase, fosfoserina-transferase e fosfoserina-fosfatase.
Outros órgãos importantes no que diz respeito à síntese de serina são o fígado, rins, testículos e baço. As enzimas que sintetizam serina.
Uma das primeiras rotas de síntese da serina conhecida foi a via catabólica envolvida na gliconeogênese, onde a L-Serina é obtida como um metabolito secundário. No entanto, a contribuição desta rota para a produção de corpora serina é baixa.
Metabolismo
Atualmente, sabe-se que a serina pode ser obtida do metabolismo de carboidratos no fígado, onde o ácido D-glicérico, o ácido 3-fosfoglicérico e o ácido 3-fosfo-hidroxipírico é produzido. Graças a um processo de transaminação entre o ácido 3-hidroxi pirúvico e a alanina é produzida serina.
Experimentos com ratos marcando radioficamente o carbono 4 da glicose, concluíram que esse carbono é efetivamente incorporado aos esqueletos de carbono da serina, sugerindo que o referido aminoácido tem um precursor de três carbonos provavelmente do piruvato.
Nas bactérias, a enzima L-serina-desaminase é a principal enzima encarregada de metabolizar a serina: converte L-Serina em um piruvato. Sabe -se que essa enzima está presente e ativa em colheitas de E. coli Concessão em mídia mínima com glicose.
Não se sabe ao certo qual é a função real da L-Serina-desaminase nesses microorganismos, uma vez que sua expressão é induzida por efetores mutacionais que danificam o DNA por radiação ultravioleta, devido à presença de nalidíxico, mincomicina e outros, miatomicina e outros, então se segue que deve ter implicações fisiológicas importantes.
Pode atendê -lo: Dryopithecus: Descoberta, características, crânio, comidaSerine Rich Foods
Todos os alimentos com altas concentrações de proteína são ricos em serina, principalmente ovos, carnes e peixes. No entanto, este é um aminoácido não essencial; portanto, não é estritamente necessário ingeri -lo, tendo em vista o fato de que o corpo é capaz de sintetizá -lo por si só.
Algumas pessoas sofrem de um distúrbio incomum, uma vez que têm um fenótipo de deficiência em relação aos mecanismos de síntese de serina e glicina; portanto, precisam ingerir suplementos alimentares concentrados para ambos os aminoácidos.
Além disso, marcas comerciais especializadas na venda de suplementos vitamínicos (Lamberts, agora Sport e Holomega) oferecem concentrados de fosfatidilserina e L-Serina para aumentar a produção de massa muscular em atletas de alta competição e liffros de peso.
Doenças relacionadas
O mau funcionamento das enzimas envolvidas na biossíntese da serina pode causar patologias graves. Ao diminuir a concentração de serina no plasma sanguíneo e no líquido cefalorraquidiano, pode causar hipertonia, atraso psicomotor, microcefalia, epilepsia e distúrbios complexos do sistema nervoso central.
Atualmente, foi descoberto que a deficiência de serina está envolvida no desenvolvimento de diabetes mellitus, uma vez que a L-Serina é necessária para a síntese de insulina e a de seus receptores.
Os bebês que apresentam defeitos na biossíntese de serina são neurologicamente anormais no nascimento, têm atrasos no crescimento intra -uterino, microcefalia congênita, catarata, convulsões e um sério atraso no desenvolvimento neurológico.
Referências
- Elsila, J. E., DWORKIN, J. P., Bernstein, m. P., Martin, m. P., & Sandford, S. PARA. (2007). Mecanismos de formação de aminoácidos em análogos interestelares de gelo. The Astrophysical Journal, 660 (1), 911.
- Ichord, r. N., & Bearden, D. R. (2017). Encefalopatias metabólicas perinatais. Na neurologia pediátrica de Swaiman (pp. 171-177). Elsevier.
- MOTHET, J. P., Pai, a. T., Wolosker, h., Brady, r. QUALQUER., Linden, d. J., Ferris, c. D.,… & Snyder, S. H. (2000). D-serina é um ligante endógeno para o local da glicina do receptor n-metil-d-aparato. Anais da Academia Nacional de Ciências, 97 (9), 4926-4931
- Nelson, d. eu., Lehninger, a. eu., & Cox, M. M. (2008). Lehninger Principles of Biochemistry. Macmillan.
- Rodríguez, a. E., Ducker, g. S., Billingham, l. K., Martinez, c. PARA., Mainolfi, n., Suri, v.,… & Chandel, n. S. (2019). O metabolismo serina suporta a produção de Macrófagos IL-1β. Metabolismo celular, 29 (4), 1003-1011.
- Tabatabaie, l., Klomp, l. C., Berger, r., & Koning, T. J. (2010). Síntese de L-Serina no sistema nervoso central: uma revisão sobre distúrbios de deficiência de serina. Genética Molecular e Metabolismo, 99 (3), 256-262.
- « Estrutura, características, funções gliceraldeído, características, funções
- História de zinco, propriedades, estrutura, riscos, usa »

