Saponificação

- 1750
- 155
- Tim Mann
Explicamos o que é esponificação, sua reação, por que é importante e damos vários exemplos
 Sabonetes artesanais preparados através da saponificação
Sabonetes artesanais preparados através da saponificação O que é saponificação?
O Saponificação É o processo químico pelo qual o sabão é feito. De fato, a saponificação significa literalmente fabricação de sabão. Este processo consiste em hidrólise alcalina, ou em um meio fortemente básico, dos ésteres de ácidos graxos, como os alcançados em gorduras e óleos comestíveis.
Saponificação é conhecida há séculos. No começo, foi usado para determinar a composição de alguns triglicerídeos comuns, como estearina.
O químico que descobriu a reação pela primeira vez o usou para demonstrar que estearina não passava da união entre um álcool, neste caso a glicerina ou glicerol, com três moléculas de um ácido graxo chamado ácido estearico.
Reação de saponificação
A saponificação É uma reação de hidrólise de um éster de ácidos graxos. Isso significa que o link éster está quebrado (lise - quebrar) por meio da ação da água (hidro - água). Para isso, é necessário o uso de uma base forte, como hidróxido de sódio ou hidróxido de potássio.
Como produtos, um sal ácido é obtido (que é o próprio sabão) e um álcool, como mostrado abaixo:

Mecanismo de reação de saponificação
O mecanismo dessa reação é um processo de três etapas, que começa com um ataque do íon hidróxido, depois a eliminação do álcool e, finalmente, a formação de sal.
-
Etapa 1: ataque de íons hidróxido
O primeiro passo, e a razão pela qual é necessário adicionar hidróxido de sódio ou alguma outra base forte é o ataque do hidróxido ao éster:
Pode atendê -lo: chitosano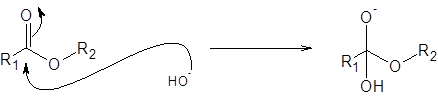
-
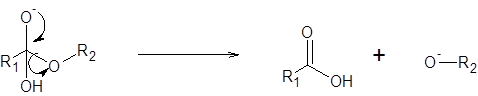
Etapa 2: Eliminação de álcool na forma de um íon alcoxido
Nesta fase, o par de elétrons de oxigênio empurra o álcool e o separa do éster na forma de um íon alcoxido. Este íon é uma base muito forte. Além do alcoxide, também é formada uma molécula de ácido carboxílico (que é um ácido graxo).
-
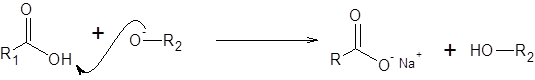
Etapa 3: formação de sal
O íon alcoxídico formado no estágio anterior é uma base muito forte e remove facilmente o próton do ácido carboxílico. Ao fazer isso, faz ácido.
Triglicerídeos
Em geral, a reação de saponificação é realizada com gorduras ou óleos, vegetais ou animais.
 Os óleos vegetais, como o azeite, geralmente são usados para fazer sabonetes de saponificação
Os óleos vegetais, como o azeite, geralmente são usados para fazer sabonetes de saponificação Os ésteres presentes nessas gorduras e óleos são quase sempre triglicerídeos ou ésteres de ácidos graxos com um álcool especial chamado glicerol ou glicerina.
Nesses casos, a reação de saponificação é vista como:
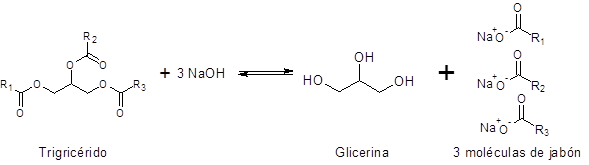
R1, R2 e r3 Eles representam as correntes de ácidos graxos. Como existem muitos ácidos graxos diferentes, a saponificação pode fornecer sabonetes diferentes com sabonetes diferentes.
Produtos de saponificação
Dependendo do óleo ou gordura inicial e de qual base é usada, os sabonetes com propriedades diferentes serão obtidos.
- Por exemplo, O uso de hidróxido de sódio ou potássio dará como produto um sal de sódio ou um sal de potássio (um sabão de sódio ou potássio). Em geral, os sabonetes de potássio têm menos ponto de fusão que o sódio, e alguns são até líquidos à temperatura ambiente.
Da mesma forma, as características do ácido graxo que fazem parte do éster também afetarão as propriedades do sabão resultante. Quanto mais tempo a corrente, maior seu ponto de fusão.
Por esse motivo, quando você deseja preparar sabonetes líquidos, por exemplo, os ácidos graxos são selecionados com correntes mais curtas e hidrolisados com hidróxido de potássio em vez de sódio.
Importância da saponificação
Saponificação é uma reação muito importante.
- Em nível industrial, é a reação usada para a fabricação de todos os sabonetes de macarrão, como sabonetes de mão ou sabonetes de lavagem de barras.
- Por outro lado, também é frequentemente usado como o primeiro passo na obtenção de ácidos graxos, que são usados em uma ampla variedade de indústrias como a fabricação de cosméticos.
- Em outros casos, os ácidos graxos são frequentemente usados como solventes ou agentes dispersos na fabricação de pinturas, embora seja mais comum alcançar óleos minerais nesses casos.
- Além disso, essa reação também é usada para limpar qualquer superfície gordurosa, como o interior dos fornos ou a superfície das cozinhas.
Nos casos em que as gorduras estão muito próximas da superfície ou são char gordas. Dessa maneira, a gordura se torna sabão, o sabão se dissolve na água e a superfície está limpa.
Pode atendê -lo: carbocação: formação, características, tipos, estabilidadeExemplos de reações de saponificação
-
Saponificação de estearina
A estearina é um triglicerídeo que contém três moléculas de ácido esteárico ligadas à glicerina. Sua saponificação produz três moléculas de sabão, neste caso de sódio ou estearato de potássio.
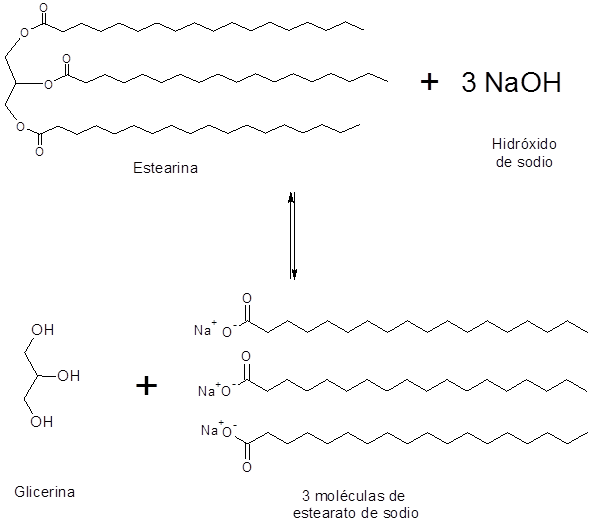
-
Saponificação de ácido oleico
Os óleos de azeitona e girassol contêm mais de 80% de ácido oleico. Esta é uma gordura insaturada que possui 18 cadeias de carbono. A saponificação desses óleos produz, entre outras coisas, óleo de sódio.
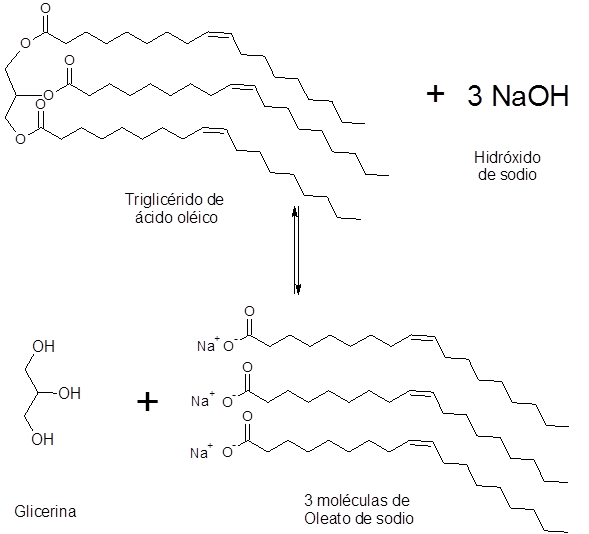
-
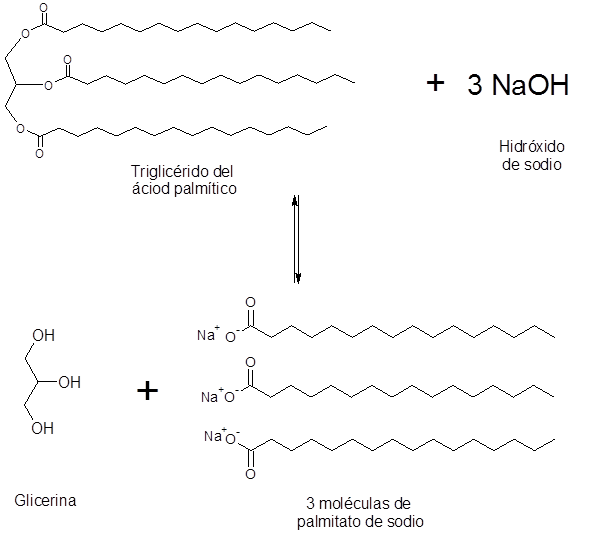
Saponificação de ácido palmítico
O ácido palmítico é um ácido graxo saturado a longo prazo contendo 16 átomos de carbono. Este é o ácido graxo mais importante da dieta humana. É o principal ácido graxo saturado em nosso corpo.
Em alimentos, o ácido palmítico é um dos principais componentes da gordura animal, portanto, sabonetes preparados a partir de gorduras como manteiga de gado, principalmente o sedimento ou o palmitato de potássio.
Além disso, o ácido palmítico forma mais de 40% do óleo de palma (daí o seu nome). De fato, a saponificação de óleo de palma é a principal fonte industrial de ácido palmítico em todo o mundo.