Qual é o teste de bromo?

- 702
- 54
- Conrad Schmidt
O teste de bromo É um ensaio que se aplica a amostras de compostos orgânicos de composição desconhecida e permite detectar a presença de links duplos, links triplos, grupos fenólicos e anilinas.
A amostra desconhecida é adicionada a uma solução aquosa de bromo, que é marrom ou laranja. Se, ao adicionar a amostra, a coloração marrom desaparecer, significa que ocorre uma insaturação presente e, se a formação de um sólido branco ocorrer, é um sinal de que existe um fenol ou uma anilina.
 Água de bromo. Se, ao adicionar uma amostra, sua coloração marrom avermelhada desaparecer, isso indica a presença de insaturação. Madowiki/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/3.0). Fonte: Wikimedia Commons.
Água de bromo. Se, ao adicionar uma amostra, sua coloração marrom avermelhada desaparecer, isso indica a presença de insaturação. Madowiki/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/3.0). Fonte: Wikimedia Commons. É um teste qualitativo, pois as quantidades não são determinadas, mas apenas a presença dos grupos funcionais mencionados acima mencionados.
A insaturação presente nos alcenos (ligações duplas c = c) reage facilmente com o bromo. Isso também acontece com os fenóis e anilinas em que o anel aromático se torna muito reativo devido à influência dos grupos -OH e -nhH2 respectivamente.
Existem dois ensaios relacionados a este teste que usam a mesma reação química. Eles permitem obter parâmetros importantes para se qualificar de maneira qualitativa de refino de petróleo e alguns de seus derivados.
[TOC]
Fundação de teste interrompida
O Bromo reage com ligações duplas e triplas e também com moléculas que contêm nitrogênio básico, como aminas aromáticas e álcoois aromáticos (fenóis). No entanto, olefinas são os lugares mais reativos.
Bromo
Este elemento (Br) pertence ao grupo halogens, juntamente com fluoreto, cloro e iodo. O brominato molecular (BR2) É um líquido marrom avermelhado. Uma solução aquosa saturada de bromo molecular a 20 ° C contém 3,6 % (massa/volume) deste elemento.
 Água saturada de bromo. Matthew Sergei Perrin, de Auckland, Nova Zelândia/CC por (https: // criativecommons.Org/licenças/por/2.0). Fonte: Wikimedia Commons.
Água saturada de bromo. Matthew Sergei Perrin, de Auckland, Nova Zelândia/CC por (https: // criativecommons.Org/licenças/por/2.0). Fonte: Wikimedia Commons. Olefinas ou alcenos
Eles são compostos insaturados com a Fórmula CnH2n. Eles são chamados de insaturados porque têm uma ou mais ligações duplas C = C. O nome desses compostos termina em -Env, como etene (também chamado de etileno), profeno (propileno), bu young.
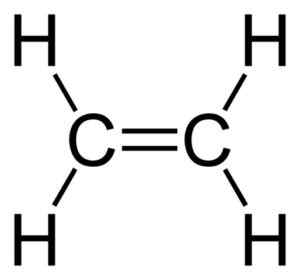 Etene ou etileno. Você pode ver a ligação dupla C = C. Autor: Benjah-BMM27. Fonte: Wikimedia Commons.
Etene ou etileno. Você pode ver a ligação dupla C = C. Autor: Benjah-BMM27. Fonte: Wikimedia Commons. 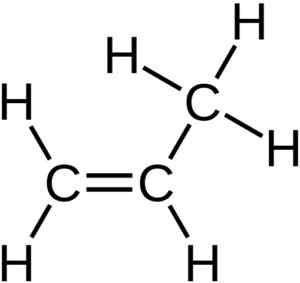 Propano ou propileno. Nohingserius / Domínio de Pub. Fonte: Wikimedia Commons.
Propano ou propileno. Nohingserius / Domínio de Pub. Fonte: Wikimedia Commons. 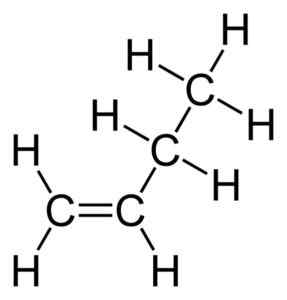 Buteno ou butileno. Autor: Benjah-BMM27. Fonte: Wikimedia Commons.
Buteno ou butileno. Autor: Benjah-BMM27. Fonte: Wikimedia Commons. São substâncias instáveis se comparadas aos alcanos, então eles reagem facilmente com bromo e outros compostos.
Reação de bromo com olefinas e alguns alcinos
O bromo molecular reage com a ligação dupla de alcenos que formam compostos dibromados. Esta reação é chamada de adição. Abaixo está um exemplo de adição bromica a uma ligação dupla:
Pode atendê -lo: sulfato férrico: estrutura, propriedades, riscos e usos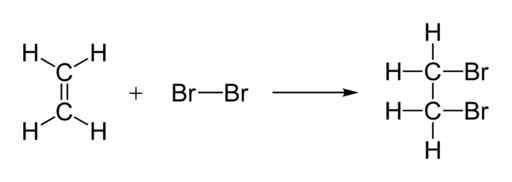 Adição de bromo ao etileno. Benjah-BMM27 / Domínio Público. Fonte: Wikimedia Commons.
Adição de bromo ao etileno. Benjah-BMM27 / Domínio Público. Fonte: Wikimedia Commons. Ao adicionar o alceno à solução de laranja marrom ou bromo, ele reage com a olefina formando um composto incolor. A água de bromo descolor.
Alquinos tem links triplos (C≡C). A bromação de Etino (HCidor) produz Cis- e Trans-1.2-dibrometeno e 1,1,2,2-tetrabromoetano. Na figura encontrada abaixo, o Trans-1.2-dibromoteno.
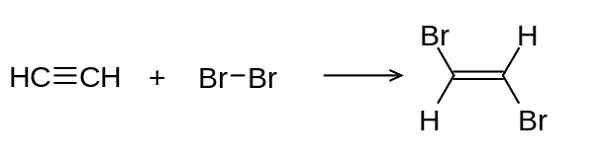 Adição de bromo ao link Triple Etino. Roland Mattern/GFDL (http: // www.gnu.Org/copyleft/fdl.html). Fonte: Wikimedia Commons.
Adição de bromo ao link Triple Etino. Roland Mattern/GFDL (http: // www.gnu.Org/copyleft/fdl.html). Fonte: Wikimedia Commons. Fenóis e reação com bromo
São compostos cuja fórmula geral é Aroh, onde AR é um grupo aromático como fenil, fenil de substituição ou qualquer outro grupo aromático. Eles diferem dos álcoois em que o grupo -OH está diretamente ligado ao anel aromático.
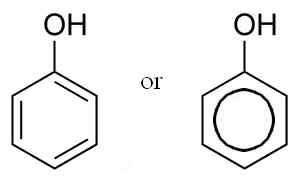 O fenol é um álcool onde o oxigênio está diretamente ligado ao anel aromático. Autor: Dbenbenn. Fonte: Wikimedia Commons.
O fenol é um álcool onde o oxigênio está diretamente ligado ao anel aromático. Autor: Dbenbenn. Fonte: Wikimedia Commons. Uma de suas propriedades químicas mais importantes, além da acidez, é a alta reatividade de seu anel aromático em relação à substituição eletrofílica. Isto é, a substituição de um hidrogênio anel por um átomo E -Aavid.
É por isso que eles reagem facilmente com o bromo.
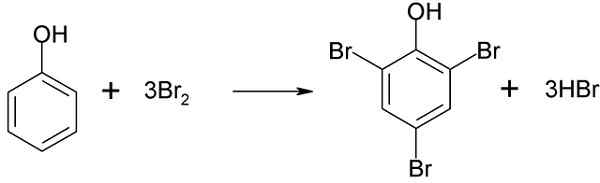 Reação de bromo com fenol. AKANE700/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/3.0). Fonte: Wikimedia Commons.
Reação de bromo com fenol. AKANE700/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/3.0). Fonte: Wikimedia Commons. Anilines e reação com bromo
São aminas aromáticas, ou seja, compostos que têm um grupo amino (-nh2) cujo átomo de nitrogênio está diretamente ligado a um anel aromático. O membro mais simples é Aniline:
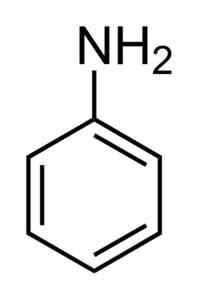 Estrutura de anilina. O nitrogênio está diretamente ligado ao anel aromático. Brilho. / Domínio público. Fonte: Wikimedia Commons.
Estrutura de anilina. O nitrogênio está diretamente ligado ao anel aromático. Brilho. / Domínio público. Fonte: Wikimedia Commons. Eles apresentam uma basicidade apreciável. O nitrogênio do grupo amino possui um par de elétrons livres que oferecem um alto grau de nucleofilicidade ou afinidade em relação aos compostos que estão ausentes de elétrons e fornecem alta reatividade ao anel aromático.
Por esse motivo, eles reagem facilmente com o bromo, que ataca o anel aromático. Por exemplo, a anilina com bromo forma 2,4,6-tribromoanilina.
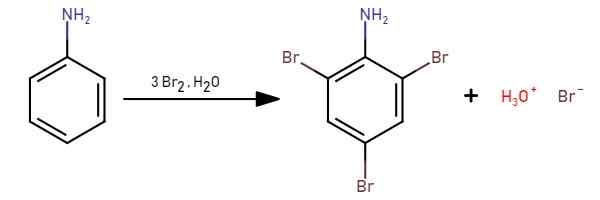 Reação de anilina com bromo. FUNG06831/CC BY-SA (https: // criativeCommons.Org/licenças/BY-SA/4.0). Fonte: Wikimedia Commons.
Reação de anilina com bromo. FUNG06831/CC BY-SA (https: // criativeCommons.Org/licenças/BY-SA/4.0). Fonte: Wikimedia Commons. Testes relacionados a este ensaio
Existem outros testes que também aproveitam a reação do bromo com as ligações duplas. São métodos qualitativos para medir os locais reativos de uma amostra. Os testes são o número de bromo e o índice de bromo.
Pode atendê -lo: Pentena: estrutura química, propriedades, síntese, usaNúmero de Bromo
São gramas de bromo (g) que reagem com 100 g da amostra. É usado em destilados de petróleo, como gasolina, keroseén e algum gás. Também é aplicado em misturas comerciais de monoolonefins alifáticos.
ÍNDICE DE BROMINA
É o número de miligramas (mg) de bromo que reage com 100 g da amostra. É usado na indústria química em materiais ou líquidos que têm um teor de olefina muito baixo.
Geração de bromo No local
Nesses ensaios, o bromo é gerado no site usando uma solução de brometo e bromato.
Irmão3- + 5 br- + 6 h+ → 3 br2 + 3 h2QUALQUER
Uma vez formado, o bromo reage com os links c = c. A reação é monitorada por titulação eletrométrica. O procedimento preciso foi publicado pela Sociedade Americana de Testes e Materiais ou ASTM (sigla para a Sociedade Americana de Inglês para testes e materiais).
O número de bromo corresponde ao método ASTM D1159 e o índice de bromo é descrito nos métodos ASTM D 2710, ASTM D 1492 e ASTM D 5776.
Aplicações desses ensaios
O número de bromo é uma medida de insaturação alifática em amostras de petróleo e seus destilados. Em monoolonefins alifáticos comerciais, serve para fornecer evidências de sua pureza e identidade.
O índice de bromo se aplica apenas a hidrocarbonetos essencialmente livres de olefinas, permitindo medir traços destes.
Correntes de alimentação da FCC
Ambos os parâmetros também são medidos em materiais pesados, como alimentos para o sistema de rachaduras catalíticas em leito fluidizado ou FCC (sigla para inglês Rachaduras catalíticas de fluido), usado em refino de petróleo.
Ambos os testes fazem parte de uma série de testes aplicados rotineiramente às correntes de alimentação da FCC, que são importantes para sua caracterização na estrutura molecular, pois permitem desenvolver modelos cinéticos para prever o desempenho dos produtos desejados.
 Instalações da FCC em uma refinaria de petróleo. Valero Energy Corporation / TX / Domínio Público. Fonte: Wikimedia Commons.
Instalações da FCC em uma refinaria de petróleo. Valero Energy Corporation / TX / Domínio Público. Fonte: Wikimedia Commons. Razões para o conteúdo de Alkeen ser baixo
Nos processos da FCC, as olefinas podem polimerizar e gerar produtos indesejáveis, como lodo e coca. É por isso que é desejado que as correntes de alimentação da FCC tenham menos de 5% (peso) de olefinas.
Pode atendê -lo: atividade enzimática: unidade, medição, regulamentação e fatoresAs correntes de alimentação hidrotratadas têm um número de bromo menor que 5, no diesel de vácuo pesado é 10 e no diesel de coquização é de 50. Como regra geral, diz -se que a fração de olefinas de uma amostra é aproximadamente metade de seu bromo.
Combustíveis
Nos motores de combustão, os alcenos presentes na gasolina podem polimerizar a formação de borracha e vernizes que são depositados nas paredes do sistema, filtros e tubos finos cobrindo -os.
Isso pode resultar em fluxo de combustível, redução de energia do motor e até mesmo impedir que este começo.
 Gasolina. Hambúrguer / domínio público. Fonte: Wikimedia Commons.
Gasolina. Hambúrguer / domínio público. Fonte: Wikimedia Commons.  A presença de excesso de olefinas na gasolina pode causar problemas do motor. Autor: Steve Howard. Fonte: Pixabay.
A presença de excesso de olefinas na gasolina pode causar problemas do motor. Autor: Steve Howard. Fonte: Pixabay. Por esses motivos, a determinação das olefinas em alguns derivados de petróleo é importante, pelo menos qualitativamente com esses testes.
Referências
- Sadeghbeigi, R. (2012). Caracterização da alimentação da FCC. Número de bromo e índice de bromo. No manual de rachaduras catalíticas de fluido. Capítulo 3. (Terceira edição). Recuperado de cientedirect.com.
- Marczenko, Z. e Balkcak, M. (2000). Separação, pré -concentração e espectrofotometria na análise inorgânica. Na biblioteca de espectroscopia analítica. Recuperado de cientedirect.com.
- Fundação Wikimedia. (2020). Teste de bromo. Recuperado de.Wikipedia.org.
- Saikia, i. et al. (2016). Uso de compostos de bromo e bromo-orgânico na síntese orgânica. REVISÕES QUÍMICAS 2016, 116, 12, 6837-7042. Recuperado de bares.ACS.org.
- Morrison, r.T. e boyd, r.N. (2002). Química orgânica. 6ª edição. Prentice-Hall.
- Mettler Toledo. ASTM D1159 Número de bromo de produtos petrolíferos - Mettler Toledo. MT recuperou.com.
- ASTM D2710-09 (2018). Método de teste padrão para Índice de bromo de hidrocarbonetos de petróleo por titulação eletrométrica. Recuperado da ASTM.org.
- ASTM D1159-07 (2017). Método de teste padrão para números de bromo de destilados de petróleo e olefinas alifáticas comerciais por titulação eletrométrica. Recuperado da ASTM.org.
- Metrohm ag. (2018). Boletim de aplicação 177/5 E. Determinação automática do número de bromo e o índice de bromo em produtos petrolíferos. Metrohm recuperado.com.

