O que é corrosão e como evitá -la?

- 3639
- 422
- Ralph Kohler
 Metal corroído
Metal corroído O que é corrosão?
Para saber Como evitar a corrosão É importante saber o que é corrosão e por que ocorre. O processo natural é chamado de corrosão na qual um metal se deteriora gradualmente como resultado de reações eletroquímicas (ou químicas) com seu ambiente.
Essas reações fazem com que os metais refinados pareçam. A corrosão também ocorre em materiais não metálicos, como cerâmica e polímeros, mas é diferente e geralmente é chamado de degradação.
A corrosão é um processo inimigo do ser humano, uma vez que esses danos degradam os materiais, mudam sua coloração e os enfraquecem, aumentando a possibilidade de ruptura e aumentar os custos por reparo e substituição deles.
Por esse motivo, existem campos inteiros na ciência dos materiais dedicados à prevenção desse fenômeno, como a engenharia de corrosão. Os métodos de prevenção de corrosão são variados e dependerão dos materiais afetados.
Métodos para evitar a corrosão
Primeiro, deve -se levar em consideração que nem todos os metais funcionam na mesma velocidade, e alguns têm a peculiaridade de não serem naturalmente corroerados, como no caso de aço inoxidável, ouro e platina.
Isso acontece porque existem materiais para os quais a corrosão é termodinamicamente desfavorável (ou seja, eles não atingem maior estabilidade com os processos que os levam a isso) ou porque têm uma reação cinética tão lenta que os efeitos da corrosão levam tempo para mostrar.
Pode atendê -lo: bromotimol azulMesmo assim, para os elementos que estão em execução, há uma série de métodos para evitar esse processo natural e dar a eles mais vida:
Galvanizado
É o método de prevenção de corrosão no qual uma liga de ferro e aço com uma fina camada de zinco é coberta. O objetivo deste método é fazer com que os átomos de zinco do revestimento reagam com as moléculas de ar, oxidando e atrasando a corrosão da peça que eles cobrem.
Esta metodologia faz do zinco um ânodo galvânico ou ânodo de sacrifício, fazendo com que seja exposto à degradação da corrosão para salvar um material mais valioso.
O galvanizado pode ser alcançado pela imersão das partes metálicas em zinco derretido a altas temperaturas, bem como em camadas mais finas que são alcançadas com eletrogalvanização.
Este último é a metodologia que protege mais, já que o zinco está ligado ao metal por processos eletroquímicos e não apenas por processos mecânicos, como na imersão.
Pinturas e cobertura
A aplicação de pinturas, placas de metal e esmaltes é outra maneira de adicionar uma camada protetora aos metais propensos a corrosão. .
Outras coberturas têm propriedades específicas que os tornam corrosão ou inibidores anticorrosivos. Estes são adicionados primeiro a líquidos ou gases e depois são adicionados na forma de um metal no metal.
Esses compostos químicos são muito usados na indústria, especialmente em tubos que transportam líquidos; Além disso, eles podem ser adicionados à água e refrigerantes para garantir que não gerem corrosão no equipamento e tubos através dos quais passam.
Pode atendê -lo: Princípio da AufbauAnodização
É um procedimento de passivação eletrolítica; isto é, o processo pelo qual um filme um tanto inerte é formado na superfície de um elemento metálico. Este processo é usado para aumentar a espessura da camada de óxido natural que este material tem em sua superfície.
Esse processo tem a grande vantagem de não apenas adicionar proteção contra corrosão e fricção, mas também fornece maior adesão para camadas de tinta e cola do que o material descoberto.
Apesar de ter experimentado mudanças e evoluções ao longo do tempo, esse processo é comumente realizado pela introdução de um objeto de alumínio em uma solução eletrolítica e passando uma corrente direta por meio disso.
Essa corrente fará com que o ânodo de alumínio libere hidrogênio e oxigênio, gerando óxido de alumínio que se juntará a ele para aumentar a espessura de sua camada superficial.
A anodização gera mudanças na textura microscópica da superfície e na estrutura cristalina do metal, causando uma alta porosidade a ser gerada na mesma.
Portanto, apesar de melhorar a força e a resistência à corrosão do metal, também pode torná -lo mais quebradiço, além de reduzir sua resistência a altas temperaturas.
Biipels
Biipels são grupos de microorganismos que se ligam na forma de uma camada em uma superfície, se comportando como um hidrogel, mas ainda representando uma comunidade viva de bactérias ou outros microorganismos.
Embora essas formações estejam geralmente associadas à corrosão, nos últimos anos houve um desenvolvimento no uso de biofilmes bacterianos para proteger metais em ambientes altamente corrosivos.
Pode atendê -lo: relacionamento de química com outras ciênciasAlém disso, biofilmes com propriedades antimicrobianas foram descobertas, que impedem os efeitos da bactéria reduzindo o sulfato.
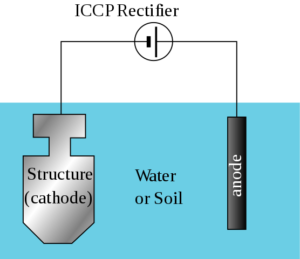
Correntes impressas
Nessas estruturas muito grandes ou onde a resistividade de eletrólitos é alta, os ânodos galvânicos não podem gerar corrente suficiente para proteger toda a superfície; portanto, um sistema de proteção catódica é usado por correntes impressas.
Esses sistemas consistem em ânodos conectados a uma fonte de energia de corrente direta, principalmente um transformador-recipiente conectado a uma fonte de corrente alternada.
Este método é usado principalmente em cargueiros e outros navios, que requerem um alto nível de proteção em uma superfície maior de sua estrutura, como hélices, ludges e outras peças nas quais a navegação depende.
Mudanças nas condições ambientais
Finalmente, a taxa de corrosão pode parar ou reduzir com a alteração das condições ambientais nas quais o material metálico está localizado.
O conteúdo de umidade e enxofre, cloretos e oxigênio em líquidos e gases devem ser mantidos em níveis baixos para aumentar a expectativa de vida de um material e usar menos solução salina e/ou água dura tem um efeito positivo.
Referências
- Wikipedia. (s.F.). Corrosão. Obtido de in.Wikipedia.org
- Balance, t. (s.F.). Proteção de corrosão para metais. Obtido de The Galance.com
- EoCoat. (s.F.). Métodos de prevenção de corrosão. Obtido da EoCoat.com
- MetalsuperMarkets. (s.F.). Como evitar a corrosão. Obtido a partir de metalsupermarkets.com
- Corrosionpedia. (s.F.). Proteção catódica atual impressa (ICCP). Obtido da corrosionpedia.com