Oxácido
- 2452
- 719
- Ernesto Bruen
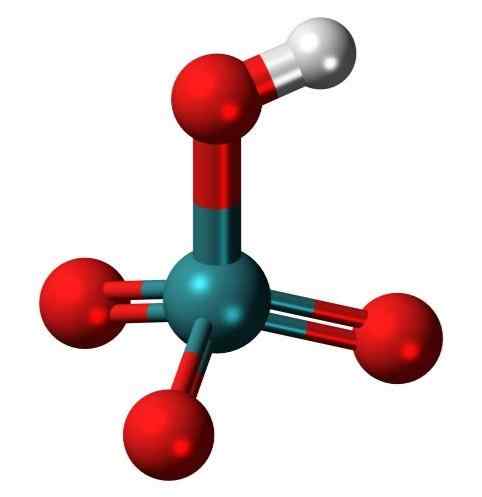
 Molécula de ácido pertetalético, um ácido oxo muito raro de Tecnecio. Fonte: Jynto, Wikimedia Commons
Molécula de ácido pertetalético, um ácido oxo muito raro de Tecnecio. Fonte: Jynto, Wikimedia Commons O que é um oxácido?
A Oxácido, U oxoacid, é um ácido que contém oxigênio. É composto de hidrogênio, oxigênio e um elemento não -metálico que constitui o átomo central chamado. Dependendo do número de átomos de oxigênio e, portanto, os estados de oxidação do elemento não -metálico podem formar vários oxácidos.
Oxcacids têm um grande número de usos, que são difíceis de descrever em geral. Sua aplicação dependerá muito do átomo central e do número de oxigênio.
Eles podem servir a partir de compostos para síntese de materiais, fertilizantes e explosivos, mesmo para fins analíticos ou produção de refrigerantes, como ocorre com ácido carbônico e ácido fosfórico, H3Po4, fazer parte da composição dessas bebidas.
Características e propriedades do oxcacid
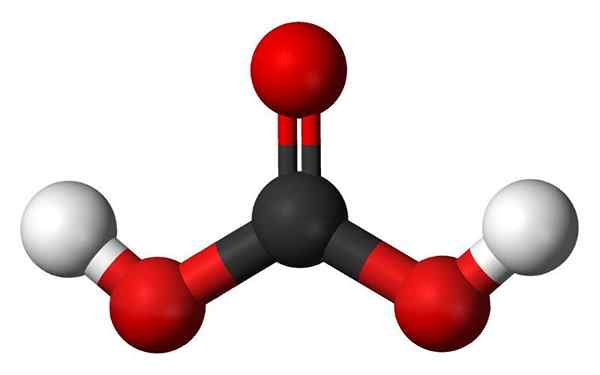 Molécula de ácido carbônico. Fonte: Jynto e Ben Mills, Wikimedia Commons
Molécula de ácido carbônico. Fonte: Jynto e Ben Mills, Wikimedia Commons - Grupos hidroxila: Uma das principais características de um oxácido não é apenas que ele tem oxigênio, mas também é como um grupo OH. Por outro lado, alguns oxácidos têm o que é chamado de grupo oxo, e = o. No caso de ácido fosfora, possui um grupo oxo, p = O. Eles não têm átomos H, então "eles não são responsáveis" pela acidez.
- Átomo central: O átomo central (e) pode ou não ser um elemento eletronegativo, dependendo de sua localização no bloco P da tabela periódica. Por outro lado, o oxigênio, um elemento ligeiramente mais eletronegativo que o nitrogênio, atrai os elétrons da ligação OH, permitindo assim a liberação do íon h+. E, portanto, está ligado a grupos OH. Quando um íon h é liberado+ A ionização ácida ocorre, ou seja, adquire uma carga elétrica, que no seu caso é negativa. Um oxcacid pode liberar tantos íons h+ Como os grupos de OH têm em sua estrutura, e quanto mais existem, maior a carga negativa será.
- Força ácida: A força de quase todos os oxácidos que têm o mesmo átomo central (sem metal) aumenta com o aumento do status de oxidação do elemento central, que por sua vez está diretamente relacionado ao aumento do número de átomos de oxigênio.
Por exemplo, três séries de oxácidos são mostradas cujas forças de acidez são ordenadas do menos para o maior:
H2SW3 < H2SW4
Hno2 < HNO3
HCLO < HClO2 < HClO3 < HClO4
Na maioria dos oxacídeos que têm elementos diferentes com o mesmo estado de oxidação, mas pertencentes ao mesmo grupo da tabela periódica, a força de acidez aumenta diretamente com a eletronegatividade do átomo central:
H2SEO3 < H2SW3
H3Po4 < HNO3
Hbro4 < HClO4
Formação de oxcacid
Como mencionado no início, o oxácidos é gerado quando certas substâncias, chamadas óxidos ácidos, reagem com água. Isso será explicado usando o mesmo exemplo de ácido carbônico.
Co₂+h₂o h2Co3
Óxido ácido + água => oxácido
O que acontece é que a molécula de H₂o se liga covalentemente à de co₂. Se a água for eliminada pelo calor, o equilíbrio para a regeneração dos movimentos de co₂, ou seja, uma bebida de refrigerante quente em breve perderá sua sensação efervescente do que um resfriado.
Por outro lado, os óxidos ácidos são formados quando um elemento não -metálico reage com a água, embora, com mais precisão, quando o elemento reagente forma um óxido com um caráter covalente, cuja solução na água gera tons h -íons h+.
Já foi dito que os íons h+ Eles são o produto da ionização de oxácido resultante.
Exemplos de treinamento
O óxido clorico, CL2QUALQUER5, Reaja com água para dar o ácido clorico:
Cl2QUALQUER5 + H₂o => hclo3
Óxido sulfúrico, então3, Reage com água para formar ácido sulfúrico:
SW3 + H₂o => h2SW4
E o óxido periúdio, eu2QUALQUER7, reage com a água para formar o ácido periódico:
Yo2QUALQUER7 + H₂o => hio4
Além desses mecanismos clássicos para a formação de oxácidos, existem outras reações para o mesmo objetivo.
Pode atendê -lo: reação endotérmicaPor exemplo, tricloreto de fósforo, PCL3, Ele reage com a água para produzir ácido fosforoso, um oxácido e ácido clorídrico, um ácido halo -hídrico.
Pcl3 + 3h2O => H3Po3 + Hcl
E pentacloreto de fósforo, PCL5, reage com água para dar ácido fosfórico e ácido clorídrico.
Pcl5 + 4 h₂o => h3Po4 + Hcl
Oxcacídeos metálicos
Alguns metais de transição formam óxidos ácidos, ou seja, se dissolvem na água para dar oxácidos.
Óxido de manganês (VII) (Anidrum Permanganic) MN2QUALQUER7 E óxido de cromo (VI) são os exemplos mais comuns.
Mn2QUALQUER7 + H₂o => hmno4 (ácido permanganic)
Cro3 + H₂o => h2Cro4 (ácido crômico)
Nomenclatura
Cálculo do Valencia
Para nomear corretamente um oxácido. A partir da fórmula genérica do HEO, o seguinte é considerado:
- O O tem Valência -2.
- A Valencia de Los H Es +1.
Com isso em mente, o oxácido. Assim, você tem a seguinte soma algébrica:
-2 + 1 + e = 0
E = 1
Portanto, E é +1 Valencia.
Então as valores possíveis que podem ter e. Se entre suas valências são valores +1, +3 e +4 e depois "trabalhar" com sua menor valência.
Nome ácido
Nomear o HEO começa chamando -o de ácido, seguido pelo nome de E com os sufixos -ico, se você trabalha com a maior Valência, ou -Ono, se você trabalha com o menor. Quando há três ou mais, os hipo-prefixos são usados para se referir ao menor e maior das valências.
Assim, Heo seria chamado:
Ácido soluço(Nome de E)urso
Como +1 é o menor de seus três vales. E se fosse heo2, Então eu teria Valencia +3 e seria chamado:
Pode atendê -lo: difenilaminaÁcido (e)urso
E da mesma maneira para Heo3, Com e trabalhando com Valencia +5:
Ácido (e)ico
Exemplos
- Ácido crômico (H2Cr2QUALQUER4). É um ácido forte e instável a altas temperaturas.
- Ácido dicrômico (H2Cr2QUALQUER7). Sua presença é perceptível em misturas de ácido crômico usadas para limpar o vidro.
- Ácido hipocloroso (HCLO). Repare rapidamente os tecidos da pele.
- Ácido bromo (hbro2). É um composto intermediário e instável. Composto Bromo.
- Ácido ortofosfórico (H3Po4). Ácido irritante para a pele não combustível.
- Ácido permanganic (hmno4). Ácido muito forte.
- Ácido periódico (hio4). Na química orgânica, é usado para analisar as estruturas de outras moléculas.
- Ácido brômico (hbro3). Oxcacid de bromo. Seus sais são poderosamente oxidantes.
- Ácido hipobromo (hbro). É usado em solução aquosa diluída e é obtida por reação entre água e o BR2.
- Ácido metafosfórico (HPO3). Muito corrosivo, incolor e sólido ao banheiro à temperatura ambiente.
- Ácido yodium (hio3). Reativo usado para detectar morfina em um produto.
- Ácido de enxofre (H2SW3). Causando chuva ácida.
- Ácido sulfúrico (H2SW4). Regular para processamento de metal e fertilizantes, é um dos compostos químicos mais usados.
- Ácido nítrico (hno3). Reagente de laboratório, muito perigoso porque pode queimar a pele.
- Ácido clorico (HCLO3). Ao decompor, produz muitos produtos. É frio estável para uma concentração de 30%.
- Ácido arsenioso (h3ASO3). Contém arsênico e é muito tóxico e carcinogênico. É usado em herbicidas e pesticidas.
- Ácido ortossílico (H4SiO4). Ácido fraco usado como agente de suporte ou dessecante.
- Ácido carbônico (H2Co3). É usado para fazer refrigerantes.
- Ácido nitroso (hno2). Em solução, é notavelmente dissociado.
- Ácido metabórico (HBO2). Sólido branco cristalino levemente solúvel.
Referências
- Compostos oxoácidos comuns. Recuperado do pensamento.com.

