Número atômico
- 943
- 88
- Terrell Stokes
Qual é o número atômico?
O número atômico de um elemento químico indica o número de prótons contidos no núcleo atômico do referido elemento. No caso de ser um átomo neutro, o número atômico coincidirá com o número de elétrons do referido elemento.
Como é conhecido, o núcleo atômico consiste em prótons e nêutrons. Os prótons têm uma carga positiva e seu valor coincide com o valor absoluto da carga negativa do elétron, que é 1,6 x 10-19 Coulomb em unidades de sistema internacional.
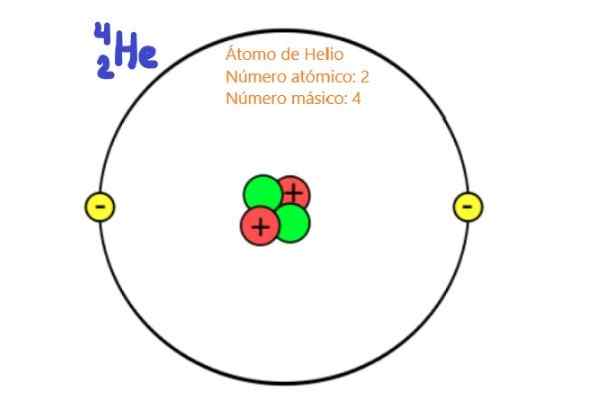
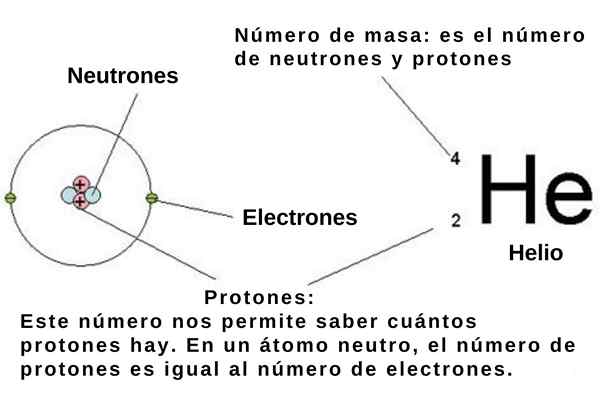
 figura 1. Esquema de um átomo de hélio (ele). O número de prótons é o número atômico. O número de nêutrons mais o número de prótons é o número de massa. Fonte: Wikimedia Commons.
figura 1. Esquema de um átomo de hélio (ele). O número de prótons é o número atômico. O número de nêutrons mais o número de prótons é o número de massa. Fonte: Wikimedia Commons. Porque eles são partículas do núcleo atômico, prótons e nêutrons são conhecidos como Nucleonas. São essas partículas que praticamente determinam a massa do átomo, uma vez que os núcleons são cerca de dois mil vezes mais massivos que os elétrons do átomo. Por esse motivo, o número de núcleos em um átomo é chamado Número de massa.
No entanto, o número atômico É aquele que determina a afinidade química dos elementos atômicos, porque em átomos neutros esse número coincide com o número de elétrons.
Representação do número atômico
Na tabela periódica, o símbolo X de um elemento químico é acompanhado no lado esquerdo inferior com o número Z que representa o número atômico do referido elemento, enquanto no canto superior esquerdo do símbolo químico do elemento o número de massa é indicado para.
Pode servir a você: Andrômeda: descoberta, origem, características, estruturaA figura a seguir mostra esta notação:
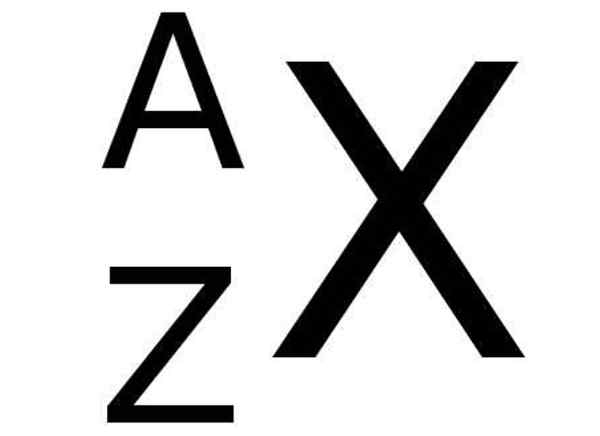 Figura 2. Número atômico Z do elemento químico X e Mass Número A do elemento químico X, de acordo com a convenção usada na tabela periódica. Fonte: Wikimedia Commons.
Figura 2. Número atômico Z do elemento químico X e Mass Número A do elemento químico X, de acordo com a convenção usada na tabela periódica. Fonte: Wikimedia Commons. E então, a Tabela 1 mostra alguns exemplos de elementos químicos com sua respectiva notação e número atômico e de massa:
tabela 1
| Elemento | Notação | Número atômico Z | Número de massa a |
|---|---|---|---|
| Hidrogênio | 1 1 H | 1 | 1 |
| Carbono | 12 6 C | 6 | 12 |
| Oxigênio | 16 8 QUALQUER | 8 | 16 |
| Urânio | 238 92 OU | 92 | 238 |
Número atômico e ordem dos elementos na tabela periódica
A tabela periódica Os elementos químicos permitem a ordem seqüencial e crescente dos elementos, de acordo com o valor de seu número atômico.
Pelo menos 118 deles são conhecidos, começando com hidrogênio até atingir o elemento 118, que é o Oganeseon -Antes de chamado AACTIO-, cujo produto químico é OG e o número de massa é 294.
Os 10 primeiros elementos químicos com ordem crescente em número atômico são muito mais familiares. Assim, por exemplo, temos o mais conhecido:
- Hidrogênio, h
- Helio, ele
- Lithium, Li
- Berílio, Be
- Boro, b
- Carbono, c
- Nitrogênio, n
- Oxigênio, o
- Fluoreto, f
- Neon, NE
 Figura 3. Tabela periódica simplificada mostrando os símbolos dos elementos químicos e seu número atômico
Figura 3. Tabela periódica simplificada mostrando os símbolos dos elementos químicos e seu número atômico Configuração eletronica
O número atômico indica o número de prótons no núcleo atômico de um elemento químico e cada próton, como dissemos, tem uma carga positiva elementar de 1.602 x 10-19 C.
Se o átomo for neutro, o número de elétrons com carga negativa elementar de -1.602 x10-19 C deve ser igual ao número atômico. Então, conhecendo a posição numérica de um elemento químico na tabela periódica, seu número de elétrons também é conhecido.
Pode atendê -lo: transistor de poderNo átomo, esses elétrons ocupam regiões chamadas Orbitais, que dependem da energia e do momento angular do elétron. Por sua vez, tanto a energia quanto o momento angular dos elétrons no átomo são quantizados. Isso significa que eles só podem levar alguns valores discretos.
Agora, os orbitais são preenchidos com elétrons de energia inferior a maior, seguindo certas regras que determinam a configuração eletrônica.
Dessa forma, o número de elétrons nos orbitais ou mais níveis externos de um átomo estabelece os links que ele pode formar com outros átomos para formar moléculas. Este número depende da configuração eletrônica e do número atômico.
 Fonte: Usuário: MaterialScientist, CC0, via Wikimedia Commons
Fonte: Usuário: MaterialScientist, CC0, via Wikimedia Commons Números quânticos
A energia de um elétron no átomo é determinada por seu número quântico principal n, que pode levar valores inteiros 1, 2, 3 ..
O momento angular do elétron no átomo é determinado pelo número quântico secundário eu (Carta Ele) e seus valores dependem de n.
Por exemplo, para n = 2 o número quântico secundário leva os valores de 0 a N-1, ou seja: 0 e 1. Da mesma forma, para n = 1 que é o menor nível de energia, o número quântico secundário L só leva o valor 0.
Números quânticos secundários 0, 1, 2, 3 são alternadamente denotados com letras S, P, D e F. Os orbitais S são esféricos e os orbitais p são lobados.
Existem mais dois números quânticos:
- O número quântico magnético ml, Isso leva os valores de -l a +l passando por zero.
- O número quântico de rotação s, Isso leva apenas valores+½ e -½ e é uma característica do elétron.
Finalmente é o princípio de exclusão de Pauli, que afirma que dois elétrons não podem ter os quatro números quânticos idênticos. Como conseqüência desse princípio, um orbital pode ter no máximo dois elétrons com o giro oposto.
Diagrama de configuração eletrônica
O diagrama de configuração eletrônico serve para conhecer a ordem de preenchimento de elétrons dos orbitais de energia menor até a energia mais alta, uma vez que o número atômico de um elemento químico é conhecido. A Figura 4 mostra este diagrama:
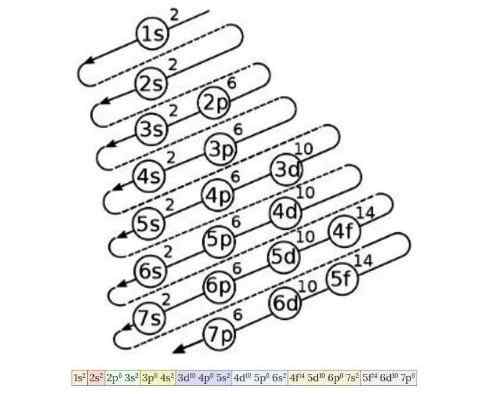 Figura 4. Configuração eletronica. Fonte: Wikimedia Commons.
Figura 4. Configuração eletronica. Fonte: Wikimedia Commons. A idéia esquematizada existe a seguinte: a primeira edição indica o número quântico principal, então a letra indica o número quântico secundário e, finalmente, o número da pesquisa indica o máximo de elétrons possíveis nesse orbital.
Exemplo
Configuração eletrônica de carbono e silício
Conforme indicado acima, o carbono tem um número atômico 6, o que significa que possui 6 elétrons que são distribuídos da seguinte forma: 1S2 2S2 2P2. Por sua vez, o silício tem o número 14 atômico e seus elétrons são distribuídos nesta outra forma: 1S2 2S2 2P6 3S2 3P2.
Ambos os elementos estão na mesma coluna da tabela periódica, porque, mesmo que tenham números atômicos diferentes, eles têm a mesma configuração eletrônica no mais orbital externo.
Referências
- Connor, n. O que é núcleo - estrutura do núcleo atômico - Definição. Recuperado de: periódico-rabo.org.
- Povos da cúpula. Número atômico: o que é, como é representado. Recuperado de: Summit.org
- Lifeder. O que é periodicidade química? Recuperado de: Lifer.com
- Wikipedia. Configuração eletronica. Recuperado de: é.Wikipedia.com
- Wikipedia. Número atômico. Recuperado de: é.Wikipedia.com

