Modelo atômico de Dalton

- 3617
- 810
- Melvin Mueller
Explicamos o modelo atômico de Dalton, seus postulados e limitações
 O modelo atômico de Dalton foi o primeiro a ser baseado em pesquisas científicas. Fonte: f. Zapata.
O modelo atômico de Dalton foi o primeiro a ser baseado em pesquisas científicas. Fonte: f. Zapata. Qual é o modelo atômico de Dalton?
Ele Modelo atômico de Dalton Ele propõe que toda a matéria seja composta de unidades minúsculas e indivisíveis, chamadas átomos, retomando as idéias que ex -pensadores gregos haviam formulado dois mil anos atrás.
É o primeiro modelo atômico que emergiu de uma experimentação cuidadosa em laboratório, porque, embora a humanidade sempre tenha tentado entender o que é o assunto, até o início do século XIX, as possibilidades de verificar experimentalmente as teorias ainda eram limitadas.
No entanto, além de ser um bom observador da natureza, o professor de inglês John Dalton (1766-1844), também se destacou no campo da instrumentação, porque criou vários dispositivos de medição, que mais tarde usaria em seu laboratório para o estudo do estudo do gases.
Assim, Dalton percebeu que as substâncias são combinadas seguindo certas regras e, para explicar, postulou que toda a matéria era composta de átomos, pequenas esferas homogêneas e falta de estrutura interna. Os átomos, disse ele, formam compostos seguindo certas proporções e, durante uma reação química, eles se separam e se combinam novamente, criando novos compostos.
Dalton não apenas desenvolveu o primeiro modelo atômico baseado em experimentação rigorosa. Ele também criou um sistema de nomenclatura para os elementos, ordenou -os para seu peso atômico, estabeleceu a lei de múltiplas proporções, a lei das pressões parciais e descreveu a cegueira a certas cores, uma condição que ele próprio sofreu, chamado daltonismo.
Suas extensas contribuições para a ciência ganharam inúmeras distinções ao longo de sua carreira científica, mas Dalton sempre viveu de uma maneira modesta e simples, dedicada à ciência até o final de seus dias.
Breve história
Desde os tempos remotos, a humanidade procurou uma explicação sobre a natureza da matéria. Pensadores gregos do século V.C, e antes que eles, alguns filósofos hindus, postularam que o assunto era constituído por unidades elementares chamadas átomos. No entanto, eles não tinham o apoio experimental necessário para verificar suas teorias.
Pode atendê -lo: quais são as propriedades térmicas e o que são? (Com exemplos)O primeiro modelo atômico é atribuído a Leucipo e seu discípulo de Demócrito de Abdera (460 a. C. - 370 a. C.). Desde o primeiro pouco, é conhecido, mas o Demócrito era um sábio de grande renomado, comparável a Platão e Aristóteles, embora alguns fragmentos de seu trabalho sejam mal preservados.
Demócrito concebeu o átomo como a partícula final que forma a matéria, indivisível e indestrutível. De acordo com suas teorias, toda a matéria era composta por essas partículas, muito pequenas para serem vistas. E de acordo com a maneira de combinar, os átomos forneceram ao sujeito suas propriedades características.
Em contraste com isso, depois de comentar. As idéias contínuas de Aristóteles finalmente prevaleceram até o início do século 19.
Obras de Dalton
Em 1793, John Dalton estava interessado em meteorologia e passou a trabalhar no estudo de gases atmosféricos e suas propriedades. Graças a seus experimentos, ele percebeu que elementos como oxigênio, sempre combinados em uma certa proporção, dada por um número inteiro.
Em 1803, Dalton explicou que essas proporções são devidas ao fato de que o assunto é composto por partículas básicas, chamadas átomos, como o Democrito disse há muito tempo. Ele apresentou sua proposta no trabalho "Novo sistema de filosofia química", na qual descreveu os resultados de seus experimentos.
Além disso, nesse trabalho também incluiu símbolos especiais para representar os átomos individuais de cada elemento, colocando assim os fundamentos da química moderna.
Pode servir a você: sons agudos: características e exemplosExplicação do modelo atômico de Dalton
Durante la época en que Dalton desarrolló su trabajo, otros científicos ya habían descubierto algunas de las leyes que rigen la materia y las combinaciones entre los elementos: Antoine Lavoisier estableció que, durante una reacción química, la masa no se crea o destruye, sino que torna-se.
Esta lei foi seguida pela lei de Proust sobre as proporções definidas, estabelecendo que, quando dois elementos são combinados, eles sempre o fazem em proporções fixas.
Agora, uma parte dos experimentos de Dalton consistia em estudar a absorção da água na água. Lá ele observou que um certo volume de água só poderia absorver certa quantidade de gás e que essa quantidade variou de acordo com o gás. Além disso, o gás pode ser recuperado da água, mantendo suas propriedades intactas.
Ele também descobriu que, quando dois elementos podem ser combinados para originar mais de um composto, a quantidade de cada um permanece fixo e mantendo um relacionamento numérico simples, por exemplo 1: 1, 1: 2; 2: 3 e assim por diante. Esta é a chamada Lei de múltiplas proporções.
Para explicar esses fatos, Dalton argumentou que o gás, a água e, em geral, tudo isso consiste em peças básicas, que, quando combinadas, dão origem a diferentes compostos. Cada elemento consiste em partículas distintas (Dalton não os chamou de átomos no início), mas mesmo em combinação, essas partículas mantêm suas qualidades inalteradas.
O modelo atômico de Dalton postula
O modelo atômico de Dalton está resumido nas seguintes declarações:
1. A matéria é constituída por pequenas partículas indivisíveis chamadas átomos.
2. Cada elemento consiste em átomos idênticos entre si e com propriedades iguais. Os átomos de um elemento diferem dos de outros.
3. Ao se juntar a dois ou mais átomos de diferentes elementos, eles o fazem em certas e simples proporções, criando assim os compostos, formados por moléculas. As moléculas de um determinado composto são idênticas entre si.
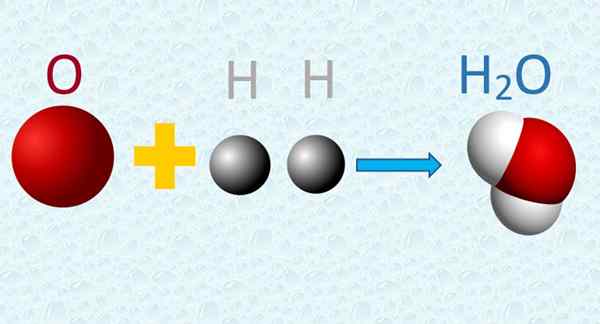 Em uma molécula de água, os átomos de oxigênio e hidrogênio são combinados em proporções simples. Fonte: f. Zapata.
Em uma molécula de água, os átomos de oxigênio e hidrogênio são combinados em proporções simples. Fonte: f. Zapata. 4. Durante uma reação química, os átomos são trocados, mas não sofrem nenhuma transformação, nem são criados ou destruídos no processo.
Falhas do modelo de Dalton
A pesquisa científica experimentou um boom notável durante o século XIX, promovido pela Revolução Industrial. E as principais falhas do modelo atômico de Dalton não foram reveladas:
Pode atendê -lo: tensão interfacial: definição, equação, unidades e medição1. O átomo não é indivisível
Esta é uma das falhas mais importantes do modelo atômico de Dalton. Os experimentos realizados durante os séculos XIX e XX mostraram que o átomo é composto de uma infinidade de partículas subatômicas.
O primeiro a se conhecer foi o elétron e o próton, e depois foi aprendido sobre a existência do nêutron. Então, tanto o próton quanto o nêutron revelaram sua estrutura interna.
2. Átomos do mesmo elemento podem não ser idênticos
Os elementos têm isótopos que, embora tenham as mesmas propriedades químicas, diferem no número de nêutrons, de modo que seu peso atômico é diferente. Por exemplo, os isótopos de hidrogênio são protio, deutério e trítio.
3. Os átomos não são invariáveis
Existem substâncias radioativas que emitem partículas e energia, transformando -se em outros elementos.
4. Os átomos nem sempre combinam em proporções inteiras
Está provado que existem compostos orgânicos e mais complexos, que não seguem exatamente a lei de proporções múltiplas de Dalton.
Artigos de interesse
Modelo Atômico de Schrödinger.
Modelo Atômico de Broglie.
Modelo Atômico de Chadwick.
Modelo Atômico de Heisenberg.
Modelo atômico de perrina.
Modelo Atômico de Thomson.
Modelo Atômico Dirac Jordan.
Modelo Atômico do Demócrito.
Modelo Atômico de Leucipo.
Modelo atômico Bohr.
Modelo Atômico de Rutherford.
Modelo atômico atual.

