Metais
- 1467
- 33
- Conrad Schmidt
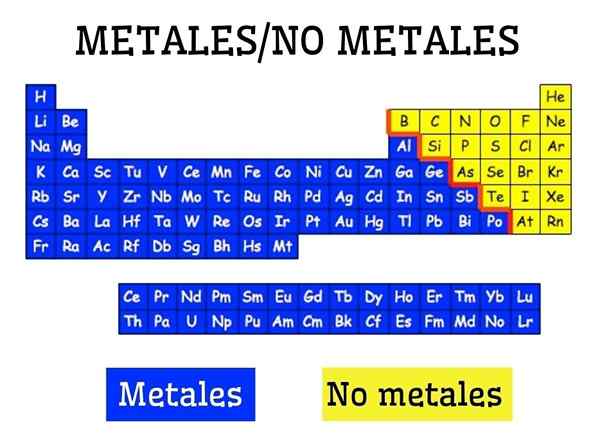
 Metais e não -metais na tabela periódica dos elementos
Metais e não -metais na tabela periódica dos elementos O que são metais?
Os metais são formados por um grupo de elementos localizados no lado esquerdo, com exceção do hidrogênio não -metal, da tabela periódica. Os metais constituem cerca de 75 % dos elementos químicos, para que possa ser afirmado que grande parte da natureza é metálica.
Os metais que o homem processou inicialmente na pré -história foram os seguintes: ouro, prata, cobre, lata, chumbo e ferro. Isso ocorreu devido ao fato de serem nativos ou à facilidade de seu processamento para executar objetos de utilidade.
Parece uma questão de mágica que muitas rochas e minerais podem ser extraídos corpos lustrosos e prateados (com certas exceções importantes e notáveis). Esse é o caso de bauxita e alumínio, cujo argila argila esse metal reduzido em placas ou papéis de prata é obtido.
Os metais são a estrutura das indústrias; Sua fiação, reatores, unidades, recipientes, tudo de uma maneira ou de outra são compostos de metais e suas ligas.
Com metais, as primeiras moedas, armas, ferramentas, armaduras foram feitas e depois usadas em fabricantes de veículos, bicicletas, navios, aviões, computadores, entre outros objetos indispensáveis na vida moderna.
História
Idade de cobre
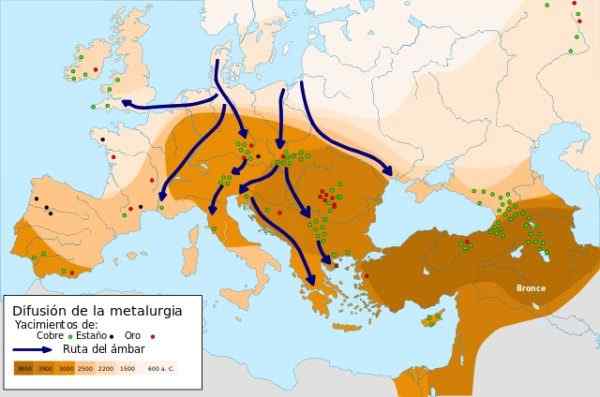 Expansão de metalurgia - Fonte: Difusão metalúrgica.SVG sob o Creative Commons Attribution-Compartyrigue 4 Licença 4.0 Internacional
Expansão de metalurgia - Fonte: Difusão metalúrgica.SVG sob o Creative Commons Attribution-Compartyrigue 4 Licença 4.0 Internacional Em 9000 a.C. Os primeiros objetos metálicos de cobre forjados no Oriente Próximo foram elaborados, quando o homem descobriu que, quando o cobre estava martelando, ele aumentou sua força e resistência, usando -o para a fabricação de facas. Esta é a idade do cobre.
Descobriu-se que o cobre poderia ser obtido através do aquecimento de minerais azuis, como o Corvellita e a malaquita (4000-3000 para.C.).
O período calcolítico é um período de tempo que precede a Idade do Bronze, correspondendo a 5000-3000 a.C. O homem começou a experimentar a fusão e a fundição do cobre, para obter cobre forjado de óxido de cobre.
Idade do Bronze (3000-1500 A.C.)
 Materiais da Idade do Bronze - Fonte: Gaguilella sob o Creative Commons Attribution -Shareigual 4 Licença 4.0 Internacional.
Materiais da Idade do Bronze - Fonte: Gaguilella sob o Creative Commons Attribution -Shareigual 4 Licença 4.0 Internacional. O homem iniciou acidentalmente a elaboração de ligas, inicialmente de cobre e arsênico, e depois com cobre e estanho para obter bronze no Oriente Próximo.
Os artigos de bronze, correspondentes a esse tempo, tinham 87 % de cobre, 11 % de lata e pequenas quantidades de ferro, arsênico, níquel, chumbo e antimônio.
Idade do Ferro (700 A.C.)
O homem usou sua experiência na produção de cobre forjado para a produção de ferro forjado no Oriente Próximo. Nesse mesmo período de tempo, houve a granulação de Etrusco Dust, Itália.
A primeira produção de aço conhecida, uma liga de ferro e carbono, se manifestou em peças de metal em um sítio arqueológico na Anatólia (1800 para.C.)
Pode servir a você: gravimetria: análise gravimétrica, métodos, usos e exemplosEm direção a 1122 d.C., Em uma data e local desconhecidos, o ferro fundido é introduzido. Em 1440 d.C. O grande sino de Pequim é produzido, China. Quase três séculos depois, em 1709 d.C., O ferro fundido é produzido usando Coca -Cola como material combustível.
Em 1779, o ferro fundido na Inglaterra foi usado como material arquitetônico. Em 1855, Henry Bessenir usou o Arrabio como matéria -prima para obter aço macio. A patente inglesa de Clark and Wood (1872), uma liga, atualmente considerada como aço inoxidável.
Propriedades físicas de metais
 O bronze desses sinos antigos demonstra a utilidade dos metais para fins ornamentais ou religiosos. Fonte: pxhere.
O bronze desses sinos antigos demonstra a utilidade dos metais para fins ornamentais ou religiosos. Fonte: pxhere. Entre algumas propriedades físicas de metais, temos:
-Os metais são brilhantes e são capazes de refletir a luz.
-Em geral, eles são bons condutores de eletricidade e calor.
-Eles têm altos pontos de fusão e ebulição.
-Eles são maleáveis, ou seja, podem ser martelados para produzir lençóis baixos grossos.

-Eles são dúcteis, com eles, você pode fabricar fios ou fibras de muito pouco diâmetro.
-Eles são apresentados em um estado sólido, com exceção do mercúrio que à temperatura ambiente está em estado líquido, e o gálio, que derrete apenas apertando as mãos nas mãos. Na imagem a seguir, você pode ver um recipiente de mercúrio:

-Eles são corpos opacos, seus folhas finas não são atravessadas pela luz.
-Eles têm muita dureza, exceto por sódio e potássio que podem ser cortados por uma faca.
-Eles têm uma alta densidade, sendo o ósmio e irídio do mais alto, e o lítio da menor densidade.
Propriedades químicas de metais
Entre algumas das propriedades químicas dos metais que temos:
-Eles tendem a perder elétrons e formar cátions de metal, Mn+, onde n indica seu número de oxidação, que apenas para metais alcalinos e alcalistas coincide com seu número de valência.
-Suas eletronegatividades são baixas.
-Eles correm e sofrem de dano de oxidação.
-Eles formam óxidos básicos ao reagir com oxigênio. Esses óxidos quando combinados com água formam hidróxidos de metal. Os óxidos de metal reagem com ácidos para formar sais e água.
-Eles são bons agentes redutores, pois produzem seus elétrons.
Tipos de metais
Os metais são classificados como os seguintes: Alcalina, julgamento alcalino, pós-transição, transitória e chamada terras raras.
Metais alcalinos

Eles geralmente não se vêem de natureza livre porque oxidam facilmente. Tem um suborbital s1 Em sua camada orbital externa, para que eles tenham um estado de oxidação +1. São metais que reagem exotermicamente com água e estão reduzindo fortemente.
Metais alcalinos-térreos
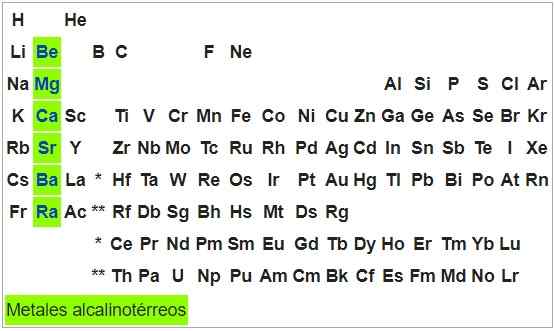
Eles são metais maleáveis e dúcteis. Os átomos dos elementos deste grupo têm uma configuração S2, Para que eles possam produzir dois elétrons e seu status de oxidação é +2. Com exceção do berílio, eles são oxidáveis para a exposição ao ar.
Pode atendê -lo: amurotopes de carbonoMetais pós -transitórios
Eles são metais do bloco P SO -chamado, localizado entre metais de transição e metalóides na tabela periódica.
Os elementos do grupo 3 têm estados de oxidação +1 e +3 como os mais comuns, embora o alumínio apresente apenas o estado de oxidação +3. Também faz parte dos metais pós -transitórios localizados nos grupos 14 e 15.
Metais de transição d
Eles formam um grupo entre os elementos da base e os formadores de ácido. Os orbitais atômicos d e f estão incompletos e estão sendo preenchidos. Embora o termo metais de transição se referam a metais de transição D.
Os metais de transição têm mais de um estado de oxidação. Eles têm pontos de fusão e ebulição mais altos do que outros grupos de metal. A transição metais é um grupo metálico muito heterogêneo que inclui, entre outros, ferro, cromo, prata, etc.
Terra rara
 Mineral de terras raras
Mineral de terras raras Este grupo de metais é composto pelos elementos Scandio e Ititrio e os elementos da série de Lantanides e Actinids. O termo 'Terra Rara' refere -se ao fato de que eles não são encontrados na natureza em estados puros e são apegáveis por ácidos.
Usos/aplicações de metais
Metais alcalinos
O lítio é usado como uma transferência de calor significa em alguns reatores nucleares. É usado em algumas baterias secas e acumuladores de pouco peso. O brometo de cloreto e lítio são compostos higroscópicos que são usados em processos de secagem e ar condicionado industriais.
O sódio é usado na metalurgia metal, como titânio e zircônio. É usado na iluminação pública em lâmpadas de arco de sódio. O cloreto de sódio (NaCl) é usado como sabor de alimento e preservação de carne.
Metais alcalinéticos
O magnésio foi usado na fotografia como luz flash e fogos de artifício. O bário é um componente de ligas usadas em velas de ignição devido à facilidade do elemento para emitir elétrons. Os sais de bário são usados para limitar os danos causados por raios X em placas do trato gastrointestinal.
O cálcio é usado para eliminar as impurezas dissolvidas em metais fundidos e na eliminação de gases residuais em tubos de vácuo. Faz parte do gesso, material usado na construção e no tratamento de fraturas ósseas.
Metais pós -transitórios
Alumínio porque é um metal leve é usado na construção de aviões e navios. Também é usado na elaboração de vários utensílios de cozinha. É usado como matéria -prima na fabricação de desodorantes que limitam a transpiração.
Pode atendê -lo: soluções percentuaisO gálio é usado em transistores e termômetros para altas temperaturas. O isótopo 67GA é usado em medicina no tratamento de alguns melanomas. O chumbo é usado na construção de baterias e na proteção contra a radiação ionizante.
Metais de transição
O cobre é usado em tubos de abastecimento de água, em geladeiras e sistemas de ar condicionado. Também é usado como parte do mecanismo de dissipação de calor dos computadores. É usado na condução da corrente elétrica, em eletromagnets e na coloração do vidro.
O níquel é usado na elaboração do aço inoxidável, bem como em cordas de guitarra e baterias recarregáveis. Também é usado em galvanoplastia em proteção de metal. É usado em ligas encontradas em partes de veículos, como válvulas, rolamentos e freios.
O níquel tem sido usado há muito tempo na elaboração de moedas.
O zinco é usado na proteção de metais de corrosão, na produção de latão. Óxido de zinco e sulfato de zinco são usados na fabricação de placas usadas em telhados, sarjetas e calhas.
O cromo é usado na proteção de corrosão de metal e os suprimentos brilham. É usado como um catalisador na reação de síntese de amônia (NH3). O óxido de cromo é usado na proteção de madeira.
Terra rara
O Scandio é usado no alumínio de alumínio para componentes aeroespaciais. É um aditivo em lâmpadas de vapor de mercúrio.
O Lantano é usado em alta refração e vidro resistente a álcalis. Além disso, é usado na fabricação de lentes de câmeras e como um catalisador catalítico fluidos para refinarias de petróleo.
Cerio é usado como um agente químico. Além disso, é usado para o fornecimento de uma coloração de vidro amarelo e cerâmica, bem como catalisador para fornos auto -empregados.
Exemplos de elementos de metal
Alcalino
Sódio (Na), potássio (K), Cesio (CS), Lítio (Li) e Rubidium (RU).
Terreros alcalinos
Beryllium (BE), magnésio (mg), cálcio (CA), estrôncio (MR), bário (BA) e rádio (RA).
Pós -transição
Alumínio (Al), Gálio (GA), Indiano (IN), Talio (TL), TIN (SN) e chumbo (PB).
Transitório
Titânio (Ti), vanádio (V), cromo (CR), manganês (Mn), ferro (fé), cobalto (CO), níquel (Ni), cobre (CUINC), zinco (Zn), zircônio (ZR), Niobio (NB), Molibdênio (MO), Paladio (PD), Prata (AG), Volframium (W), Renio (Re), Osmio (OS), Iridido (IR),
Platina (Pt), Ouro (Au) e Mercúrio (HG).
Terra rara
Scandio (SC), Itrio (Y), Lantano (LA), Cerio (CE), Praseodimio (PR), Neodímio (ND), Samário (SM), Europio (EU), Gadolinio (GD), Holmio (HO), Erbio (ER), Tulio (TM), Iterbio (YB) e Luthacio (LU).
Referências
- Whitten, Davis, Peck e Stanley. (2008). Química. (8ª ed.). Cengage Learning.
- Shiver & Atkins. (2008). Química Inorgânica. (Quarta edição). Mc Graw Hill.
- Helmestine, Anne Marie, Ph.D. (5 de outubro de 2019). Metais versus não metais. Recuperado de: pensamento.com
- Metais e suas propriedades-físicas e químicas. [PDF]. Recuperado de: csun.Edu
- Jonathan Mestre. (2019). 18 tipos diferentes de metal (fatos e usos). Recuperado de: makeitfrometal.com

