Estrutura de hidreto de magnésio, propriedades e usos
- 1923
- 123
- Pete Wuckert
Ele Hidreto de magnésio (MGH2 de fórmula molecular), é um composto químico com o teor de peso de hidrogênio de um 7.66%, e encontrado na natureza como um sólido cristalino branco. É usado principalmente para preparar outras substâncias químicas, embora também tenha sido estudado como um potencial de armazenamento médio para hidrogênio.
Pertence à família de hidratantes salinos (ou iônicos), aqueles definidos por um íon carregado negativamente. Esses hidretos são considerados aqueles que são formados a partir de metais alcalinos e metais alcalinos aterrorizantes, mas no caso de magnésio (e berílio), eles têm sindicatos covalentes, além daqueles iônicos que caracterizam essa família de hidros.
 Modelo de célula de hidreto de magnésio unitário, MGH2.
Modelo de célula de hidreto de magnésio unitário, MGH2. [TOC]
Preparação e fórmula
O hidreto de magnésio é formado através da hidrogenação direta do magnésio metálico (mg) em condições de alta pressão e temperatura (200 atmosferas, 500 ° C) com um catalisador MGI2. Sua reação é equivalente a:
Mg+h2→ MGH2
A produção de MGH também foi investigada2 Em temperaturas mais baixas com o uso de magnésio nanocristalino produzido em moinhos de bolas.
Existem também outros métodos de preparação, mas eles representam reações químicas mais complexas (hidrogenação do magnésio-antraceno; a reação entre dietilmagnésio com hidreto de lítio-alumínio; e como um produto de um complexo MGH2).
Estrutura química
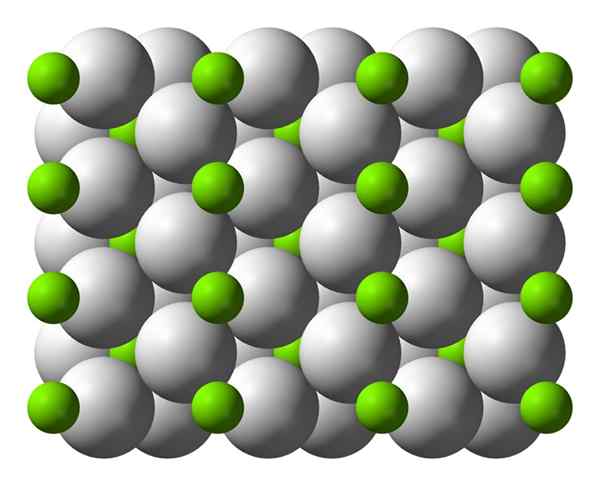
 Estrutura cristalina do hidreto de magnésio
Estrutura cristalina do hidreto de magnésio Este átomo tem uma estrutura rutilo à temperatura ambiente, com uma estrutura cristalina tetragonal. Possui pelo menos quatro formas diferentes em condições de alta pressão, e uma estrutura não cente foi observada com deficiências de hidrogênio; O último é apresentado apenas em quantidades muito pequenas de partículas ao formar.
Como mencionado acima, os links que existem na estrutura de Rutilo têm propriedades parcialmente covalentes em vez de serem puramente iônicas, como outros hidros salinos.
Isso causa o átomo de magnésio possui uma forma esférica e totalmente ionizada, mas que seu íon hidreto é uma estrutura alongada.
Propriedades do hidreto de magnésio
Propriedades físicas
- Aparência: Cristais brancos.
- Missa molar: 26.3209 g/mol
- Densidade: 1.45 g/cm3
- Ponto de fusão: 285 ° C é quebrado
- Solubilidade: Na água, ele quebra.
Este composto químico tem um peso molecular de 26.321 g/mol, uma densidade de 1.45 g/cm³ e tem um ponto de fusão de 327 ºC.
Propriedades quimicas
- Precursor para a fabricação de outros produtos químicos.
- Armazenamento de hidrogênio, como uma possível fonte de energia.
- Agente redutor na síntese orgânica.
É importante indicar que esse composto não pode ser trazido para um estado líquido e, quando tomado ou seu ponto de fusão ou introduzido na água, decompõe -se. Este hidreto é insolúvel em éter.
É uma substância altamente reativa e extremamente inflamável, e também é pirofórica, ou seja, pode ser inflamada espontaneamente no ar. Essas três condições representam riscos de segurança que serão mencionados na última seção deste artigo.
Usa/aplicações
Armazenamento de hidrogênio
O hidreto de magnésio reage facilmente com a água para formar gás hidrogênio, através da seguinte reação química:
MGH2+2h2O → 2h2+Mg (oh)2
Além disso, esta substância se decompõe à temperatura de 287 ºC e 1 barra de pressão, como segue:
MGH2→ mg+h2
Portanto, o uso de hidreto de magnésio como um meios de armazenamento de hidrogênio para seu uso e transporte foi proposto.
A hidrogenação e a desidrogenação de uma quantidade de magnésio metálico é levantada como forma de transporte.
Reações de hidrogenação e desidrogenação
Embora a temperatura de decomposição do hidreto de magnésio represente uma limitação de uso, foram levantados métodos para melhorar a cinética das reações de hidrogenação e desidrogenação. Um deles é com a redução do tamanho da partícula de magnésio com o uso de moinhos de bolas.
Pode atendê -lo: sistema não homogêneoLama
Além disso, foi levantado um sistema que produz um hidreto de magnésio em forma de lama (mais gerenciável e certamente o de poeira ou outras partículas sólidas), que seriam reagidas com água para obter o hidrogênio desejado.
Estima -se que a lama previamente nomeada seja formada por um hidreto finamente moído, protegido com uma camada de proteção contra petróleo e suspenso em agentes de dispersão para garantir que ele mantenha sua consistência sem perda de material e que não absorve a umidade do ambiente.
Essa lama tem a vantagem de ser bombeada através de qualquer diesel comum, gasolina ou bomba de água, tornando esta proposta econômica além de eficiente.
Células de combustível
O hidreto de magnésio pode ser implementado na produção de células de combustível avançado e também na criação de baterias e armazenamento de energia.
Transporte e energia
Durante as últimas décadas, o uso de hidrogênio foi considerado como fonte de energia. A implementação do hidrogênio como combustível requer encontrar sistemas de armazenamento seguro e reversível e com altas capacidades volumétricas (quantidade de hidrogênio por unidade de volume) e gravimétrico (quantidade de hidrogênio por unidade de massa).
Alquilação
Alco3R) de compostos orgânicos em meio básico, onde há presença de grupos -OH em baixas concentrações e temperaturas mais altas que o ponto de fusão do hidreto.
Nesse caso, os hidrogênios presentes no hidreto de magnésio (MGH2), Eles se juntam aos grupos -oh formando água. O magnésio livre pode receber o halogênio que geralmente acompanha a molécula alquilica que se destina a unir a cadeia de hidrocarbonetos.
Riscos
Reação da água
Como já mencionado, o hidreto de magnésio é uma substância que reage com muita facilidade e violência com a água, apresentando a capacidade de explorar em grandes concentrações.
Pode atendê -lo: sais básicos: fórmula, propriedades, nomenclatura, exemplosIsso ocorre porque sua reação exotérmica gera calor suficiente para acender o gás de hidrogênio liberado na reação de decomposição, levando a uma reação em cadeia bastante perigosa.
É pirofórico
O hidreto de magnésio também é pirofórico, o que significa que ele pode ativar chamas espontaneamente na presença de ar úmido e formar óxido de magnésio e água.
Sua inalação em estado sólido ou contato com seus vapores não é recomendado: a substância no estado natural e seus produtos de decomposição podem causar ferimentos graves ou até morte.
Pode gerar soluções corrosivas em contato com a água e a contaminação dele. O contato com a pele e os olhos não é recomendado e também gera irritação nas membranas mucosas.
Não foi demonstrado que o hidreto de magnésio pode gerar efeitos crônicos à saúde, como câncer, defeitos reprodutivos ou outras consequências físicas ou mentais, mas o uso de equipamentos de proteção ao manipular é recomendado (especialmente respiradores ou máscaras, por seu caráter de pó fino).
Ao trabalhar com essa substância, a umidade do ar em níveis baixos deve ser mantida, desligue todas as fontes de ignição e transportam -a em tambores ou outros contêineres.
Você sempre deve evitar trabalhar com grandes concentrações dessa substância quando ela pode ser evitada, uma vez que a possibilidade de uma explosão diminui significativamente.
Se um derramamento de hidreto de magnésio for apresentado, a área de trabalho deverá ser isolada e a poeira com uma ferramenta de vácuo deve ser isolada. Você nunca deve usar o método de varredura seco; aumenta as possibilidades de alguma reação com hidreto.
Referências
- Zumdahl, s. S. (1998). Enciclopédia Britannica. Tirado de Britannica.com.
- PubChem. (2005). Banco de dados de química aberta pubchem. Retirado de PubChem.NCBI.Nlm.NIH.Gov.
- Hidrogênio seguro, L. (2006). Congresso de carro verde. Retirado de GreencarConress.com.
- Produtos químicos, c. (n.d.). Cameo Chemicals. Retirado de cenários.NOAA.Gov.
- Serviços, n. J. (1987). Departamento de Saúde de Nova Jersey e Serviços Sênior. Tirado de NJ.Gov.
- « Nascimento do rio amarelo, turnê, boca, flora
- Descolonização na história da Ásia, causas e consequências »

