Propriedades de hidrocarbonetos alifáticos, nomenclatura, reações, tipos

- 3111
- 276
- Pete Wuckert
O Hidrocarbonetos alifáticos Eles são todos aqueles que não têm aromaticidade, não em um sentido olfativo, mas em relação à estabilidade química. Classificar hidrocarbonetos dessa maneira é hoje muito ambíguo e impreciso, pois não discrimina entre vários tipos de hidrocarbonetos que não são aromáticos.
Assim, temos hidrocarbonetos alifáticos e hidrocarbonetos aromáticos. Estes últimos são reconhecidos por sua unidade básica: o anel Benncénico. Os outros, por outro lado, podem adotar qualquer estrutura molecular: linear, ramificada, cíclica, insaturada, policiclica; Contanto que eles não tenham sistemas conjugados, como o benzeno.
 O combustível fluido dos isqueiros consiste em uma mistura de hidrocarbonetos alifáticos. Fonte: Pixnio.
O combustível fluido dos isqueiros consiste em uma mistura de hidrocarbonetos alifáticos. Fonte: Pixnio. O termo 'aliphatic' nasceu da palavra grega 'Aleiphar', que significa gordura, também usada para se referir aos óleos. Portanto, no século XIX, essa classificação foi atribuída aos hidrocarbonetos obtidos dos extratos oleosos; Enquanto hidrocarbonetos aromáticos foram extraídos de árvores e resinas perfumadas.
No entanto, como a base da química orgânica consolidada, descobriu -se que havia uma propriedade química que diferenciava hidrocarbonetos, ainda mais importantes do que suas fontes naturais: aromaticidade (e não fragrância).
Dessa maneira, hidrocarbonetos alifáticos deixaram de ser apenas aqueles obtidos de gorduras, para ser todos aqueles que não possuem aromaticidade. Dentro desta família, temos alcenos e alcinos, independentemente de serem lineares ou cíclicos. É por isso que 'alifático' é considerado impreciso; Embora seja útil para abordar alguns aspectos gerais.
Por exemplo, quando é dito 'extremos' ou 'correntes' alifáticas, as regiões moleculares são aludidas a onde anéis aromáticos estão ausentes. De todos os hidrocarbonetos alifáticos, o mais simples por definição é metano, CHO4; Enquanto o benzeno é o mais simples dos hidrocarbonetos aromáticos.
[TOC]
Propriedades de hidrocarbonetos alifáticos
As propriedades dos hidrocarbonetos alifáticos oscilam em diferentes graus, dependendo de quais são considerados. Existem massas moleculares baixas e altas, bem como lineares, ramificadas, cíclicas ou policiclicais, mesmo as de estruturas tridimensionais incríveis; Como no cubano, na forma de um cubo.
No entanto, existem algumas generalidades que podem ser mencionadas. A maioria dos hidrocarbonetos alifáticos são gases ou líquidos hidrofóbicos e apolares, tendo um pouco mais apolar do que outros, uma vez que mesmo aqueles em cujas cadeias de carbono têm halogênio, oxigênio, nitrogênio ou átomos de enxofre são incluídos na lista.
Pode atendê -lo: boro: história, propriedades, estrutura, usosEles também são compostos inflamáveis, pois são suscetíveis a oxidação no ar antes de uma fonte de calor mínima. Esse recurso se torna mais perigoso se adicionarmos sua alta volatilidade, devido às fracas interações dispersivas que mantêm moléculas alifáticas coesas coesas.
Por exemplo, vemos isso no butano, um gás que pode ser liquefeito com relativa facilidade e propano. Ambos são muito voláteis e inflamáveis, por isso são componentes ativos de gás de cozinha ou isqueiros de bolso.
Obviamente, essa volatilidade tende a diminuir à medida que a massa molecular e o hidrocarboneto causa mais e mais líquidos viscosos.
Nomenclatura
A nomenclatura de hidrocarbonetos difere ainda mais do que suas propriedades. Se eles são alko ou alcinos, os mesmos padrões estipulados pelo IUPAC são seguidos: selecione a cadeia mais longa, atribuindo os indicadores mais baixos à extremidade mais substituída ou aos heteroatomos ou mais grupos reativos.
Dessa forma, você sabe em que carbono cada substituinte é encontrado, ou mesmo insatação (links duplos ou triplos). No caso de hidrocarbonetos cíclicos, o nome é precedido pelos substituintes listados em ordem alfabética, seguida pela palavra 'ciclo', contando os números de carbono que o integram.
Por exemplo, considere os dois ciclohexanos a seguir:
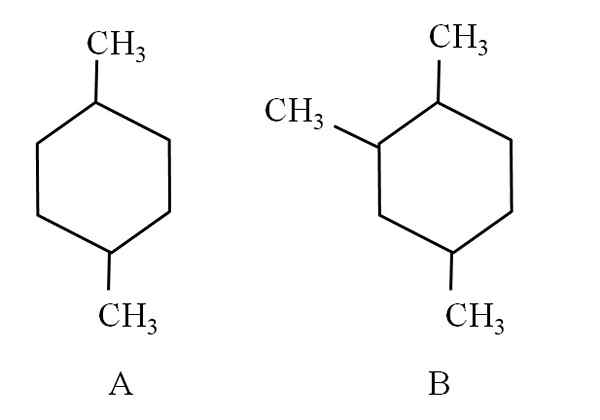 Dois ciclohexanos, que são classificados como hidrocarbonetos alifáticos. Fonte: Gabriel Bolívar.
Dois ciclohexanos, que são classificados como hidrocarbonetos alifáticos. Fonte: Gabriel Bolívar. Cyclohexan A, é chamado 1,4-dimetilciclohexano. Se o anel fosse cinco carbonos, seria 1,4-dimetilciclopentano. Enquanto isso, o ciclohexano B é chamado 1,2,4-trimetilciclohexano, e não 1,4,6-ciclohexana, pois procura usar os indicadores mais baixos.
Agora, a nomenclatura pode se tornar muito complicada para estruturas operabóticas hidrocarbonetos. Para eles, existem regras mais específicas, que devem ser explicadas separadamente e cuidadosamente; Como nos objetivos, terpenos, políticas e compostos policíclicos.
Reações
Combustão
Felizmente, as reações são menos variadas para esses hidrocarbonetos. Um deles já foi mencionado: eles facilmente combustam, produzindo dióxido de carbono e água, além de outros óxidos ou gases, dependendo da presença de heteroatômicos (Cl, N, P, O, etc.). No entanto, o CO2 e h2Ou são os principais produtos de combustão.
Adição
Se eles tiverem insaturação, podem sofrer reações adicionais; Ou seja, eles incorporam pequenas moléculas em seu esqueleto como substituintes seguindo um mecanismo específico. Entre essas moléculas, temos a de água, hidrogênio e halogênios (f2, Cl2, Br2 e eu2).
Halogenação
Por outro lado, hidrocarbonetos alifáticos sob a incidência de radiação ultravioleta (Hv) e o calor pode quebrar os links C-H para alterá-los por links C-X (C-F, C-Cl, etc.). Esta é a reação de halogenação, que é observada em alcanos de cadeia muito curta, como metano ou pentan.
Pode atendê -lo: nitritos: propriedades, estrutura, nomenclatura, formaçãoCraqueo
Outra reação que os hidrocarbonetos alifáticos podem sofrer, especialmente os alcanos de cadeia longa, é a rachadura térmica. Consiste no fornecimento de calor intenso para que a energia térmica quebre as ligações C-C e, portanto, pequenas moléculas, mais citadas no mercado de combustíveis, de grandes moléculas são formadas.
As quatro reações acima são as principais que podem sofrer um hidrocarboneto alifático, sendo a combustão a mais importante de todas, pois não discrimina nenhum composto; Todos vão queimar na presença de oxigênio, mas nem todos adicionarão moléculas ou se dividem em pequenas moléculas.
Pessoal
Grupo de hidrocarbonetos alifáticos compostos intermináveis, que por sua vez são classificados mais específicos, indicando o grau de sua insaturação, bem como o tipo de estrutura que eles têm.
De acordo com o quão insaturados eles são, temos os alcanos (saturados), alcenos e alcinos (insaturados).
Os alcaneos são caracterizados por ter links c-c simples, enquanto em alcenos e alcinas observamos links c = c e c 3., respectivamente. Uma maneira muito geral de visualizá -los é pensar nos esqueletos de carbono dos alcaneos como zigue -zague e correntes dobradas, sendo "quadrado" para alcenos e "linhas retas" para alcinos.
Isso ocorre porque as ligações duplas e triplas têm energia e restrição estenrica em suas rotações, "endurecendo" suas estruturas.
Alkitos e Alcines podem ser ramificados, cíclicos ou policíclicos. É por isso que cicloalcanos, cicloalquenos, cicloalquinos e compostos como Decalin (estrutura de bicicleta), Adamantano (semelhante a um boné de beisebol), heptaleno, gonano, entre outros, hidrocarbonetos alifáticos também são considerados.
De alcenos, outros tipos de hidrocarbonetos surgem, como os objetivos (com duas ligações duplas), polienous (com muitas ligações alternativas duplas) e terpenos (compostos derivados do isopreno, um dieno).
Formulários
Novamente, os usos para esses hidrocarbonetos podem variar dependendo de qual é considerado. No entanto, nas seções de propriedades e reações, ficou claro que toda a combustão, não apenas para liberar moléculas de gás, mas também leve e calor. Assim, são reservatórios de energia, úteis para servir como combustíveis ou fontes de calor.
É por isso que eles são usados como parte da composição da gasolina, para gás natural, em isqueiros de Bunsen e, em geral, para poder originar fogo.
Pode atendê -lo: regra de octetoUm dos exemplos mais notáveis é o do acetileno, HCidor, cuja combustão permite excitar os íons metálicos de uma amostra na espectrometria de absorção atômica realizada em testes analíticos. Da mesma forma, o incêndio resultante pode ser usado para soldas.
Hidrocarbonetos alifáticos líquidos, como parafinia, são frequentemente usados como solventes de extração de gordura. Além disso, sua ação de solvente pode ser usada para remover pontos, esmaltes, pinturas ou simplesmente para preparar soluções de um composto orgânico específico.
A maior massa molecular, já viscosa ou sólida, é destinada à elaboração de resinas, polímeros ou medicamentos.
No que diz respeito ao termo 'alifático', geralmente é usado para se referir a essas regiões, em uma macromolécula, que não possui aromaticidade. Por exemplo, asfaltens são descritos superficialmente como um núcleo aromático com correntes alifáticas.
Exemplos
A princípio, foi dito que o metano é o mais simples dos hidrocarbonetos alifáticos. Eles são seguidos por propano, CHO3CH2CH3, Butano, cap3CH2CH2CH3, Pentano, cap3CH2CH2CH2CH3, octane, nonano, reitor e assim por diante, tendo alcanes cada vez mais longos.
O mesmo se aplica ao etileno, Cho2= Cap2, Profeno, cap3Ch = ch2, Buteno, cap3CH2Ch = ch3, E pelo resto dos Alcines. Se houver duas ligações duplas, elas são Oley, e se houver mais de duas, Polienas. Da mesma forma, pode haver links duplos e triplos no mesmo esqueleto, aumentando a complexidade estrutural.
Entre os cicloalcanos, podemos mencionar o ciclopropano, ciclobutano, ciclopentano, ciclohexana, cicloheptano, ciclooctano, bem como ciclohexeno e ciclohexina. De todos esses hidrocarbonetos, são obtidos derivados ramificados, multiplicando ainda mais os exemplos disponíveis (como 1.4-dimetilciclohexano).
Dos terpenos mais representativos, temos limoneno, mentol, pinene, vitamina A, escualeno, etc. O polietileno é um polímero saturado com unidades -ch2-CH2-, Portanto, é também um exemplo desses hidrocarbonetos. Outros exemplos já foram citados nas seções anteriores.
Referências
- Morrison, r. T. e boyd, r, n. (1987). Quimica Organica. 5ª edição. Interamericano Editorial Addison-Wesley.
- Carey f. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Graham Solomons t.C., Craig b. Fryhle. (2011). Química orgânica. Aminas. (10ª edição.). Wiley Plus.
- Helmestine, Anne Marie, Ph.D. (22 de agosto de 2019). Definição de hidrocarbonetos alifáticos. Recuperado de: pensamento.com
- Wikipedia. (2019). Composto alifático. Recuperado de: em.Wikipedia.org
- Química Librettexts. (20 de agosto de 2019). Hidrocarbonetos alifáticos. Recuperado de: química.Librettexts.org
- Elizabeth Wyman. (2019). Hidrocarbonetos alifáticos: definição e propriedades. Estudar. Recuperado de: estudo.com
- « Dimensão social sendo humana, educação, conhecimento, certo, saúde
- 100 dados de animais curiosos »

