Estrutura, propriedades e usos de Heptano (C7H16)
- 4004
- 802
- Conrad Schmidt
Ele heptano É um composto orgânico cuja fórmula química é c7H16 e compreende nove isômeros estruturais, dos quais o mais conhecido é o linear. É um hidrocarboneto, especificamente um alcano ou parafina, que é na maioria dos laboratórios de química orgânica, seja ensinando ou pesquisa.
Ao contrário de outros solventes parafinic, o heptano tem uma volatilidade mais baixa, o que torna seu uso relativamente mais seguro; Sempre que não há fonte de calor ao redor de seus vapores e é trabalhado dentro de um sino de extrator. Deixando sua inflamabilidade de lado, é um composto suficientemente inerte servir como um meio de reações orgânicas.
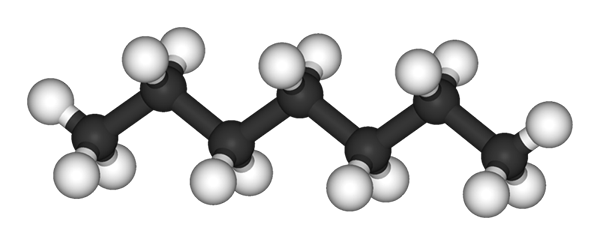
 Molécula n-heptano representada por um modelo de esferas e bares. Fonte: Ben Mills e Jynto [Domínio Público]
Molécula n-heptano representada por um modelo de esferas e bares. Fonte: Ben Mills e Jynto [Domínio Público] Na imagem superior, você tem a estrutura do n-Heptano, o isômero linear de todos os heptanos. Por ser o isômero mais comum e de maior valor comercial, bem como o mais fácil de sintetizar, tende a ser no final que o termo 'heptano' se refere exclusivamente a n-heptano; salvo indicação em contrário.
No entanto, nas garrafas deste composto líquido, é especificado que ele contém n-heptano. Eles precisam descobrir dentro de uma campainha de extrator e executar as medidas cuidadosamente.
É um excelente solvente para gorduras e óleos, por isso é frequentemente usado durante essências vegetais ou outros produtos naturais.
[TOC]
Estrutura
n-heptano e suas interações intermoleculares
Como pode ser visto na primeira imagem, a molécula de n-O heptano é linear e, devido à hibridação química de seus átomos de carbono, a cadeia adota uma forma de Zigzaguada. Esta molécula é dinâmica, porque suas ligações C-C podem girar, o que faz com que a corrente se dobre levemente em ângulos diferentes. Isso contribui para suas interações intermoleculares.
Pode servir você: link piEle n-O Heptano é uma molécula apolar e hidrofóbica e, portanto, suas interações são baseadas nas forças dispersivas de Londres; São aqueles que dependem da massa molecular do composto e de sua área de contato. Duas moléculas de n-heptan.
Essas interações são eficazes o suficiente para manter as moléculas de n-heptano coesivo em um líquido que ferve a 98 ºC.
Isômeros
 Os nove isômeros do heptano. Fonte: Steffen 962 [Domínio Público]
Os nove isômeros do heptano. Fonte: Steffen 962 [Domínio Público] A princípio foi dito que a Fórmula C7H16 representou um total de nove isômeros estruturais, sendo o n-heptano o mais relevante (1). Os outros oito isômeros são mostrados na imagem superior. Observe a olho nu que alguns são mais ramificados do que outros. Da esquerda para a direita, começando de cima, temos:
(2): 2-metilhexan
(3): 3-metilhexan, que consiste em um par de enantiômeros (A e B)
(4): 2,2-dimetilpentano, também conhecido como neoheptono
(5): 2,3-dimetilpentano, novamente com um par de enantiômeros
(6): 2,4-dimetilpentano
(7): 3.3-dimetilpentano
(8): 3-etilpentano
(9): 2,2,3-trimetilbutano.
Cada um desses isômeros tem propriedades e aplicações independentes do n-Heptano, reservado mais do que qualquer coisa para áreas de síntese orgânica.
Propriedades do heptano
Aspecto físico
Líquido incolor com um cheiro semelhante à gasolina.
Massa molar
100.205 g/mol
Ponto de fusão
-90.549 ºC, tornando -se um cristal molecular.
Ponto de ebulição
98,38 ºC.
Pressão de vapor
52,60 atm a 20 ºC. Observe quão alta é a sua pressão de vapor, apesar de ser menos volátil do que outros solventes parafinic, como Hexano e Pentan.
Densidade
0,6795 g/cm3. Por outro lado, os vapores de heptano são 3,45 vezes densos que o ar, o que significa que seus vapores durarão nos espaços onde um pouco de derramamento de seu líquido.
Pode atendê -lo: ácido fórmico (hcooh)Solubilidade em água
O heptano por ser um composto hidrofóbico mal pode se dissolver na água para causar uma solução com uma concentração de 0,0003% a uma temperatura de 20 ºC.
Solubilidade em outros solventes
O heptano é miscível com tetracloreto de carbono, etanol, acetona, éter de óleo e clorofórmio.
Índice de refração (nD)
1.3855.
Gosma
0,389 MPa · s
Capacidade de calor
224.64 J/K · mol
ponto de ignição
-4 ºC
Temperatura de auto -dirigir
223 ºC
Tensão superficial
19,66 mn/m a 25 ºC
Calor de combustão
4817 KJ/mol.
Reatividade
Os vapores heptanos quando estão próximos de uma fonte de calor (uma chama), reaja exotérmica e vigorosamente com o oxigênio do ar:
C7H16 + 11o2 => 7co2 + 8h2QUALQUER
No entanto, fora da reação de combustão, o heptano é um líquido bastante estável. Sua falta de reatividade se deve ao fato de que seus links C-H são difíceis de quebrar, por isso não é suscetível a substituições. Também não é muito sensível a agentes oxidantes fortes, desde que não haja fogo nas proximidades.
O maior perigo de Heptano é representado por sua alta volatilidade e inflamabilidade, então há um risco de incêndio se for derramado em sites quentes.
Formulários
Solvente e meia de reação
 Hepthane é um excelente solvente para dissolver óleos e gorduras. Fonte: pxhere.
Hepthane é um excelente solvente para dissolver óleos e gorduras. Fonte: pxhere. O caráter hidrofóbico do heptano é um excelente solvente para dissolver óleos e gorduras. Nesse aspecto, tem sido usado como um degrestante. No entanto, sua maior aplicação está em ser usada como solvente de extrator, pois dissolve os componentes lipídicos, bem como os outros compostos orgânicos de uma amostra.
Por exemplo, se você deseja extrair todos os componentes do café moído, seria macerado em heptano em vez de água. Este método e suas variações foram implementadas com todos os tipos de sementes, graças às essências das plantas e outros produtos naturais.
Pode atendê -lo: célula unitária: propriedades, constantes vermelhas e tiposO heptano, que é naturalmente incolor, será tingido da cor do óleo extraído. Então, isso é girado para finalmente ter um volume do óleo o mais puro possível.
Por outro lado, a pouca reatividade do heptano também permite que você seja uma opção ao considerar um meio de reação para realizar uma síntese. Sendo um bom solvente de compostos orgânicos, garante que os reagentes permaneçam em solução e interajam entre si enquanto reagem.
Agente precipitado
Na química do petróleo, é uma prática comum precipitar asfaltens de uma amostra bruta adicionando heptano. Este método permite estudar a estabilidade de diferentes brutos e determinar o quão suscetível seu teor de asfalteno é precipitar e levar uma série de problemas para a indústria de petróleo.
Octano
O heptano tem sido usado como combustível devido à grande quantidade de calor que oferece quando queima. No entanto, em relação aos motores de carro, seria prejudicial à sua operação se fosse usado puramente. Porque queima de maneira muito explosiva, serve para definir o 0 na escala octana da gasolina.
A gasolina contém uma alta porcentagem de heptano e outros hidrocarbonetos para nivelar os valores conhecidos (91, 95, 87, 89, etc.).
Referências
- Morrison, r. T. e boyd, r, n. (1987). Quimica Organica. 5ª edição. Interamericano Editorial Addison-Wesley.
- Carey f. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Graham Solomons t.C., Craig b. Fryhle. (2011). Química orgânica. (10ª edição.). Wiley Plus.
- Wikipedia. (2020). Heptano. Recuperado de: em.Wikipedia.org
- Centro Nacional de Informações sobre Biotecnologia. (2020). Banco de dados de heptane pubchem. CID = 8900. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Elsevier b.V. (2020). Heptans. Cientedirect. Recuperado de: ScientEdirect.com
- Bell Chem Corp. (7 de setembro de 2018). Usos industriais de heptano. Recuperado de: Bellchem.com
- Andrea Kropp. (2020). Heptano: estrutura, uso e fórmula. Estudar. Recuperado de: estudo.com
- « Fórmula condensada O que é e exemplos (metano, etano, glicose ...)
- Fórmulas de energia mecânica, conceito, tipos, exemplos, exercícios »

