Modelo de gás ideal, comportamento, exemplos
- 3939
- 627
- Alfred Kub
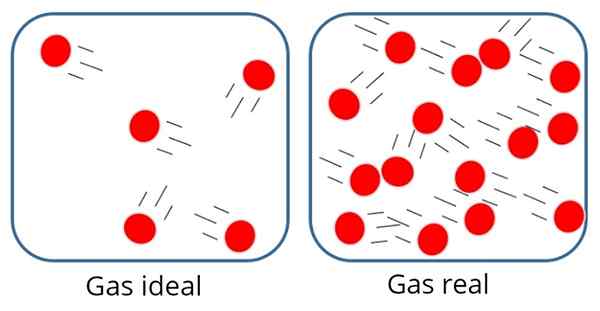
A Gás ideal qualquer Gás perfeito É aquele em que a força de atração ou repulsão molecular é considerada insignificante entre as partículas que a compõem; portanto, toda a sua energia interna é cinética, ou seja, energia associada ao movimento.
Em tal gás, as partículas geralmente estão muito longe uma da outra, embora ocasionalmente colidam entre si e com as paredes do recipiente.
 No gás ideal, as partículas estão longe uma da outra
No gás ideal, as partículas estão longe uma da outra Por outro lado, no gás ideal, o tamanho ou massa das partículas não importa, pois o volume ocupado por elas deve ser muito pequeno em comparação com o volume do próprio gás.
Isso, é claro, é apenas uma abordagem, porque na realidade sempre há algum grau de interação entre átomos e moléculas. Também sabemos que as partículas ocupam espaço e têm massa.
No entanto, essas suposições funcionam muito bem em muitos casos, como gases de baixo peso molecular, em uma boa gama de pressões e temperaturas.
No entanto, gases de alto peso molecular, especialmente em altas pressões ou baixas temperaturas, não se comportam como gases ideais e precisam de outros modelos criados com o objetivo de descrevê -los com maior precisão.
[TOC]
Primeiros experimentos
As leis que governam os gases são empíricas, ou seja, surgiram da experimentação. Os experimentos mais notáveis foram realizados nos anos XVII, XVIII e início do século XIX séculos.
Primeiro são os de Robert Boyle (1627-1691) e Edme Mariotte (1620-1684), que modificaram independentemente o pressão em um gás e registrou sua mudança de volume, descobrindo que eles eram inversamente proporcionais: a maior pressão, menos volume.
 Robert Boyle
Robert Boyle Por sua parte, Jacques Charles (1746-1823) estabeleceu esse volume e temperatura absoluto eram diretamente proporcionais, desde que a pressão permanecesse constante.
Pode servir a você: ondas estacionárias: fórmulas, características, tipos, exemplosAmadeo Avogadro (1776-1856) descobriu que dois volumes idênticos de gases diferentes continham a mesma quantidade de partículas, desde que a pressão e a temperatura fossem iguais. E, finalmente, Joseph de Gay Lussac (1778-1850), disse que, mantendo o volume fixo, a pressão em um gás é diretamente proporcional à temperatura.
As leis dos gases ideais
Essas descobertas são expressas através de fórmulas simples, chamando p para a pressão, V para o volume, n para o número de partículas e T A temperatura ideal do gás:
Lei Boyle-Maleotte
Desde que a temperatura seja fixa, ocorre o seguinte:
P⋅v = constante
Charles Law
Quando o gás está sob pressão constante:
V / t = constante
Lei Gay Lussac
Manter o gás em um volume fixo é verdadeiro que:
p / t = constante
Lei Avogadro
Volumes de gás idênticos, sob a mesma pressão e temperatura, as condições têm o mesmo número de partículas. Portanto, podemos escrever:
V ∝ n
Onde n é o número de partículas e ∝ é o símbolo da proporcionalidade.
Modelo de gás ideal
O modelo de gás ideal descreve um gás de modo que:
-Quando as partículas interagem o fazem por um tempo muito curto, através de confrontos elásticos, nos quais o ímpeto e a energia cinética são preservados.
-Suas partículas constituintes são pontuais; em outras palavras, seu diâmetro é muito menor que a distância média que percorrem entre uma e outra colisão.
-Forças intermoleculares não existentes.
-A energia cinética é proporcional à temperatura.
Gases monoatómicos -cuyos átomos no están ligados entre sí- y de bajo peso molecular, en condiciones estándar de presión y temperatura (presión atmosférica y 0 º C de temperatura), tienen un comportamiento tal que el modelo de gas ideal es una muy buena descripción para eles.
Pode atendê -lo: Vy Canis majoris: descoberta, características, estrutura, treinamento e evoluçãoEquação de status de gás ideal
As leis dos gases acima são combinadas para formar a equação geral que governa o comportamento ideal do gás:
V ∝ n
V ∝ t
Portanto:
V ∝ n⋅t
Além disso, da lei de Boyle:
V = constante / p
Então podemos afirmar que:
V = (constante x n⋅t) / p
A constante é chamada de constante de gás E é indicado pela letra r. Com essa escolha, a equação ideal do gás relaciona quatro variáveis que descrevem o estado do gás, a saber, n, r, p e t, deixando:
P⋅v = n⋅r⋅t
Esta equação relativamente simples é consistente com as leis dos gases ideais. Por exemplo, se a temperatura for constante, a equação é reduzida à lei Boyle-Maleotte.
A constante de gás
Como já dissemos antes, em condições padrão de temperatura e pressão, ou seja, a 0ºC (273.15 k) e 1 atmosfera de pressão, o comportamento de muitos gases está próximo do gás ideal. Sob essas condições, o volume de 1 mol de gás é 22.414 l.
Em tal caso:
R = (p⋅v) / (n⋅t) = (1 atm x 22.414 L) / (1 mol x 273.15 k) = 0.0821 atm ⋅ l /mol ⋅ k
A constante de gás também pode ser expressa em outras unidades, por exemplo, no sistema internacional, se vale a pena:
R = 8.314 J⋅ mol-1⋅ k-1
Quando um problema é resolvido através da lei ideal para gases, é conveniente prestar atenção às unidades em que a constante é expressa, pois, como podemos ver, existem muitas possibilidades.
Comportamento de um gás ideal
Como dissemos, qualquer gás nas condições padrão de pressão e temperatura com baixo peso molecular, se comporta muito próximo ao gás ideal. Portanto, a equação p⋅v = n⋅r⋅t é aplicável para encontrar a relação entre as quatro variáveis que a descrevem: n, p, v e t.
Pode atendê -lo: Heisenberg Atomic ModelDessa forma, podemos imaginar uma porção de gás ideal travada em um recipiente e formada por pequenas partículas, que ocasionalmente colidem entre si e com as paredes do recipiente, sempre elástica.
É isso que vemos na seguinte animação de uma porção de hélio, um gás nobre e monoatômico:
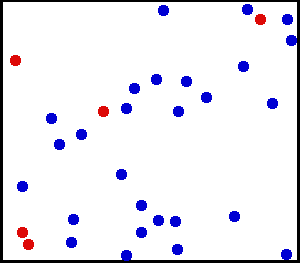 O hélio é um gás nobre, na animação uma porção de átomos de hélio é mostrada em um contêiner. Os vermelhos servem para melhor distinguir o movimento. Fonte: Wikimedia Commons.
O hélio é um gás nobre, na animação uma porção de átomos de hélio é mostrada em um contêiner. Os vermelhos servem para melhor distinguir o movimento. Fonte: Wikimedia Commons. Exemplos de gases ideais
Um gás ideal é um gás hipotético, ou seja, é uma idealização, no entanto, na prática, muitos gases se comportam de uma maneira muito próxima, possibilitando o modelo pulas.
gases nobres
Exemplo de gases que se comportam como ideais em condições padrão são gases nobres, além de gases leves: hidrogênio, oxigênio e nitrogênio.
O balão aerostático
 O modelo de gás ideal explica como o balão de ar quente. Fonte: Wikimedia Commons.
O modelo de gás ideal explica como o balão de ar quente. Fonte: Wikimedia Commons. Para o balão aerostático da Figura 1, pode ser aplicado pela lei de Charles: o gás é aquecido, portanto o ar que enche o globo se expande e, como conseqüência, sobe.
Balões de hélio
Hélio é, juntamente com o hidrogênio, o elemento mais comum no universo, e ainda assim é escasso na terra. Como um gás nobre é inerte, diferentemente do hidrogênio, os balões cheios de hélio são amplamente utilizados como elementos decorativos.
Referências
- Atkins, p. 1999. Química Física. Edições Omega.
- Chang, R. 2013. Química. 11VA. Edição. Mc Graw Hill Education.
- Cengel, e. 2012. Termodinâmica. 7ª edição. McGraw Hill.
- Cimbala, c. 2006. Mecânica de fluidos, fundamentos e aplicações. Mc. Graw Hill.
- Giambattista, a. 2010. Física. 2º. Ed. McGraw Hill.
- « Características do ambiente natural, elementos, importância, exemplos
- Exemplos de função apelativa e características »

