Epmers
- 1297
- 86
- Orlando MacGyver
 Estrutura de um epímero. Fonte: Gabriel Bolívar
Estrutura de um epímero. Fonte: Gabriel Bolívar Quais são os epigrafts?
O Epmers Eles são diaiaisômeros nos quais apenas um de seus centros aquirais difere da configuração espacial, diferentemente dos enantiômeros, onde todos os centros aquirais têm configurações diferentes, e representam algumas imagens especulares que não podem se sobrepor no outro.
O restante dos digoisômeros (isômeros geométricos, por exemplo), pode ter mais de dois centros com diferentes configurações. Portanto, uma grande porcentagem de estereoisômeros são diaiastoisômeros.
Os EPMERs ocorrem frequentemente em carboidratos: por exemplo, D-glicose e D-Manosa diferem em C2, que é o primeiro átomo de carbono quiral.
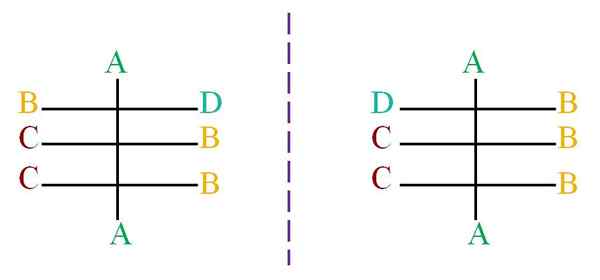
Suponha que uma estrutura com um esqueleto de átomos pretos ligados às letras A, B, C e D (Imagem Superior).
A linha pontilhada representa o espelho, demonstrando que o torque das moléculas acima não são enantiômeros, uma vez que todos os seus centros quirais têm a mesma configuração, exceto o primeiro centro, ligados às letras B e D.
A molécula à esquerda tem a letra D olhando para o lado direito, enquanto a letra D da molécula direita, olha para o lado esquerdo. Para saber qual deve ser usada a configuração de cada.
Características dos Epigmers
- A principal característica dos Epigmers está apenas em um centro aquiral (ou estereogênico).
Alterar a orientação espacial de D e B pode causar conformadores mais estáveis ou instáveis, ou seja, as rotações dos links simples fazem com que dois átomos ou grupos de átomos volumosos sejam ou se afastem.
Assim, um epímero pode ser muito mais estável do que o outro. Aquele que gira seus elos gera estruturas mais estáveis, será o epimerus com a maior tendência de se formar em um equilíbrio.
Pode atendê -lo: sistema não homogêneoVoltando às cartas, D e B podem ser muito volumosos, enquanto C é um pequeno átomo. Portanto, ser o epímero da direita é mais estável, já que D e C foram encontrados à esquerda dos dois primeiros centros sofrem de menos impedimento estérico.
- Microscopicamente, isso se torna uma característica para o par de epiteles considerados.
- Macroscopicamente, as diferenças são acentuadas e terminam, por exemplo, tendo pontos de fusão, índices de refração, diferentes espectros de RMN (além de muitas outras propriedades).
- No campo da biologia e reações catalisadas por enzimas, é onde os epitadores diferem ainda mais. Um pode ser metabolizado pelo corpo, enquanto o outro não.
Treinamento
Os EPMers são formados por uma reação química chamada epimerização. Se ambos os epitancadores não diferirem em um grande grau de estabilidade, é estabelecido um equilíbrio de epimerização, o que nada mais é do que uma interconversão:
EPB EPA
Onde a EPA é Epimer A e Epb, o Epimer. Se um deles for muito mais estável que o outro, terá uma concentração maior e causará o que é conhecido como mutarrotação. Em outras palavras, ele será capaz de alterar a direção de um feixe de luz polarizada.
A epimerização pode não ser um equilíbrio e, portanto, ser irreversível. Nesses casos.
A via sintética dos epitares varia dependendo dos reagentes envolvidos, da reação significa e das variáveis de processo (uso de catalisadores, pressão, temperatura, etc.).
Por esse motivo, a formação de cada par de epitares deve ser estudada individualmente de outros, cada um com seus próprios mecanismos e sistemas químicos.
Pode servir a você: Redutor Agente: Conceito, os Exemplos mais fortesTautomerização
Entre todos os processos de formação de epitemer, a tautomerização de dois dias de dois dias pode ser considerada como um exemplo geral.
Isso consiste em um equilíbrio em que a molécula adota uma forma de cetona (c = o) ou o crescente (c-oh). Uma vez que a forma cetônica é convertida, a configuração de carbono adjacente ao grupo carbonil (se for quiral) muda, gerando alguns epithemers.
Um exemplo do acima mencionado é o torque cis-decalona e trans-desviado.
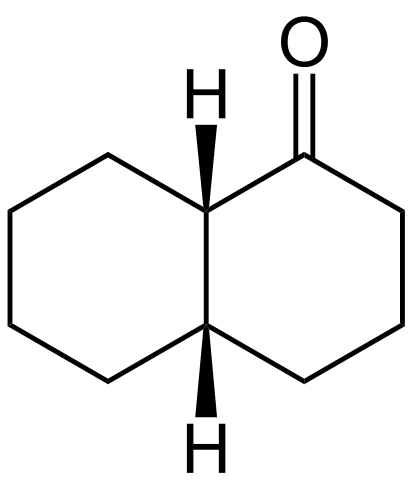 Estrutura cis-decalona. Fonte: Wikimedia Commons
Estrutura cis-decalona. Fonte: Wikimedia Commons A estrutura do cis-decalona é mostrada acima. Os átomos de H estão localizados no topo dos dois anéis, enquanto na trans-des-desceala, um está acima dos anéis e o outro está abaixo.
O carbono à esquerda do grupo C = O é o centro quiral e, portanto, aquele que diferencia os epitches.
Exemplos
Anômeros de glicose
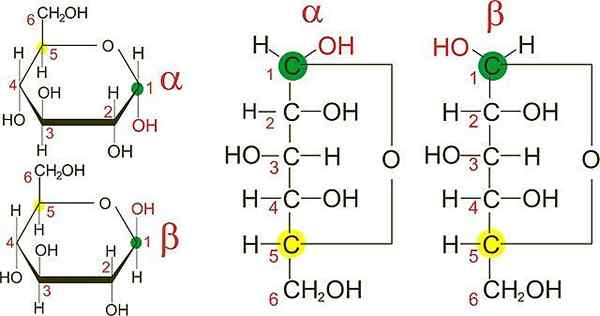 Anômeros em D-glicose. Fonte: Wikimedia Commons
Anômeros em D-glicose. Fonte: Wikimedia Commons Na imagem superior, você tem os anéis furanos dos dois anômeros de D-glicose: α e β. A partir dos anéis, pode -se observar que os grupos OH no carbono 1 são encontrados na mesma direção do OH adjacente, no anímer α, ou em direções opostas, como no anômer β.
As projeções de Fisher de ambos os anômeros (à direita da imagem) tornam a diferença entre os dois epitãos ainda mais claros, que são, por sua vez, anômeros.
No entanto, dois anômeros α podem ter diferentes configurações espaciais em um dos outros carbonos e, portanto, epithemers.
No C-1 da projeção de Fisher para o anímer α, o grupo OH "parece" para a direita, enquanto no β "Look" β Anômer.
Pode atendê -lo: Faraday constanteIsômeros mentol
 Estereoisômeros de Mentol. Fonte: Wikimedia Commons
Estereoisômeros de Mentol. Fonte: Wikimedia Commons Na imagem, você tem todos os estereoisômeros da molécula de Mentol. Cada coluna representa um par de enantiômeros (observar cuidadosamente), enquanto as fileiras correspondem aos diastereoisômeros.
Portanto, os epitares devem ser aqueles que quase não diferenciam nada mais do que na posição espacial de um carbono.
O (+)-mentol e o neoisomentol (-)-são epitéricos e também diabeteroisômeros (eles não estão na mesma coluna).
Se for observado em detalhes, em ambos os grupos -oh e -ch3 Eles deixam o avião (acima do anel), mas no (-)-neoisomentol, o grupo isopropil também aponta para fora do avião.
Não apenas o (+)-mentol é o epímero de (-)-neoisomentol, mas também (+)-neomentol. O último difere apenas que o grupo -ch3 aponta para baixo no avião. Outros epitamentos são:
- (-)-isomentol e (-)-neomentol
- (+)-isomentol e (+)-neomentol
- (+)-neoisomentol e (-)-neomentol
- (+)-neomentol e (-)-neoisomentol
Esses estereoisômeros representam um exemplo prático para esclarecer o conceito de epithemers, e pode -se observar que, de vários diastereoisômeros, muitos só podem ser diferenciados em um único carbono assimétrico ou quiral.
Referências
- Carey f. (2008). Quimica Organica. Mc Graw Hill.
- Epmers. Recuperado das salas de aula.Uruguaieduca.Edu.oh

