Estrutura de Einstenio (s), propriedades, obtenção, usos

- 3276
- 738
- Terrence King IV
Ele Einstenio É um elemento químico que pertence à classe de actinídeos ou actinóides. Seu número atômico é 99 e é representado pelo símbolo é. É um elemento sintético, pois não foi encontrado em nenhum material mineral ou terrestre. Foi descoberto em 1952 em restos do primeiro teste de explosão da bomba de hidrogênio.
Actinóides são uma série cujo primeiro membro é actinium e faz parte das chamadas Elementos de transição internos. Einstenio também é o sétimo elemento transurico, pois sete lugares estão localizados posteriormente de urânio na tabela periódica dos elementos.
 Símbolo, número atômico e massa atômica padrão de Einsenio. Me/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/2.5). Fonte: Wikimedia Commons.
Símbolo, número atômico e massa atômica padrão de Einsenio. Me/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/2.5). Fonte: Wikimedia Commons. É um sólido muito radioativo e uma vez formado começa a se desintegrar a formação de outros elementos, o que tornou muito difícil estudá -lo. Embora o número de isótopos possíveis de Einstenio seja grande, apenas menos de 20% foi descoberto.
Einstenio não tem usos comerciais. É produzido em quantidades muito pequenas em laboratórios nucleares e só é destinado a experimentos científicos. Além disso, os pesquisadores nesses ensaios o usam em muito poucos microgramas e com devida precauções, uma vez que a exposição à sua radiação é letal.
[TOC]
Nomenclatura
- Einstenio, símbolo químico: é
- Einstenio-253, ES-253 ou 253É: Einstenio isotópio com uma massa atômica de 253.
Descoberta
Origem
Este elemento foi identificado pela primeira vez por Albert Ghiorso (cientista nuclear dos EUA) e seus colaboradores em dezembro de 1952 em fragmentos dispersos pela explosão termonuclear do primeiro teste de bomba de hidrogênio.
Esta bomba H, chamada "Ivy Mike" e também "La Salachicha" por sua forma, foi detonada em novembro do mesmo ano em uma ilha pertencente a um atol de corais do Pacífico.
 Explosão da bomba de hidrogênio Ivy Mike. OU.S. Departamento de Energia / Domínio Público. Fonte: Wikimedia Commons.
Explosão da bomba de hidrogênio Ivy Mike. OU.S. Departamento de Energia / Domínio Público. Fonte: Wikimedia Commons. Para detonar, uma bomba de fissão de urânio foi usada. Os átomos deste último capturaram vários nêutrons durante a explosão e sofreram várias etapas de decaimento beta, em cada um dos quais um elétron e um próton são emitidos, o que levou à formação de Einstenio-253, um isótopo do ES.
Um isótopo é uma variante do mesmo elemento que tem um número diferente de nêutrons no núcleo do átomo, por isso possui o mesmo número atômico (neste caso 99), mas a massa atômica diferente. O número isótopo indica sua massa atômica.
Pode servir a você: Trioxide de enxofre (SO3): estrutura, propriedades, riscos, usosPublicação da descoberta
No início, o trabalho foi mantido em segredo, mas depois de um ano os autores decidiram publicá -lo por medo de que outros cientistas independentes pudessem produzi -lo em outros laboratórios, obter o crédito da descoberta e atribuir o nome ao elemento.
Então, de novembro de 1953 a março de 1954, eles relataram quatro de seus isótopos. Finalmente, no verão de 1955, a descoberta do novo elemento Einstenio com o número 99 atômico foi anunciado.
 Os núcleos dos átomos têm prótons e nêutrons. Os isótopos de um elemento são átomos do mesmo que têm um número diferente de nêutrons em seu núcleo. Autor: Gerd Altmann. Fonte: Pixabay.
Os núcleos dos átomos têm prótons e nêutrons. Os isótopos de um elemento são átomos do mesmo que têm um número diferente de nêutrons em seu núcleo. Autor: Gerd Altmann. Fonte: Pixabay. É importante observar que a coleção das amostras da explosão termonuclear reivindicou a vida do primeiro tenente Jimmy Robinson, que foi exposto à radiação destes.
Seleção de nome
O nome de "Einstenio" foi escolhido porque Albert Einstein lançou algumas das bases da teoria quântica que explicariam como os átomos interagem entre si.
A coisa mais significativa sobre a presença de seu nome é a aplicação de sua famosa equação e = mc2, que explica a conversão da massa em energia nas armas mais destrutivas criadas pelo ser humano.
 Albert Einstein não concordou com o uso da ciência para criar armas destrutivas. Autor: Stux. Fonte: Pixabay.
Albert Einstein não concordou com o uso da ciência para criar armas destrutivas. Autor: Stux. Fonte: Pixabay. Os autores da descoberta sugeriram que o elemento tinha o símbolo "E", mas em 1957 a União Internacional da Química Pura e Aplicada, ou IUPAC (acrônimo de inglês União Internacional de Química Pura e Aplicada), mudou o símbolo para "é".
Estrutura eletrônica
Sua configuração eletrônica é:
1s2; 2s2 2p6; 3s2 3p6 3d10; 4s2 4p6 4d10 4F14; 5s2 5p6 5d10; 6s2 6p6; 5Fonze 7s2,
ou resumo:
[RN] 5Fonze 7s2,
onde [RN] é a estrutura eletrônica do Noble Radon Gas (que também é radioativo).
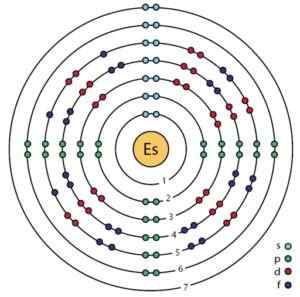 Esquema dos orbitais e elétrons de um átomo de Einstenio, de acordo com um modelo Bohr aprimorado. Ahazard.ScienceWriter/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/4.0). Fonte: Wikimedia Commons.
Esquema dos orbitais e elétrons de um átomo de Einstenio, de acordo com um modelo Bohr aprimorado. Ahazard.ScienceWriter/CC BY-SA (https: // CreativeCommons.Org/licenças/BY-SA/4.0). Fonte: Wikimedia Commons. Propriedades de Einstenio
Estado físico
Sólido metálico à temperatura ambiente.
Pode atendê -lo: nitrato de prata (AGNO3): estrutura, propriedades, usos, toxicidadeMassa atômica
252.083
Ponto de fusão
860 ºC
Ponto de ebulição
996 ºC
Propriedades quimicas
Estudos com 253Está mostrando que o comportamento deles é o que normalmente é observado em um elemento de atuação trivalente, isto é, em suas reações Valencia +3 predomina.
Alguns dos compostos com estado de oxidação +3 foram caracterizados, como cloreto (SCL3), Bromuro (ESBR3), Yoduro (ESI3), oxicloreto (ESOCL) e óxido (é2QUALQUER3).
 Imagem de Eintenio Yoduro tirada no escuro. A luz é causada por emissão de radioatividade. O laboratório nacional de Alamos. / Domínio público. Fonte: Wikimedia Commons.
Imagem de Eintenio Yoduro tirada no escuro. A luz é causada por emissão de radioatividade. O laboratório nacional de Alamos. / Domínio público. Fonte: Wikimedia Commons. No entanto, valências +2 e +4 também foram relatadas, embora não tenham sido confirmadas. Nesse caso, seria o primeiro metal divalente da série Actinid.
Os dados cristalográficos de raio X e seus compostos são muito difíceis de obter, porque sua desintegração espontânea produz radiação gama e raios X que superexamporam o detector de instrumentos e o filme.
Isótopos
Até agora, 19 isótopos do ES foram descobertos com massas atômicas entre 241 e 257 e 3 isômeros. Nenhum é estável. No entanto, de todos os isótopos possíveis de Einstenio foram produzidos e identificados menos de 20%.
Seu isótopo mais estável é o Eintenio-252, que tem meia-vida de 471,7 dias. Berkelio-248 se desintegra através da emissão de uma partícula alfa (formada por 2 prótons e 2 nêutrons) ou se torna californio-252 capturando um elétron.
Obtenção atual
Atualmente, Einstenio é produzido por uma longa cadeia de reações nucleares que envolve o bombardeio de cada isótopo de cadeia com nêutrons e, no final, o isótopo resultante sofre decaimento beta.
Na decaimento ou desintegração beta, o núcleo do átomo emite uma partícula beta, que pode ser um elétron ou um pósitron, para equilibrar a razão de nêutrons/prótons no núcleo do átomo.
Procedimento
Nos Estados Unidos Oak Ridge Laboratories lá tem Reator de isótopos de alto fluxo). Um micrograma é o milionésimo de um grama, ou seja, é equivalente a 0,000001 grama.
Pode atendê -lo: tiisO método foi o seguinte:
- Por vários anos grandes quantidades (quilogramas) de 239PU (Polonio-239) para produzir 242Pu.
- O 242Pu em óxido de plutônio e misturado com óxido de alumínio ao2QUALQUER3 Para formar esferas compactadas.
- As esferas do material foram incorporadas em bares especiais para serem irradiados por um ano na fábrica do rio Savannah, nos Estados Unidos.
- Então as barras foram irradiadas no HFIR por mais 4 meses.
- Finalmente, o material resultante foi submetido a procedimentos químicos para separar o Einstenio dos isótopos californio (filhos do ES).
 Núcleo de um átomo. Os núcleos de polônio são bombardeados com nêutrons como parte do procedimento para obter Einstenio. Autor: Clker-Free-Vector-Imagens. Fonte: Pixabay.
Núcleo de um átomo. Os núcleos de polônio são bombardeados com nêutrons como parte do procedimento para obter Einstenio. Autor: Clker-Free-Vector-Imagens. Fonte: Pixabay. Nas operações especiais do HFIR, elas podem ser obtidas até 2 miligramas (mg) de Einstenio.
Formulários
Esse elemento só ocorreu em quantidades muito pequenas, também é muito radioativo, por isso não tem uso comercial. Atualmente tem aplicação apenas em pesquisa científica básica.
Na obtenção de Mendelevio
Em 1961, uma quantidade macroscópica de 253É com um peso de 0,01 microgramas (μg) medidos com um equilíbrio magnético especial. Esta amostra foi então bombardeada com nêutrons para produzir o elemento Mendelevio (número atômico 101).
Em estudos sobre os efeitos da radiação
A auto -comissão intensa de radiação einstenio pode ser usada para estudar o envelhecimento acelerado e os danos exercidos por radiação.
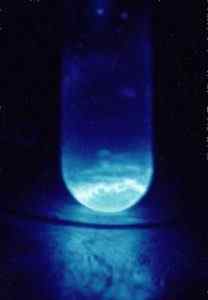 Radiação emitida por Einstenio-253. Foto tirada no escuro. Haire, r. G., Departamento de Energia dos EUA.Tocada pelo material -cientista em.Wikipedia. / Domínio público. Fonte: Wikimedia Commons.
Radiação emitida por Einstenio-253. Foto tirada no escuro. Haire, r. G., Departamento de Energia dos EUA.Tocada pelo material -cientista em.Wikipedia. / Domínio público. Fonte: Wikimedia Commons. Por exemplo, tem sido usado em estudos sobre as consequências químicas da desintegração radioativa.
Devido à meia-vida relativamente curta do ES-253 (20,47 dias), você pode estudar o crescimento interno de seu filho Sonotopo BK-249, cuja meia-vida é de 330 dias e a do neto CF-249 (vida média de 351 anos).
Certos dados sugerem que ele é um divalente pode diminuir para um caliporto divalente divalente (ainda desconhecido).
Em estudos químicos e físico -químicos
É o elemento mais pesado com o qual os estudos podem ser realizados que permitem o desenvolvimento de pesquisas fundamentais sobre o papel que os elétrons 5F Na organização e classificação de actinídeos.
O ES-252 está disponível apenas em quantidades mínimas. Os isótopos ES-253 (meia-vida de 20,47 dias) e ES-254 (275,7 dias) têm uma meia-vida mais longa e têm uma maior disponibilidade destes, para que sejam usados em estudos físico-químicos.
No entanto, apenas alguns microgramas (μg) são usados em experimentos para reduzir a exposição dos trabalhadores e minimizar os efeitos da auto -irradiação intensa.
 Einstenio é muito perigoso porque é um elemento poderosamente radioativo. Autor: Clker-Free-Vector-Imagens. Fonte: Pixabay.
Einstenio é muito perigoso porque é um elemento poderosamente radioativo. Autor: Clker-Free-Vector-Imagens. Fonte: Pixabay. Uso potencial em medicina
Estima -se que possa ser usado para tratamentos médicos de radiação destinados a certos órgãos.
Referências
- Chumbo, d.R. (Editor) (2003). Manual de Química e Física do CRC. 85º CRC Press.
- PubChem (2020). Einsteinium - é (elemento). Recuperado de PubChem.NCBI.Nlm.NIH.Gov.
- Algodão, f. Albert e Wilkinson, Geoffrey. (1980). Química inorgânica avançada. Quarta edição. John Wiley & Sons.
- Meierfrankenfeld, d. et al. (2011). Descoberta de Scandium, Titanium, Mercury e Einsteinium Isotopes. Dados atômicos e tabelas de dados nucleares 97 (2011) 134-151. Recuperado de cientedirect.com.
- Sociedade Real de Química. (2020). Einsteinium. RSC se recuperou.org.
- Ross, r. (2017). Fatos sobre Einsteinium. Recuperado da LiveScience.com.
- « Características e exemplos de empresas mistas
- Características do mercado -alvo, tipos, como defini -lo, exemplos »

