Derivados halogenados

- 981
- 149
- Terrence King IV
Explicamos quais são os derivados halogenados, suas propriedades, usos/aplicativos e damos vários exemplos
O que são derivados halogenados?
O derivados halogenados Todos são compostos que têm um átomo de halogênio; isto é, qualquer um dos elementos do grupo 17 (f, cl, br, i). Esses elementos diferem do resto porque são mais eletronegativos, formando uma diversidade de halogenetos inorgânicos e orgânicos.
A imagem inferior dos halogênios é mostrada na imagem inferior. De cima para baixo: fluoreto (f2), Cloro (CL2), Bromo (BR2) e iodo (eu2). Cada um deles tem a capacidade de reagir com a grande maioria dos elementos, inclusive entre congêneres do mesmo grupo (interhalógenos).

Assim, derivados halogenados têm uma fórmula MX se for um haluro de metal, rx se for alquil e arx se for aromático. Os dois últimos estão localizados na categoria Haluros Organic. A estabilidade desses compostos requer um "benefício" de energia em frente à molécula de refrigerante original.
Como regra geral, o fluoreto forma halogenado mais estável que o iodo. O motivo é devido às diferenças entre seus rádios atômicos (as esferas roxas são mais volumosas que as amarelas).
Ao aumentar o raio atômico, a sobreposição dos orbitais entre o halogênio e o outro átomo é mais pobre e, portanto, o link é mais fraco.
Nomenclatura
A maneira de nomear corretamente esses compostos depende se são inorgânicos ou orgânicos.
Inorgânico
Os halogenetos metálicos consistem em uma ligação, iônica ou covalente, entre um halogênio X e um me metal (dos grupos 1 e 2, metais de transição, metais pesados, etc.).
Nesses compostos, todos os halogênios têm um estado de oxidação de -1. Porque? Porque suas configurações de valência são ns2NP5.
Portanto, eles precisam ganhar apenas um elétron para completar o octeto de Valência, enquanto os metais oxidam, dando -lhes os elétrons que eles têm.
Pode atendê -lo: equilíbrio de precisão: características, funções, peças, usosAssim, o fluoreto permanece como f-, fluoreto; O cl-, cloreto; o Br-, brometo; e o i-, Eu último. MF seria nomeado: Fluoreto de (nome de metal) (n), sendo n o Valencia del Metal apenas quando tiver mais de um. No caso de grupos de grupos 1 e 2, não é necessário nomear Valencia.
Exemplos
- Naf: fluoreto de sódio.
- CACL2: cloreto de cálcio.
- AGBR: brometo de prata.
- Zni2: Zinco Yoduro.
- CUCL: cloreto de cobre (i).
- CUCL2: cloreto de cobre (ii).
- Ticl4: Cloreto de titânio (iv) ou tetracloreto de titano.
No entanto, elementos de hidrogênio e não -metal - mesmo os mesmos halogênios - também podem formar haluros. Nesses casos, a valência do metal não é nomeada no final:
- Pcl5: pentacloreto de fósforo.
- BF3: Boro Trifluoruro.
- Todos3: Triyoduro de alumínio.
- HBR: brometo de hidrogênio.
- Se7: heptofluoreto de iodo.
Orgânico
Independentemente de RX ou ARX, o halogênio está covalentemente ligado a um átomo de carbono. Nesses casos, os halogênios são mencionados por seus nomes, e o restante da nomenclatura depende da estrutura molecular de R ou AR.
Para a molécula orgânica mais simples, metano (CHO4), Os seguintes derivados são obtidos substituindo o H por Cl:
- CH3CL: Clorometano.
- CH2Cl2: diclorometano.
- Chcl3: tricilorometano (clorofórmio).
- Ccl4: Tetraclorometano (cloreto de carbono (iv) ou tetracloreto de carbono).
Aqui r consiste em um único átomo de carbono. Então, para outras cadeias alifáticas (lineares ou galhos), o número de carbonos é contado do qual está ligado ao halogênio:
CH3CH2CH2F: 1-FLUORPROPANO.
O exemplo anterior era o de um halogeneto alquil primário. No caso de a cadeia ser ramificada, a mais longa que contém o halogênio é escolhida e começa a contar, deixando isso o número possível:
Pode atendê -lo: quais são as propriedades físicas da matéria?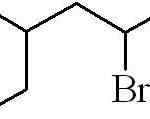
3-metil-5-bromohexan
Da mesma maneira que ocorre para outros substituintes. Além disso, para os halogenetos aromáticos, o halogênio é nomeado e, em seguida, o restante da estrutura:

A imagem superior mostra o composto chamado bromobenzeno, destacando o átomo de bromo em marrom.
Propriedades de derivados halogenados
Halogenetos inorgânicos
Os halogenetos inorgânicos são sólidos iônicos ou moleculares, embora os primeiros sejam mais abundantes. Dependendo das interações e rádios iônicos de MX, isso será solúvel em água ou outros solventes menos polares.
Os halogenetos não metálicos (como o boro) são geralmente ácidos de Lewis, o que significa que eles aceitam elétrons para formar complexos. Por outro lado, halogenetos (ou halogenuros) de hidrogênio dissolvido em água produzem o que é conhecido como hidrácio.
Seus pontos de fusão, fervura ou sublimação caem nas interações eletrostáticas ou covalentes entre metal ou não -metal com halogênio.
Da mesma forma, os rádios iônicos desempenham um papel importante nessas propriedades. Por exemplo, se m+ e x- Eles têm tamanhos semelhantes, seus cristais serão mais estáveis.
Halogenetos orgânicos
Eles são polares. Porque? Porque a diferença nas eletronegatividades entre C e o halogênio cria um momento polar permanente na molécula. Além disso, isso diminui à medida que o grupo 17 desce, do link c-f para C-i.
Sem considerar a estrutura molecular de R ou AR, os crescentes números de halogênio afetam diretamente os pontos de ebulição, pois aumentam a massa molar e as interações intermoleculares (RC-X-X-CR). A maioria é imiscível com a água, mas pode se dissolver em solventes orgânicos.
Usos de derivados halogenados
Os usos de derivados halogenados podem reservar seu próprio texto. Os "companheiros" moleculares dos halogênios são um fator -chave, dado que suas propriedades e reatividades definem os usos do derivado.
Pode servir a você: sulfato de potássio (K2SO4): estrutura, propriedades, usos, sínteseAssim, entre a grande diversidade de usos possíveis, o seguinte se destaca:
- Os halogênios moleculares são usados para criar lâmpadas de halogênio, onde você entra em contato com o incandescente filamento de tungstênio. O objetivo desta mistura é reagir o halogênio x com o tungstênio evaporado. Dessa maneira, seu depoimento é evitado na superfície da lâmpada, garantindo mais tempo de vida.
- Os sais de fluoruros são usados na fluorização de águas dentárias e pastas.
- Os hipocloritos de sódio e cálcio são dois agentes ativos em soluções comerciais de branqueamento (cloro).
- Embora eles se deteriorem a camada de ozônio, os clorofluorocarbonetos (CFCs) são usados em aerossóis e sistemas de refrigeração.
- Cloreto de vinil (CHO2= CHCL) é o monômero do cloreto de polivinil (PVC). Por outro lado, o Teflon, usado como material não -palito, consiste em cadeias poliméricas de tetrafluoretileno (f2C = cf2).
- Eles são usados na química analítica e na síntese orgânica para diferentes fins; Entre eles, a síntese de drogas.
Exemplos adicionais

A imagem superior ilustra o hormônio da tireóide, responsável pela produção de calor, bem como pelo aumento do metabolismo geral no corpo. Este composto é um exemplo de derivado halogenado presente no corpo humano.
Entre outros compostos halogenados, são mencionados os seguintes:
- Diclorodifenilriclorootan (DDT), inseticida eficiente, mas com graves impactos ambientais.
- Cloreto de lata (SNNCL2), usado como um agente redutor.
- Cloroetano ou 1-cloroetano (CH3CH2Cl), anestésica tópica que age rapidamente resfriando a pele.
- Dicloroetileno (clch = cclh) e tetracloretileno (Cl2C = ccl2), usado como solventes na indústria de limpeza a seco.
- « Estrutura química, propriedades e usos químicos do carboneto de silício
- 80 frases para o primeiro amor que nunca esquece »

