Como o modelo Brönsted-Lowry complementa o modelo de Arrhenius?
- 2606
- 644
- Shawn Leffler
 Brönsted e Lowry complementaram o modelo de Arrhenius, expandindo os conceitos de substâncias ácidas e substâncias base
Brönsted e Lowry complementaram o modelo de Arrhenius, expandindo os conceitos de substâncias ácidas e substâncias base O que são modelos Brönsted-Lowry e Arrhenius?
Tanto o modelo de Arrhenius quanto Brönsted-Lowry descrevem dois tipos de substâncias muito importantes: ácidos e bases. Ambos participam de processos biológicos e fazem parte de medicamentos e compostos úteis.
Os ácidos têm um sabor azedo característico, enquanto as bases sentem sabonetes ao toque. Por um longo tempo, essas diferenças sensoriais foram aquelas que ajudaram a distingui-las, até o químico sueco Svante Arrhenius (1859-1927), no final do século XIX, estabeleceu quantitativamente a distinção.
O modelo Arrhenius-Base Arrhenius afirma que uma substância é:
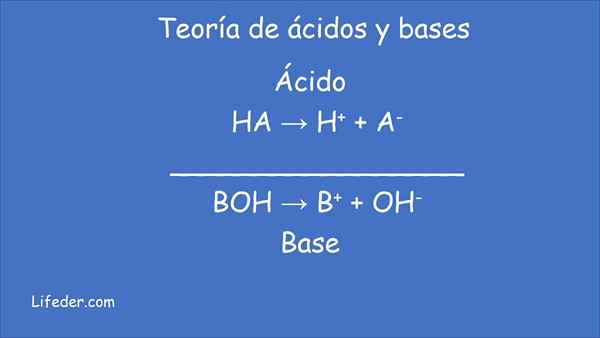
- Ácido, Se você liberar prótons (íons de hidrogênio H+) ou íons hidronio h3QUALQUER+ Em solução aquosa.
- Base, Ao produzir íons hidróxidos (oh-), também em solução aquosa.
Esta definição é limitada apenas a soluções aquosas. Portanto, ele não explica como outras substâncias também se comportam como ácidos ou bases, mesmo sem serem dissolvidos em água ou não contêm hidrogênio ou íons hidróxidos.
Portanto, dois químicos, um dinamarquês, chamados Johannes Brönsted (1879-1949) e outro inglês, Thomas Lowry (1874-1936), expandiu independentemente as definições de Arhenius, para incluir casos não contemplados por este.
De acordo com a nova teoria, a definição de ácidos e bases é a seguinte:
- Ácido É qualquer espécie química que gera prótons (íons de hidrogênio H+) para outra substância.
- Base, Espécies químicas que aceitam prótons (íons hidrogênio H+) de outra substância.
 O bicarbonato de refrigerante é uma base e vinagre, um ácido. Ao reagir, são produzidas bolhas de dióxido de carbono, um sal de acetato de sal e água e água. Fonte: Wikimedia Commons
O bicarbonato de refrigerante é uma base e vinagre, um ácido. Ao reagir, são produzidas bolhas de dióxido de carbono, um sal de acetato de sal e água e água. Fonte: Wikimedia Commons Modelo de Arrhenius
Em sua tese de doutorado, Svante Arrhenius elaborou uma teoria sobre o Dissociação eletrolítica. De acordo com isso, existem substâncias que exibem condutividade elétrica quando estão em uma solução aquosa, ou seja, eles conduzem eletricidade.
Pode atendê -lo: ácidos e bases na vida cotidiana: reações, usos, exemplosEssas substâncias são eletrólitos. Exemplo deles é um sal comum, ou cloreto de sódio, dissolvido em água, que produz íons (espécies químicas com carga líquida) na solução.
No caso do cloreto de sódio na água, a reação correspondente é:
NaCl → Na+ + Cl-
Da mesma forma, para uma base como o hidróxido de sódio NaOH, em solução aquosa, a dissociação eletrolítica é:
NaOH → Na+ + Oh-
E para um ácido, também em solução aquosa, como o ácido clorídrico HCL, você tem:
HCl → Cl- + H+
O comportamento dos eletrólitos em solução aquosa levou Arrhenius a classificar substâncias como ácido que, quando dissolvido na água, liberam prótons e como bases, para os quais os íons liberam oh-. Portanto, eles são chamados, respectivamente, ácidos e bases de Arrhenius.
A vantagem dessa teoria é revelada em reações de neutralização, nas quais um ácido e uma base base são combinados. No processo, os íons característicos de cada tipo de substância desaparecem, h+ Em ácidos e oh- Nas bases, que produzem água.
Por exemplo, a mistura de uma solução aquosa de ácido clorídrico HCL com um hidróxido de sódio NaOH é um exemplo típico de reação de neutralização:
Hcl + NaOH → NaCl + h2QUALQUER
A reação entre um ácido e uma base Baseius produz um sal mais água, originada pela reação entre os íons h+ e oh-.
Limitações do modelo de Arrhenius
O modelo Arhenius foi inovador por ser o primeiro a oferecer uma definição quantitativa de ácido e base.
Pode atendê -lo: mudanças físicasAnteriormente, a distinção entre um tipo de substância deve ser feita com a ajuda dos sentidos: se uma substância é amarga, como suco de limão ou vinagre, é um ácido; Se for escorregadio ou com sabão, é uma base.
Arrhenius estabeleceu que os ácidos contêm hidrogênio que, ao se dissolver na água, aumenta a concentração de íons de hidrogênio ou prótons de água pura. Por outro lado, dissolvendo uma base, a concentração de íons OH aumenta-.
No entanto, o modelo tem limitações importantes:
-O conceito de ácido e base é aplicado apenas em soluções aquosas, mas sabe -se que existem outras substâncias capazes de se comportar como uma ou outra, mesmo na ausência de água.
-Existem ácidos que não contêm hidrogênio (por exemplo, co2 Eu sou3) e bases sem íons hidróxido (como amônia).
-Na prática, íons de hidrogênio ou prótons, carregados positivamente, não permanecem livres na solução. Eles atraem eletricamente moléculas de água, que são polares, causando íons h hidrônicos3QUALQUER+.
O modelo de Brönsted-Lowry
As limitações ácidas-base de Arhenius tornaram necessário expandir os conceitos. Portanto, em 1923, Johannes Brönsted e Thomas Lowry concordaram, de forma independente e quase ao mesmo tempo, que o ácido ou o caráter básico de uma substância é dado por sua capacidade de ceder ou aceitar prótons.
Dessa maneira, as reações de neutralização consistem simplesmente na transferência de prótons entre ácido e base. O primeiro é capaz de doar prótons, e o segundo está pronto para aceitá -los.
Esquematicamente, a reação de neutralização seria assim:
Ácido1 + Base2 → ácido2 + Base1
Ácidos e bases de Brönsted-Lowry
Comparando a definição de ácido dado por cada modelo, conclui-se que os ácidos arhenius também são ácidos Brönsted-Lowry. Mas será lembrado que existem substâncias, como amônia, que se dissolvam em água se comportam como base, mesmo sem ter íons hidróxidos.
Pode atendê -lo: Hidróxido de Mercúrio: Estrutura, Propriedades, Usos, RiscosCom a definição de Brönsted-Lowry, o comportamento básico da amônia na água é explicado porque a molécula de amônia NH3 Aceitar um íon h+ de água, e isso se comporta como um ácido Brönsted-Lowry.
A reação de amônia e água, em solução aquosa, é:
NH3 + H2Ou ⇔ nh4+ + Oh-
A seta dupla significa que a reação é reversível.
Dessa forma, o modelo Brönsted-Lowry complementa o de Arhenius, incluindo casos que, originalmente, não contemplaram.
Substâncias anfotentas
A água se comporta como o ácido de Brönsted-Lowry quando reage com uma solução de amônia, mas também é capaz de se comportar como uma base de Brönsted-Lowry, como na próxima reação, entre ácido clorídrico e água:
HCl + H2O → h3QUALQUER+ + Cl-
Quando uma substância tem um comportamento duplo, isto é, pode ser ácido ou base de acordo com o composto com o qual reage, é chamado Anfothera.
Outras substâncias anfotentas, além da água, são o íon bicarbonato e os aminoácidos.
Referências
- Ácidos e bases. Recuperado de: FQ.Iespm.é.
- Atkins, p. (2007). Princípios da química. 3º. Edição. Editorial médico pan -American.
- Chang, R. (2013). Química. 11VA. Edição. McGraw Hill.
- Academia Khan. Ácidos e bases Bronsted-Lowry.
- Ripoll, e. Ácidos e bases. Projeto Descartes. Recuperado de: Projectodescartes.org.

