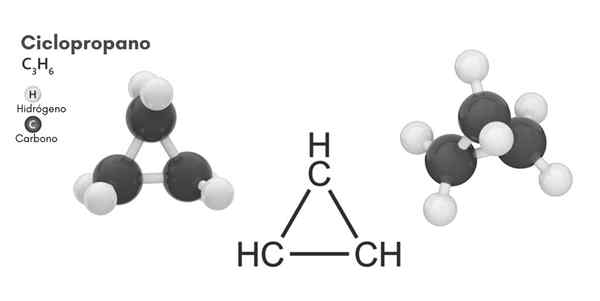
Cycopropan (C3H6)
- 2082
- 32
- Tim Mann
O que é ciclopropano?
Ele Ciclismo É uma molécula cíclica que tem a fórmula molecular C3H6, e isso consiste em três átomos de carbono unidos na forma de um anel. Na química, há uma família de hidrocarbonetos saturados que possuem um esqueleto formado por átomos de carbono unidos por ligações simples em forma de anel.
Esta família consiste em um número variado de moléculas (que diferem pelo comprimento de sua principal cadeia carbonatada) e são conhecidas por ter pontos de fusão e ebulição mais rápidos do que os de cadeias altas, além de maior reatividade do que estes.
Cycropotus foi descoberto em 1881 por um químico austríaco chamado August Freund, que estava determinado a saber qual era o elemento tóxico em etileno e que veio pensar que era o mesmo ciclopropano.
Mesmo assim, não foi até a década de 1930 que começou a ser produzido em nível industrial, quando descobriram seus usos como anestesia, porque antes desse momento eles não eram uma atração comercial.
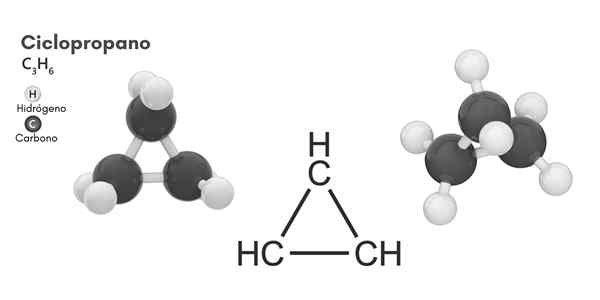
Estrutura química
 Estrutura molecular do ciclopropano
Estrutura molecular do ciclopropano Ciclismo, fórmula molecular C3H6, Consiste em três pequenos átomos de carbono que se ligam em uma configuração de modo que um anel se forma, deixando uma simetria molecular de D3h Em cada carbono da cadeia.
A estrutura desta molécula exige que os ângulos de ligação formados a partir de cerca de 60º, muito menos que os de 109,5º observados entre os híbridos SP átomos3, que é um ângulo mais estável termodinamicamente.
Isso leva ao anel que sofre de uma tensão estrutural mais significativa do que outras estruturas desse tipo, além de uma tensão de torção natural que ele tem pela conformação eclipsada de seus átomos de hidrogênio.
Pode atendê -lo: cinética enzimáticaPor esse mesmo motivo, as ligações formadas entre átomos de carbono nesta molécula são consideravelmente mais fracas do que em alcanes comuns.
De uma maneira peculiar e diferente de outros links, onde a proximidade entre duas moléculas simboliza maior energia de ligação, os vínculos entre os carbonos dessa molécula têm uma peculiaridade de ter um comprimento menor que os outros alcanes (devido à sua geometria) e no mesmo tempo eles são mais fracos que os sindicatos entre aqueles.
Além disso, o ciclopropano.
Propriedades de Ciclo -Own
Ponto de ebulição
Comparado ao outro cicloalcano mais comum, o ciclopropano.
Por outro lado, em comparação com o propano linear, o ciclopropano.
Ponto de fusão
O ponto de fusão do ciclopropano é menor que o dos outros cicloalcões, derretendo a uma temperatura de 128 ºC a menos que zero. Mesmo assim, não é o único cicloalcão que derrete a uma temperatura menor que zero, sendo capaz de observar esse fenômeno também no ciclobutano, ciclopentano e cicloheptano.
Assim, no caso de propano linear, derrete a uma temperatura inferior a 187 ºC abaixo de zero.
Densidade
Cycropopano tem a maior densidade entre os cicloalcânicos, sendo mais de duas vezes o ciclo comum mais denso (1.879 g/L para ciclopropano, superando o ciclodecano com 0,871).
Pode servir a você: óxido de alumínio: estrutura, propriedades, usos, nomenclaturaHá também uma densidade mais alta no ciclopropano do que em propano linear. A diferença nos pontos de ebulição e de fusão entre os alcanos lineares e de cicloalcanos é devida a grandes forças de Londres, que aumentam devido à forma do anel que permite uma maior área de contato entre átomos internos.
Reatividade
A reatividade do ciclopropano.
Graças a isso, o ciclopropano pode ser separado com mais facilidade e pode se comportar como alqueno em certas reações. De fato, a extrema reatividade das misturas de ciclopropano-oxigênio pode se tornar um perigo de explosão.
Usa/aplicações
O uso comercial do ciclopropano por excelência é como agente anestésico, estudando esta propriedade pela primeira vez em 1929.
Cyclo -nown é um poderoso agente anestésico de ação rápida, que não irrita o trato respiratório ou apresenta um mau cheiro. Foi usado por várias décadas, juntamente com o oxigênio para dormir pacientes durante intervenções cirúrgicas, mas os efeitos colaterais indesejados representados como "choque de ciclopropano" começaram a ser observados.
Juntamente com os custos de custo e alta inflamabilidade, estava passando por um processo de descarte e substituição por outros agentes anestésicos mais seguros.
Embora continuasse a fazer parte dos compostos usados na indução de anestesia, hoje não faz parte dos agentes usados em aplicações médicas.
Riscos
- O ciclopropano é um gás altamente inflamável, que produz gases tóxicos ao entrar em contato com uma chama. Além disso, pode reagir com agentes oxidantes, como peróxidos, peróxidos, permanganatos, nitratos e halogênios, causando incêndios e/ou explosões.
Pode atendê -lo: ácido clorogênico- Andar de bicicleta em níveis altos pode causar dores de cabeça, tontura, náusea, perda de coordenação, sentimento de desmaio e/ou desbotamento.
- Também pode gerar irregularidades na freqüência cardíaca ou arritmia, dificuldades respiratórias, coma e até morte.
- O ciclopropa liquefeito pode causar congelamento da pele devido à sua temperatura consideravelmente menor que zero.
- Sendo um gás em condições ambientais, esse composto pode facilmente entrar no corpo através do ar e também diminui o nível de oxigênio no ar.