Estrutura de ciclo -hexeno, propriedades, síntese e usos

- 4984
- 314
- Gilbert Franecki
Ele Ciclohexeno É um alceno ou olefina cíclica cuja fórmula molecular é c6H10. Consiste em um líquido incolor, insolúvel em água e miscível com muitos solventes orgânicos. É caracterizado por ser inflamável e, na natureza, geralmente é encontrado em Hulla Tar.
O ciclohexeno é sintetizado pela hidrogenação parcial do benzeno e pela desidratação do álcool ciclohexanol; isto é, uma maneira mais oxidada. Como outros cicloalquenos, experimenta adição eletrofílica e radicais livres; Por exemplo, reação de halogenação.
 Molécula de ciclo -hexeno. Fonte: Neurotoger.
Molécula de ciclo -hexeno. Fonte: Neurotoger. Esta cíclica (imagem superior) forma misturas aceotrópicas (não separáveis por destilação), com álcoois inferiores e ácido acético. Não é muito estável no armazenamento prolongado, pois se decompõe sob a ação da luz solar e da radiação ultravioleta.
O ciclohexeno é usado como solvente e, portanto, possui inúmeras aplicações, como: estabilizador de gasolina de alta octanagem e extração de óleo.
Mas o mais importante é que o ciclohexeno serve como uma matéria -prima intermediária e prima para obter numerosos compostos de grande utilidade, incluindo: ciclohexanona, ácido adipico, ácido maleico, ciclohexano, butino, ciclohexilcarboxílico, etc.
[TOC]
Estrutura do ciclo -hexeno
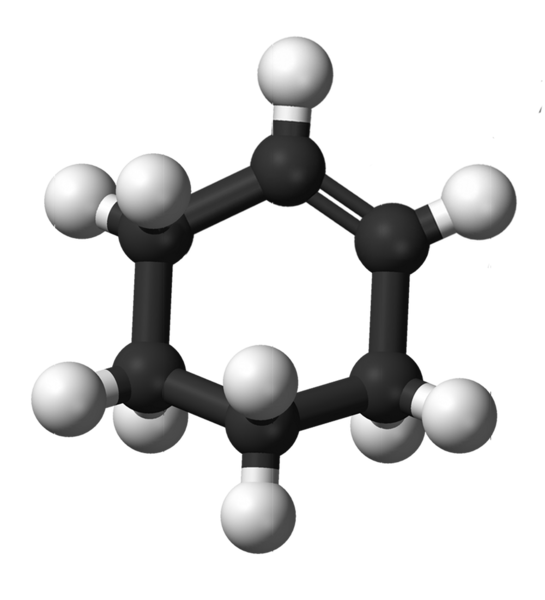 Estrutura do ciclo -hexeno. Fonte: Kemikungen [domínio público]
Estrutura do ciclo -hexeno. Fonte: Kemikungen [domínio público] A imagem superior mostra a estrutura do ciclohexeno com um modelo de esferas e barras. Você pode notar o anel de seis carbonos e a ligação dupla, ambos insatórios do composto. Nessa perspectiva, parece que o anel é plano; Mas não é nada.
Para começar, os carbonos de títulos duplos têm hibridação SP2, o que lhes dá uma geometria trigonal plana. Portanto, esses dois carbonos e aqueles adjacentes a eles são encontrados no mesmo plano; Enquanto os dois carbonos na extremidade oposta (para a ligação dupla) estão acima e sob o referido avião.
Pode atendê -lo: gravidade específicaA imagem inferior ilustra perfeitamente o recém -explicado.
 Vista frontal da estrutura do ciclohexeno. Fonte: Ben Mills.
Vista frontal da estrutura do ciclohexeno. Fonte: Ben Mills. Observe que a faixa preta é composta por quatro carbonos: os dois da ligação dupla e os outros adjacentes a eles. A perspectiva exposta é a que seria obtida se um espectador colocasse o olho na frente do link duplo. Pode -se ver que um carbono está de pé e sob este avião.
Como a molécula de ciclohexeno não é estática, os dois carbonos serão trocados: um cairá enquanto o outro se elevará acima do plano. Portanto, seria esperado que se comporte esta molécula.
Interações intermoleculares
Cyclohexen é um hidrocarboneto e, portanto, suas interações intermoleculares são baseadas nas forças de dispersão de Londres.
Isso ocorre porque a molécula é apolar, sem dipolo permanente, e seu peso molecular é o fator que mais contribui para mantê -lo coeso no líquido.
Da mesma forma, a ligação dupla aumenta o grau de interação, pois não pode se mover com a mesma flexibilidade que a dos outros carbonos, e isso favorece a interação entre moléculas vizinhas. É por esse motivo que o ciclohexeno tem um ponto de ebulição ligeiramente maior (83ºC) do que o do ciclohexano (81ºC).
Propriedades
Nomes químicos
Ciclohexeno, tetra -hidribenzeno.
Peso molecular
82.146 g/mol.
Aspecto físico
Líquido incolor.
Cheiro
Cheiro doce.
Ponto de ebulição
83 ºC a 760 mmHg.
Ponto de fusão
-103,5 ºC.
ponto de ignição
-7 ºC (copo fechado).
Solubilidade em água
Praticamente insolúvel (213 mg/l).
Solubilidade em solventes orgânicos
Miscível com etanol, benzeno, tetracloreto de carbono, éter de óleo e acetona. Espera -se que seja capaz de dissolver os compostos apolares, como alguns dos alões de carvão.
Pode atendê -lo: Torio: estrutura, propriedades, obtenção, usosDensidade
0,810 g/cm3 a 20ºC.
Densidade de vapor
2,8 (com relação aérea tomada como igual a 1).
Pressão de vapor
89 mmhg a 25ºC.
Auto-direção
244 ºC.
Decomposição
Ele se decompõe na presença de sais de urânio, sob a ação da luz solar e da radiação ultravioleta.
Gosma
0,625 mPascal a 25 ° C.
Calor de combustão
3.751,7 kJ/mol a 25 ºC.
Calor de vaporização
30,46 kJ/mol a 25 ºC.
Tensão superficial
26,26 mn/m.
Polimerização
Pode polimerizar sob certas condições.
Limiar de cheiro
0,6 mg/m3.
Índice de refração
1.4465 a 20 ºC.
ph
7-8 a 20ºC.
Estabilidade
O ciclohexeno não é muito estável durante o armazenamento de longo prazo. A exposição à luz e ao ar pode causar produção de peróxidos. Também é incompatível com fortes agentes oxidantes.
Reações
-Os cicloalques experimentam principalmente reações de adição, os radicais eletrofílicos e livres.
-Reage com o bromo para a forma 1.2-dibromociclohexan.
-Oxida rapidamente na presença de permanganato de potássio (KMNO4).
-É capaz de produzir um epóxido (óxido de ciclohexeno) na presença de ácido peroxibenzóico.
Síntese
O ciclohexeno é produzido pela Catálise de Ciclohexanol ácida:
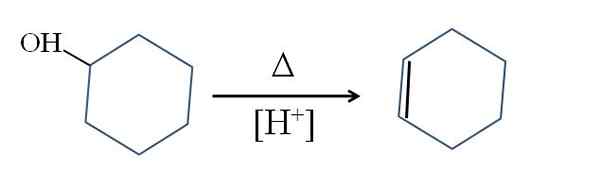 Desidratação do ciclohexanol. Fonte: Gabriel Bolívar.
Desidratação do ciclohexanol. Fonte: Gabriel Bolívar. O símbolo Δ representa o calor necessário para promover a saída do grupo OH como uma molécula de água em um meio ácido (-OH2+).
O ciclo -hexeno também ocorre por hidrogenação parcial do benzeno; Ou seja, duas de suas ligações duplas adicionam uma molécula de hidrogênio:
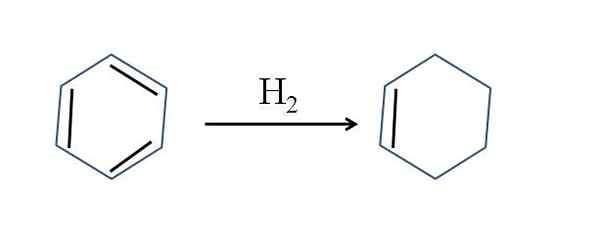 Hidrogenação parcial do benzeno. Fonte: Gabriel Bolívar.
Hidrogenação parcial do benzeno. Fonte: Gabriel Bolívar. Embora a reação pareça simples, requer grande h2 e catalisadores.
Formulários
-Tem utilidade como solvente orgânico. Além disso, é uma matéria -prima para a produção de ácido adipico, aldeído adipico, ácido maleico, ciclohexano e ácido ciclohexilcarboxílico.
Pode atendê -lo: radioatividade-É usado na produção de cloreto de ciclohexana, composto usado como intermediário da preparação de produtos farmacêuticos e um aditivo de fricção.
-O ciclohexeno também é usado na síntese de ciclohexanona, matéria -prima para a produção de medicamentos, pesticidas, perfumes e corantes.
-O ciclohexeno intervém na síntese do aminociclohexanol, um composto usado como surfactante e emulsificante.
-Além disso, o ciclohexeno pode ser usado para preparação no laboratório Butadieno. Este último composto é usado na fabricação de borracha sintética, na elaboração de pneus de carro, e também é usada na elaboração de plásticos acrílicos.
-O ciclohexeno é matéria -prima para síntese de lisina, fenol, resina de policiloolefina e aditivos de borracha.
-É usado como um estabilizador de gasolinas de alta octana.
-Intervém na síntese de revestimentos à prova d'água, filmes resistentes a rachaduras e pastas de ligação para revestimentos.
Riscos
O ciclohexeno não é um composto muito tóxico, mas pode causar contato com uma vermelhidão da pele e olhos. Sua inalação pode produzir tosse e sonolência. Além disso, sua ingestão pode causar sonolência, dificuldade em respirar e náusea.
O ciclo -hexeno é pouco absorvido no trato gastrointestinal, portanto, efeitos sistêmicos graves não são esperados devido à sua ingestão. A complicação máxima é sua aspiração pelo sistema respiratório, que pode produzir pneumonia química.
Referências
- Joseph f. Chiang e Simon Harvey Bauer. (1968). Estrutura molecular do ciclohexeno. J. SOU. Chem. Soc. 1969, 91, 8, 1898-1901.
- Karry Barnes. (2019). Ciclohexeno: perigos, síntese e estrutura. Estudar. Recuperado de: estudo.com
- Morrison, r. T. E boyd, r. N. (1987). Quimica Organica. (5ta Edição.). Editorial Addison-Wesley Iberoamericana.
- PubChem. (2019). Ciclohexeno. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Livro químico. (2019). Ciclohexeno. Recuperado de: ChemicalBook.com
- Rede de dados de toxicologia. (2017). Ciclohexeno. Toxnet. Recuperado de: toxnet.Nlm.NIH.Gov
- Quimioxi. (s.F.). A fórmula estrutural para o ciclohexeno é. Recuperado de: quimioxi.com

