Estrutura ciclohexana, usa, conformações
- 1970
- 21
- Conrad Schmidt
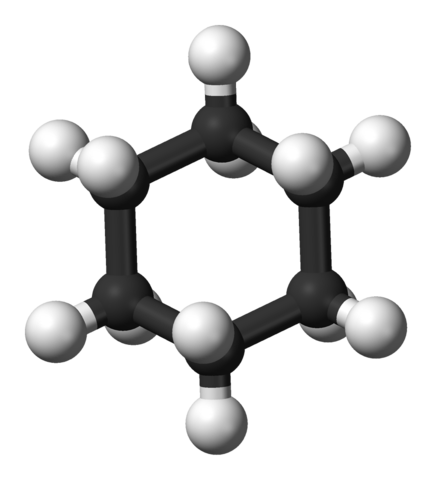
Ele Ciclohexano É um ciclo relativamente estável com a fórmula molecular C6H12. É um líquido incolor e inflamável que tem um cheiro de solvente suave, mas que pode ser penetrante em impurezas.
Tem uma densidade de 0,779 g/cm3; Ferva a 80,7 ° C; e congela a 6,4 ° C. É considerado insolúvel na água, pois sua solubilidade pode ser apenas 50 ppm (aprox.) à temperatura ambiente. No entanto, é facilmente misturado com álcool, éter, clorofórmio, benzeno e acetona.
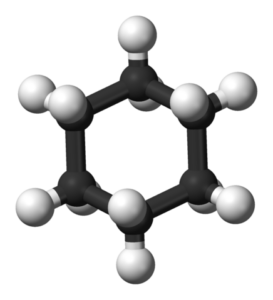 Modelo 3D da molécula de ciclo -hexano. Jynto e Ben Mills / Domínio Público
Modelo 3D da molécula de ciclo -hexano. Jynto e Ben Mills / Domínio Público Os sistemas de anel cychaxan são mais comuns entre as moléculas orgânicas da natureza do que as de outros ciclocas. Isso pode ser devido à sua estabilidade e à seletividade oferecida por suas conformações bem estabelecidas.
De fato, carboidratos, esteróides, produtos vegetais, pesticidas e muitos outros compostos importantes contêm anéis semelhantes aos da ciclohexana, cujas conformações são de grande importância para sua reatividade.
[TOC]
Estrutura
A ciclohexana é um hidrocarboneto alicíclico de seis membros. Há principalmente uma conformação na qual todas as ligações C-H nos átomos de carbono vizinhos são escalonados, com ângulos diédricos iguais a 60 °.
Porque tem o menor ângulo e tensão da torção. Isso também faz o ciclohexano.
Posições de substituintes
Existem dois tipos de posições para substituintes no anel ciclohexano: posições axiais e posições equatoriais. Os links equatoriais C-H são encontrados em uma banda ao redor do Equador do anel.
Por sua vez, cada átomo de carbono tem um hidrogênio axial que é perpendicular ao plano do anel e paralelo ao seu eixo. Os hidrogênios axiais alternam para cima e para baixo; Cada átomo de carbono tem uma posição axial e equatorial; E cada lado do anel tem três posições axiais e três equatoriais em um arranjo alternativo.
Pode atendê -lo: carbonato de sódio (Na2CO3)Modelos de estudo
Cyclohexan é melhor estudar um modelo molecular físico ou com um programa de modelagem molecular. Quando qualquer um desses modelos é usado, é possível observar facilmente as relações de torção e a orientação dos átomos de equador e hidrogênio axial.
No entanto, a disposição dos átomos de hidrogênio também pode ser analisada em uma projeção de Newman ao observar qualquer par de links c-c paralelos.
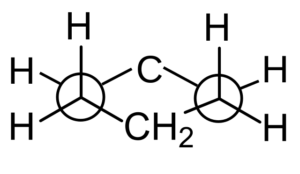 Projeção de Newman da Cychaxan. Durfo / cc0
Projeção de Newman da Cychaxan. Durfo / cc0 Conformações
A ciclohexana pode ocorrer em duas conformações que são internovertíveis: barco e cadeira. No entanto, o último é a conformação mais estável, pois não há ângulo ou tensão torcional na estrutura da ciclohexana; Mais de 99% das moléculas estão em uma conformação de cadeira a qualquer momento.
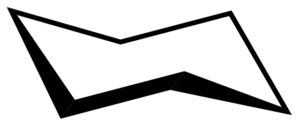 Conformação da cadeira de cychaxan. Chem Sim 2001 / Domínio Público
Conformação da cadeira de cychaxan. Chem Sim 2001 / Domínio Público Conformação da cadeira
Em uma conformação de cadeira, todos os ângulos de ligação C-C são 109,5 °, o que os libera da tensão angular. Como os links C-C são perfeitamente escalonados, a conformação da cadeira também está livre de tensão torcional. Além disso, os átomos de hidrogênio nos cantos opostos do anel ciclohexano são separados ao máximo.
Formação de barco
A conformação da cadeira pode assumir outra forma chamada formação de barco. Isso ocorre como resultado de rotações parciais em ligações c-c simples do anel. Essa conformação também não tem tensão angular, mas tem tensão de torção.
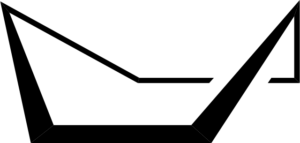 Conformação do barco ciclohexana. Keministi / domínio público
Conformação do barco ciclohexana. Keministi / domínio público Quando você vê um modelo de conformação do barco, nos eixos de ligação C-C ao longo de cada lado, verifica-se que as ligações C-H nesses átomos de carbono são eclipsados, produzindo tensão torcional.
Pode atendê -lo: derivados de benzenoAlém disso, dois dos átomos de hidrogênio estão próximos um do outro para gerar forças de repulsa de van der Waals.
Trapaceiro
Se a conformação do barco for flexionada, a conformação do barco torto que pode aliviar parte da tensão torcional e também reduzir as interações entre átomos de hidrogênio é obtido.
No entanto, a estabilidade obtida por flexão é insuficiente para tornar a conformação do barco torto mais estável do que a conformação da cadeira.
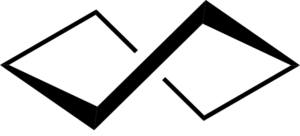 Conformação de barco de capool de ciclohexana. Keministi / CC0
Conformação de barco de capool de ciclohexana. Keministi / CC0 Formulários
Fabricação de nylon
Quase todo o ciclohexano que ocorre comercialmente (mais de 98%) é amplamente utilizado como matéria -prima na produção industrial de precursores de nylon: ácido adipico (60%), caprolactâmico e hexametilendiamina. 75% da caprolactama produzida em todo o mundo é usada para a fabricação de nylon 6.
 Guitarra com cordas de nylon. Fonte: pexels.com
Guitarra com cordas de nylon. Fonte: pexels.com Fabricação de outros compostos
No entanto, a ciclohexana também é usada na fabricação de benzeno, cloreto de ciclohexil, nitrocilohexano, ciclohexanol e ciclohexanona; na fabricação de combustível sólido; em formulações fungicidas; e na recristalização industrial de esteróides.
Aplicações minoritárias
Uma fração muito pequena do ciclo produzido é usada como solvente não polar para a indústria química e diluente em reações poliméricas. Também pode ser usado como removedor de tinta e verniz; na extração de óleos essenciais; e substitutos de vidro.
Devido às suas propriedades químicas e conformacionais únicas, o ciclohexano também é usado em laboratórios químicos analíticos para determinações de peso molecular e como padrão.
Fabricação
Processo tradicional
A ciclohexana está presente em petróleo bruto em concentrações que variam entre 0.1 e 1.0%. Portanto, costumava ser produzido tradicionalmente pela destilação fracionada da gasolina, na qual um concentrado de 85% de ciclohexano foi obtido por supurafloridade.
Pode atendê -lo: átomo de carbono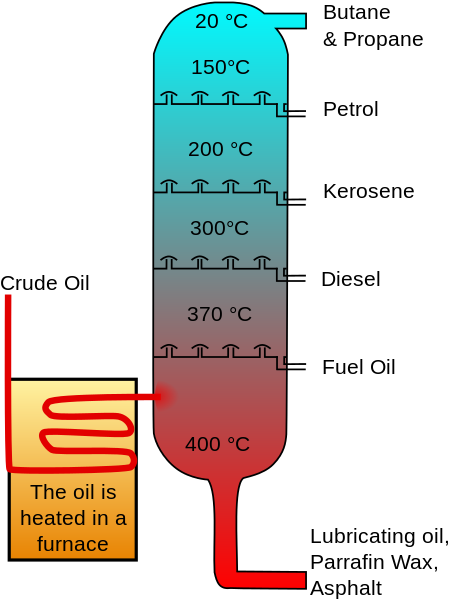 Destilação fracionada de óleo. Brude_oil_distilation-fr.SVG: Imagem Original: Psaria, Theresa Knott; Imagem Vectorielle: Rogilberterivative Work: Utain ()/CC BY-SA (http: // criativecommons.Org/licenças/BY-SA/3.0/)
Destilação fracionada de óleo. Brude_oil_distilation-fr.SVG: Imagem Original: Psaria, Theresa Knott; Imagem Vectorielle: Rogilberterivative Work: Utain ()/CC BY-SA (http: // criativecommons.Org/licenças/BY-SA/3.0/) Esse concentrado foi vendido, pois a purificação adicional necessária para realizar um processo de isomerização de pentans, rachaduras de calor para eliminar hidrocarbonetos de cadeia aberta e tratamento de ácido sulfúrico para remover compostos aromáticos.
Grande parte da dificuldade de obter ciclohexano com maior pureza foi devido ao grande número de componentes de óleo com pontos de ebulição semelhantes.
Processo de alta eficiência
Atualmente, o ciclohexano ocorre em escala industrial, reagindo benzeno com hidrogênio (hidrogenação catalítica) devido à simplicidade do processo e sua alta eficiência.
Esta reação pode ser realizada usando métodos de fase líquida ou vapor na presença de um catalisador altamente disperso ou em um leito catalítico fixo. Vários processos foram desenvolvidos nos quais níquel, platina ou paládio são usados como catalisador.
A maioria das plantas de ciclo -hexano usa o gás reformador produzido por benzeno e grandes quantidades de hidrogênio por -produtos como matéria -prima para produção de ciclohexano.
Como os custos de hidrogênio e benzeno são críticos para a fabricação de ciclohexano de maneira lucrativa, as plantas geralmente estão localizadas perto de grandes refinarias, onde estão disponíveis matérias -primas de baixo custo.
Referências
- Campbell, m. eu. (2014). Ciclo -hexano. Enciclopédia de química industrial de Ullmann (7º ed.). Nova York: John Wiley & Sons.
- McMurry, J. (2011). Fundamentos da química orgânica (7º ed.). Belmont: Brooks/Cole.
- Centro Nacional de Informações sobre Biotecnologia. (2020) Banco de dados PubChem. Ciclohexano, CID = 8078. Bethesda: Biblioteca Nacional de Medicina. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Ouellette, r. J., & Rawn, J. D. (2014). Química Orgânica - Estrutura, Mecanismo e Síntese. San Diego: Elsevier.
- Petrucci, r. H., Herring, f. G., Bissonnette, c., & Maduro, j. D. (2017). Química geral: princípios e aplicações modernas (11º ed.). Nova York: Pearson.
- Salomonos, t. C., Fryhle, c. B., & Snyder, S. PARA. (2016). Química Orgânica (12º ed.). Hoboken: John Wiley & Sons.
- Wade, l. G. (2013). Química orgânica (8ª ed.). Nova Iorque. Pearson.

