Calorimetria que estudos e aplicações
- 5144
- 963
- Conrad Schmidt
O calorimetria É uma técnica que determina as alterações no conteúdo calórico de um sistema associado a um processo químico ou físico. É baseado na medição das mudanças de temperatura quando um sistema absorve ou emite calor. O calorímetro é o equipamento usado nas reações em que uma troca térmica está envolvida.
O conhecido como "Coffee Cup" é a forma mais simples desse tipo de dispositivo. Através de seu uso, a quantidade de calor envolvida nas reações feitas sob pressão constante em uma solução aquosa é medida. Uma xícara de café do tipo consiste em um recipiente de poliestireno, que é colocado em um copo.
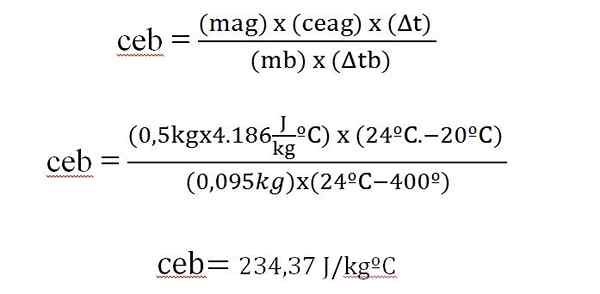
A água é colocada no recipiente de poliestireno, equipado com uma tampa do mesmo material que lhe confere um certo grau de isolamento térmico. Além disso, o contêiner possui um termômetro e um agitador mecânico.
Neste calorímetro, a quantidade de calor absorvida ou emite é medida, dependendo de a reação ser endotérmica ou exotérmica, quando uma reação ocorre em uma solução aquosa. O sistema para estudar é constituído por reagentes e produtos.
[TOC]
Que estuda calorimetria?
A calorimetria estuda a relação que a energia térmica associada a uma reação química tem e como é usada para determinar variáveis do mesmo. Suas aplicações em campos de pesquisa justificam o escopo desses métodos.
Capacidade calórica de um calorímetro
Essa capacidade é calculada dividindo a quantidade de calor que absorve o calorímetro entre a variação da temperatura. Esta variação é o produto do calor emitido em uma reação exotérmica, que é igual a:
Quantidade de calor que absorve o calorímetro + quantidade de calor que absorve a solução
A variação pode ser determinada adicionando uma quantidade conhecida de calor, medindo a mudança de temperatura. Para essa determinação da capacidade calórica, o ácido benzóico é geralmente usado, uma vez que seu calor de combustão é conhecido (3.227 kJ/mol).
A capacidade calórica também pode ser determinada pelo vício em calor por meio de uma corrente elétrica.
Pode servir a você: fosfato de alumínio (alpo4): estrutura, propriedades, obtenção, usosExemplo do uso do calorímetro para calcular o calor específico
Uma barra de 95 g de um metal é aquecida a 400 ° C, tomando imediatamente um calorímetro com 500 g de água, inicialmente a 20 ºC. A temperatura final do sistema é de 24 ºC. Calcule o calor específico do metal.
ΔQ = m x CE X Δt
Nesta expressão:
ΔQ = variação de carga.
M = massa.
CE = calor específico.
Δt = variação de temperatura.
O calor ganho pela água é igual ao calor destacado da barra de metal.
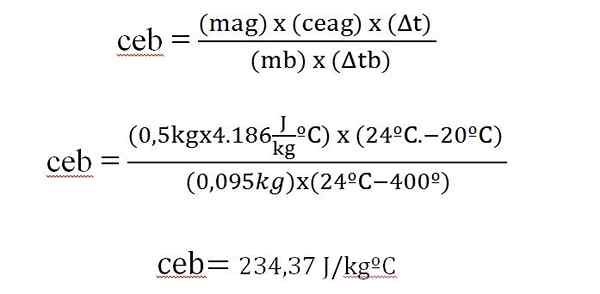
Este valor se parece com aquele que aparece em uma tabela de calor específica para prata (234 j/kg ºC).
Portanto, uma das aplicações da calorimetria é a cooperação para a identificação de materiais.
Bomba calorimétrica
Consiste em um recipiente de aço, conhecido como bomba, resistente às altas pressões que podem se originar durante as reações que ocorrem neste recipiente; Este contêiner está conectado a um circuito de ignição para iniciar as reações.
A bomba está imersa em um recipiente grande com água, cuja função é absorver o calor gerado na bomba durante as reações, fazendo a variação da temperatura. O recipiente de água está equipado com um termômetro e um agitador mecânico.
As mudanças de energia são medidas em volume e temperatura constantes, portanto, nenhum trabalho é feito nas reações que ocorrem na bomba.
ΔE = q
ΔE é a variação da energia interna na reação e que o calor gerado neste.
Tipos de calorímetro
Canto do título isotérmico (CTI)
O calorímetro tem duas células: em uma a amostra é colocada e, no outro, a referência, a água é geralmente colocada.
A diferença de temperatura gerada entre as células - devido à reação que ocorre na célula de amostra - é anulada por um sistema de feedback que injeta calor para corresponder às temperaturas das células.
Este tipo de calorímetro permite seguir a interação entre macromoléculas e seus ligantes.
Pode servir a você: álcool isoamílico: estrutura, propriedades, usos e riscosCalorímetro de varredura diferencial
Este calorímetro possui duas células, assim como o CTI, mas possui um dispositivo que permite determinar os fluxos de temperatura e calor associados a alterações em um material, dependendo do tempo.
Esta técnica fornece informações sobre a dobra de proteínas e ácidos nucleicos, bem como sua estabilização.
Formulários

-A calorimetria permite determinar a troca de calor que ocorre em uma reação química, permitindo assim claramente entender o mecanismo disso.
-Ao determinar o calor específico de um material, a calorimetria fornece dados que ajudam sua identificação.
-Como existe uma proporcionalidade direta entre a mudança de calor de uma reação e a concentração de reagentes, juntamente com o fato de que a calorimetria não requer amostras limitadas, essa técnica pode ser usada para determinar a concentração de substâncias presentes em matrizes complexas.
-No campo da engenharia química, a calorimetria é usada no processo de segurança, bem como em diferentes campos da otimização, reação química e na unidade de operação.
Usos da calorimetria de titulação isotérmica
-Colabora no estabelecimento do mecanismo de ação enzimática, bem como em sua cinética. Essa técnica pode medir reações entre moléculas, determinando a afinidade de link, estequiometria, entalpia e entropia em solução sem a necessidade de marcadores.
-Avalie a interação de nanopartículas com proteínas e, juntamente com outros métodos analíticos, é uma ferramenta importante para registrar as mudanças conformacionais das proteínas.
-Tem aplicação em conservação de alimentos e colheitas.
-Em relação à conservação de alimentos, pode determinar sua deterioração e tempo da vida nas prateleiras (atividade microbiológica). Ele pode comparar a eficiência de diferentes métodos de conservação de alimentos e é capaz de determinar a dose ideal de conservantes, bem como a degradação no controle de embalagens.
-Quanto às culturas vegetais, você pode estudar a germinação de sementes. Estando na água e na presença de oxigênio, eles liberam calor que pode ser medido com um calorímetro isotérmico. Examine a idade e o armazenamento inadequado das sementes e estude sua taxa de crescimento contra variações de temperatura, pH ou produtos químicos diferentes.
Pode atendê -lo: microscópio simples-Finalmente, você pode medir a atividade biológica dos solos. Além disso, você pode detectar doenças.
Usa calorimetria de varredura diferencial
-Juntamente com a calorimetria isotérmica, permitiu o estudo da interação de proteínas com seus ligantes, o Al, a dobra de proteínas e o mecanismo de sua estabilização.
-Você pode medir diretamente o calor liberado ou absorvido durante um evento de ligação molecular.
-A calorimetria diferencial de varredura é uma ferramenta termodinâmica para o estabelecimento direto de coleta de energia calórica que ocorre em uma amostra. Isso permite analisar os fatores envolvidos na estabilidade da molécula de proteína.
-Também estuda a termodinâmica da transição de ácidos nucleicos dobráveis. A técnica permite a determinação da estabilidade oxidativa do ácido linoléico isolado e acoplado para outros lipídios.
-A técnica é aplicada na quantificação de usos farmacêuticos e na caracterização térmica de transportadores lipídicos nanoestruturados.
Referências
- Whitten, k., Davis, r., Peck, m. e Stanley, G. Química. (2008). 8ª ed. Cengage Learning Edit.
- Rehak, n. N. e jovem, D. S. (1978). Aplicações prospectivas de calorimetria no laboratório clínico. Clin. Chem. 24 (8): 1414-1419.
- Stossel, f. (1997). Aplicações de calorimetria de reação em engenharia química. J. Eles. Anal. 49 (3): 1677-1688.
- Weber, p. C. e Salemme, f. R. (2003). Aplicações de métodos calorimétricos para descoberta de medicamentos e estudo de interações proteicas. Curr. Opinião. Estrutura. Biol. 13 (1): 115-121.
- Gill, p., Moghadem, t. e Ranjbar, B. (2010). Técnicas calimétricas de varredura diferencial: aplicações em biologia e nanociência. J. Biol. Tecnologia.21 (4): 167-193.
- Omanovic-Miklicanin, e., Manfield, i. e Wilkins, T. (2017). Aplicações de calorimetria de titulação isotérmica na avaliação de interações proteicas-nanopartículas. J. Eles. Anal. 127: 605-613.
- Consórcio da faculdade comunitária para credenciais de biociência. (7 de julho de 2014). Calímetro de xícara de café. [Figura]. Recuperado em 7 de junho de 2018, de: Commons.Wikimedia.org

