Estrutura de boro -hidreto de sódio (NABH4), propriedades, usos

- 4212
- 1319
- Conrad Schmidt
Ele boro de sódio É um sólido inorgânico cuja fórmula química é NABH4. Pode ser considerado representativo dos boro -hidruros alcalinos e é o mais comum deles. É um sólido branco cristalino.
Após contato com a água, o NABH4 pode gerar calor e hidrogênio H2 que é combustível, por isso deve ser tratado com cautela. Para a facilidade com que ele pode gerar íons hidretos h-, O boro de sódio é um composto moderadamente reduzido, por isso é amplamente utilizado em reações químicas para esse fim.
 Boro -hidreto de sódio, NABH4, sólido. Ondřej Mangl [Domínio Público]. Fonte: Wikimedia Commons.
Boro -hidreto de sódio, NABH4, sólido. Ondřej Mangl [Domínio Público]. Fonte: Wikimedia Commons. Sua propriedade redutora também é usada na indústria de papel, pois permite melhorar as características de brilho e estabilidade da polpa e papel ao agir contra a oxidação da celulose, componente principal do papel.
Como na presença de água pode formar facilmente hidrogênio, a possibilidade de usá -lo como fonte de hidrogênio reversível nas células de combustível também foi investigada.
Ele tem outros usos com base em sua propriedade redutora, como na indústria farmacêutica.
[TOC]
Estrutura
O boro de sódio é um composto iônico. É formado por ânion de boro -hidreto [BH4]- juntamente com a cátion de sódio+.
O ânion [bh4]- É tetraédrico.
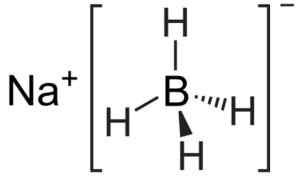 Estrutura de boro -hidreto de sódio. Kemikungen [domínio público]. Fonte: Wikimedia Commons.
Estrutura de boro -hidreto de sódio. Kemikungen [domínio público]. Fonte: Wikimedia Commons. Sua estrutura de Lewis é a seguinte:
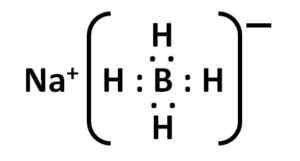 Estrutura eletrônica de Nabh Lewis4. Autor: Marilú Stea.
Estrutura eletrônica de Nabh Lewis4. Autor: Marilú Stea. Nomenclatura
-Boro de sódio
-Tetra -hidroato de sódio
-Tetra -hidrororato de sódio
Propriedades físicas
Estado físico
Sólido branco cristalino.
Peso molecular
37,84 g/mol
Temperatura de auto -dirigir
∼ 220 ºC
temperatura de decomposição
> 250 ºC
Densidade
1.074 g/cm3 A 20 ºC
Pode atendê -lo: Reagente Grignard: Preparação, Aplicações, ExemplosSolubilidade
O nabh4 É bastante solúvel em água (55 g/100ml a 25 ° C), onde hidrolisam parcialmente. É solúvel em tetra -hidrofurano (THF) e é insolúvel em dietyl éter.
Propriedades quimicas
O boro de sódio é dissolvido em água, onde sofre uma decomposição ou hidrólise inicial que torna a solução básica, o que evita a hidrólise subsequente.
[BH4]- + H2O → B (OH)3 + H2↑ + Oh-
Isso é explicado porque [bh4]- interagir com h+ De água, onde h+ Pegue um hidreto h anion- Para formar h2. Pode -se dizer que o BH3 compete com h+ Para o hidreto H-.
Em hidrólise média ácida, está completa devido à abundância de íons h+.
O nabh4 É estável no ar seco. Não é volátil.
Devido ao seu teor de íons hidretos, o boro de sódio é um composto redutor. Permite reduzir o grupo carbonil c = o um c-oh, isto é, compostos carbonila para os álcoois.
O nabh4 Por si só, não reduz as ligações duplas c = c, nem mesmo os conjugados com grupos carbonil -C = c -c (= O)-.
No entanto, ao entrar em contato com ácidos protônicos (como HCl) ou ácidos de Lewis (como BCL3 ou alcl3) Diborano B é formado2H6. E se essa reação for realizada na presença de compostos orgânicos com ligações duplas c = c o diborano B2H6 Realiza a hidrobacioná.
Na presença de catalisadores apropriados e condições específicas, o boro de sódio pode reduzir vários tipos de grupos funcionais.
Riscos
O calor da reação de hidrólise na água é suficiente para ligar o hidrogênio que é formado nele. Portanto, é importante ter cuidado ao manipulá -lo.
O nabh4 Está facilmente ligado e é facilmente queimado.
Obtenção
A típica reação de preparação do NABH4 É através do hidreto de sódio nah e b (OCH3)3 a uma temperatura de cerca de 250 ºC:
Pode atendê -lo: eletrólise de água4 Nah + B (OCH3)3 → Nabh4 + 3 Naoch3
Formulários
Em reações químicas de redução
Por ser uma fonte de sones h-, O nabh4 É um composto redutor e é usado para preparar outros compostos químicos. Para fazer isso, é usado em solventes polares apratóticos, ou seja, sem h prótons+, como dimetilsulfóxido, hexametilfosforais e dimetiloformamida.
É usado como um agente redutor nas reações químicas orgânicas e inorgânicas.
Permite reduzir aldeídos a álcoois primários e cetonas para álcoois secundários.
Também reduz halogenetos de alquil para hidrocarbonetos como o iododano para Dean.
Se agir sozinho, ao fazer a redução não afeta outros grupos funcionais, como éster, ácido carboxílico, nitrila e sulfona.
Sua propriedade de não reduzir as ligações duplas c = c, nem mesmo os conjugados com grupos carbonil -C = c-c (= o)-, permite que você prepare álcoois insaturados -C = c-ch2-Oh.
Para reduzir os compostos aromáticos, nitrados para suas anilinas correspondentes requer a presença de catalisadores como cloreto de cobalto ou lata. Reduza os dissulfetos para os tiíolos.
Na presença de condições apropriadas e catalisadores, ele permite reduzir os ácidos carboxílicos, ésteres, em meio a nitrilas, imina, epóxidos e até ligações duplas e triplas.
Em h2 Em células de combustível
O nabh4 Pode ser transformado em uma célula de combustível.
O nabh4 Na presença de uma solução alcalina de KOH ou NaOH, é hidrolisado e produz hidrogênio H2 que pode ser usado como combustível em uma bateria de combustível de eletrólito polimérico.
Também foi investigado como material h para o armazenamento de H de H2 reversivelmente.
As nanopartículas NABH são sintetizadas4 e estabilizar com um surfactante. Depois de um tratamento com NICL2 É formada uma camada ou revestimento de proteção que regula a liberação de h2 completamente reversivelmente.
Pode atendê -lo: nitrato de prata (AGNO3): estrutura, propriedades, usos, toxicidadeEste novo material nanométrico permitiria o uso de H2 como um combustível limpo e renovável produzido.
 Veículo que trabalha com célula de combustível de hidrogênio. Dr. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons.
Veículo que trabalha com célula de combustível de hidrogênio. Dr. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikimedia Commons. Na indústria de celulose e papel
O boro de sódio é usado para melhorar o brilho e outras propriedades físicas de polpa e papel.
A degradação da matriz celulósica do artigo ocorre através de processos complexos que envolvem oxidação. Os grupos hidroxila oxidam carbonil e carboxil, isso leva à descoloração do papel e a diminuição das propriedades físicas.
Ao tratar a polpa ou papel com NABH4, Isso reduz aldeídos e cetonas a grupos -OH sem afetar grupos carboxílicos ácidos, melhorando a estabilidade e o brilho dos valores maiores que as iniciais.
 O nabh4 permite melhorar o brilho do papel. Autor: RawPixel. Fonte: Pixabay.
O nabh4 permite melhorar o brilho do papel. Autor: RawPixel. Fonte: Pixabay. Em vários usos
El borohidruro de sodio se emplea para tratar aguas de desecho, como agente mejorador del sabor en la industria de alimentos y bebidas, como agente de recubrimiento y para el tratamiento de superficies, en la producción de tabaco, en la industria farmacéutica, de textiles y de couro.
Referências
- Cristão, m.eu. e Aguey-Zinsou, K.-F. (2012). Estratégia Core-Shell, levando a alta capacidade de armazenamento de hidrogênio reversível para NABH4. ACS Nano 2012, 6, 9, 7739-7751. Recuperado de bares.ACS.org.
- Nora de Souza, M.V. e Alves v., T.R. (2006). Metodologias recentes mediadas por boro -hidreto de sódio na redução de diferentes classes de compostos. Aplicativo. Organometal. Chem. 2006; 20: 798-810. Recuperado da biblioteca online.Wiley.com.
- Imamoto, t. (1991). Redução. Boro-hidreto de sódio. Na compreensão da síntese orgânica. Recuperado de cientedirect.com.
- Tang, l.C. (1986) Estabilização do papel através do tratamento de boro -hidreto de sódio. Em materiais históricos têxteis e de papel. Capítulo 24. Páginas 427-441. Avanços na química, volume 212. Recuperado de bares.ACS.org.
- Algodão, f. Albert e Wilkinson, Geoffrey. (1980). Química inorgânica avançada. Quarta edição. John Wiley & Sons.
- Morrison, Robert Thornton; e Boyd, Robert Neilson. 1992. Química orgânica. Prentice-Hall. ISBN 81-203-0765-8.
- OU.S. Biblioteca Nacional de Medicina. (2019). Boro-hidreto de sódio. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov.
- « Características e exemplos do fenômeno social
- Cloreto de cobalto (cocl2 (estrutura, nomenclatura, propriedades »

