Azul de bromotimol

- 4811
- 486
- Melvin Mueller
 Bromotimol Blue é um indicador de pH. Fonte: Wikimedia Commons
Bromotimol Blue é um indicador de pH. Fonte: Wikimedia Commons O que é azul de bromotimol?
Ele Azul de bromotimol É um derivado de trifenilmetano que serve como um indicador de pH. Um indicador é um corante orgânico cuja cor depende da concentração do íon h3QUALQUER+ ou do pH médio. Devido à cor que exibe, o indicador pode indicar a acidez ou alcalinidade da solução.
O Bromotimol Blue tem uma escala de indicação ativa entre um pH 6.0 e 7.6. Para um pH do meio menor que 6.5 (ácido) manifesta uma coloração amarela. Quando o pH médio varia entre 6.5 e 7.6 (neutro), adquire uma coloração verde. Um pH maior que 7.6 Sua cor é azul (básica).
Esse recurso oferece uma ótima utilidade, pois pode ser usada em uma escala de pH próxima à neutralidade, precisamente onde ocorrem processos fisiológicos.
A ionização azul de bromotimol em solução aquosa pode ser esquematizada da seguinte forma:
Hin (amarelo) +h₂o em- (cor azul) + h3QUALQUER+
Quando o indicador é protonado (Hin) adquire uma coloração amarela; Enquanto o indicador está desprotegido (em-) Coloração é azul.
Estrutura química
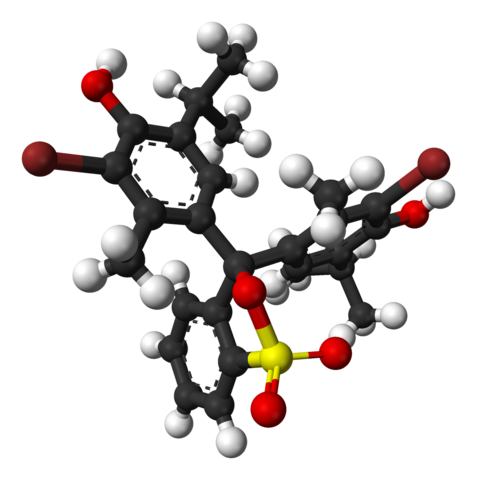 Estrutura química do bromotimol azul. Fonte: Wikimedia Commons
Estrutura química do bromotimol azul. Fonte: Wikimedia Commons Na imagem superior, a estrutura do azul de bromotimol é representada com um modelo de barra e esferas para um pH menor que 7.1. Barras marrons correspondem a átomos de bromo, dois no total.
Cada um dos três anéis aromáticos compõe, ao lado dos grupos metil, CH3, E térmico, o grupo Timol e, tendo ligado um BR, a partir daí, a razão é chamada de 'bromotimol'.
Pode atendê -lo: hidróxidosNa parte inferior, o grupo sulfonato é mostrado, r-so3-, Com esferas vermelhas e um amarelo. Este grupo pode ser ligado através de um átomo ou carbono central que se junta aos três anéis aromáticos.
Mudanças de pH
Essa estrutura molecular, embora não mude radicalmente com pH ácido ou básico, altera seus estados eletrônicos, refletidos por mudanças de cores de soluções.
Abaixo do pH 7, o indicador é amarelo e adota a estrutura da imagem, mas se o pH se tornar básico, os grupos -oh são infelizes e uma ligação dupla pode ser formada C = O.
Como resultado, o sistema conjugado da molécula (o de todas as suas ligações ressonantes duplas) muda o suficiente para que os elétrons não absorvam mais os mesmos fótons, e a solução se torna de amarelo para azul.
Se, por outro lado, o pH estiver bem abaixo de 7, a cor do indicador muda de amarelo para vermelho. Aqui a mudança no sistema conjugado é devido à protonação dos grupos -oh a -oh2+. -
Em meio ácido e básico, a molécula perde a estabilidade, absorvendo fótons menores para permitir transições eletrônicas responsáveis pelas cores percebidas por espectadores.
A cor verde observada na imagem principal é devido ao seguinte: quando o pH às 7 se aproxima.1, uma pequena porção de moléculas perde prótons, dizendo adeus a uma cor azul que, misturando com amarelo, dá a cor verde.
Propriedades dBlueotimol azul
Nome químico
Bromotimol azul ou 3.3'-dibromotimolsulfonafet.
Fórmula molecular
C27H28Br2QUALQUER5S.
Peso molecular
624.384 g/mol.
Aspecto físico
Poeira de cor sólida variando entre rosa e roxo.
Pode atendê -lo: butanal: estrutura, propriedades, usos e riscosCaracterística química
Atua como um ácido fraco em solução. Quando é protonado em um meio ácido, adquire uma cor amarela, um pH neutro é verde e quando é desagradável em um pH alcalino, é azul.
Constante de dissociação iônica (ka)
7.9 x 10-8.
Intervalo de indicação ativa
Ph 6.0 a 7.6. Isso se deve à presença de átomos de bromo que atuam extraindo elétrons e dois grupos de doadores de elétrons moderados (substituintes de alquil).
Densidade
1.25 g/cm3.
Ponto de fusão
202 ° C (396 ° F).
Ponto de ebulição
184.9 ° C.
Solubilidade
Dificilmente é solúvel em água e petróleo. Também é pouco solúvel em solventes não polares, como benzeno, tolueno e xileno, e praticamente insolúveis em éter de petróleo. É solúvel em soluções aquosas de álcalis e álcool.
Estabilidade
É estável à temperatura ambiente e incompatível com fortes agentes oxidantes.
Absorção leve
A forma protonada tem sua absorção máxima em um comprimento de onda (λ) de 427 nm, transmitindo assim a luz amarela em soluções ácidas, e a forma desprotegida tem uma absorção máxima em um comprimento de onda (λ) de 602 nm, transmitindo uma luz de azul claro para PH alcalino.
Usos e aplicações
Em estudos metabólicos
O azul de bromotimol é usado em numerosos processos nos quais o dióxido de carbono (CO₂) é produzido, com a conseqüente geração de ácido carbônico (H2Co3), que acidifica o meio, que é evidenciado por uma mudança na coloração de Bromotimol Blue.
Se uma pessoa estiver realizando um exercício físico e está conectado a um tubo que, por sua vez, está relacionado a um recipiente com uma solução de azul de bromotimol, o fenômeno a seguir será observado: como conseqüência do aumento da atividade física e do Metabolismo, um aumento na produção de CO₂ ocorrerá.
Pode atendê -lo: silício: história, propriedades, estrutura, obtenção, usosO CO₂ reagirá com água, produzindo ácido carbônico, H2Co3, que mais tarde se dissocia liberando o íon h+ e acidificando o meio. Isso resulta em Bromotimol Blue adquire uma coloração amarela, destacando a acidez do ambiente.
Em obstetrícia
O azul de bromotimol é usado em obstetrícia para mostrar uma ruptura precoce de membranas. O líquido amniótico normalmente tem um pH maior que 7.7, então o Bromotimol Blue vai colorir azul, quando entrar em contato com o líquido que escapa do Amnio.
O pH vaginal é geralmente ácido, portanto o azul de bromotimol tem uma coloração amarela. A mudança de sua cor para azul manifesta a presença de líquido amniótico na região vaginal.
Outros usos
O Bromotimol Blue também possui aplicação nos seguintes equipamentos e funções:
- Sensores ópticos
- Sistemas de detecção de combustão a gás
- Na elaboração de pinturas, brinquedos, produtos de limpeza, detergentes e têxteis
- Sensores de frescura de alimentos
- Como identificador de arroz fresco e rancid
- Na detecção de microorganismos.
Também é usado na análise de crescimento bacteriano, medicamentos psicoativos e materiais dentários.
Preparação
100 mg de azul de bromotimol são dissolvidos em 100 ml de álcool diluído e filtros, se necessário. Também está preparado da seguinte forma: 50 mg de azul de bromotimol são dissolvidos em uma mistura de 4 ml de hidróxido de sódio 0,02 N e 20 ml de álcool, completando 100 ml com água com água.
Referências
- Foist l. Bromotimol azul: definição, usos e fórmula. Estudo recuperado.com
- Indicador de pH azul de bromotimol, 1 oz. Recuperado da ScienceCompany.com
- Determinação espectrofotométrica de PK do indicador azul de bromotimol. Recuperado de FCH.UPOL.cz

