Alcenos
- 3238
- 1034
- Melvin Mueller
 Alcenos ou olefinas são hidrocarbonetos insaturados que têm pelo menos uma ligação dupla de carbono em sua estrutura
Alcenos ou olefinas são hidrocarbonetos insaturados que têm pelo menos uma ligação dupla de carbono em sua estrutura O que são alcenos?
O alcenos ou olefinas São hidrocarbonetos insaturados que têm pelo menos uma ligação dupla em sua estrutura. Eles são chamados olefinas devido à capacidade do eteno ou etileno de reagir com halogênios para produzir óleo ou óleo. Atualmente, o termo olefinas foi abandonado e esses compostos agora são chamados de alcenos.
As propriedades físicas dos alcenos são influenciadas por seu peso molecular, bem como por seu esqueleto carbonatado. Por exemplo, alcenos com 2 a 4 carbonos (buteno etene) são gases. Com 5 a 18 átomos de carbono na cadeia longa são líquidos. Enquanto alcenos com mais de 18 átomos de carbono são sólidos.
A presença de ligação dupla fornece grande reatividade, experimentando muitas reações químicas, como adição, eliminação, hidrogenação, hidratação e polimerização, que permitem gerar numerosos usos e aplicações.
Os alcenos são produzidos industrialmente pelo rachaduras térmicas de alto peso molecular (parafina ceras); Desidrogenação catalítica e cloração-desidrocloclinação.
Estrutura química dos alcenos
 Fonte: Self feito
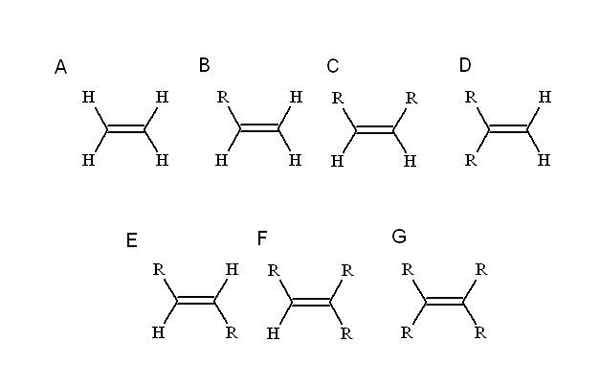
Fonte: Self feito Alcenos são caracterizados por ter um ou mais links duplos em sua estrutura. Isso é representado como C = C, com ambos os átomos de carbono uma hibridação SP2.
Portanto, a região da cadeia onde é a ligação dupla, ou insaturação, é plana. Também é Meritor para ressaltar que os dois carbonos podem ser vinculados a outros dois substituintes (ou grupos).
Quais substituintes? Qualquer pessoa que substitua um dos hidrogênios do alceno mais simples: etileno (ou eteno). Começando dele (A, Imagem Superior) R, que é um substituinte alquílico, ocupa o lugar de um dos quatro hidrogênios para causar um alceno mono-substituto (B).
Até agora, independentemente de qual hidrogênio seja substituído, a identidade de B não é alterada. Isso significa que não possui estereoisômeros, compostos com fórmulas químicas iguais, mas com uma disposição espacial diferente de seus átomos.
Pode atendê -lo: ponto de equivalênciaEstereoisômeros
Quando um segundo hidrogênio é substituído por outro r, como em C, agora os estereoisômeros C, D e E. Isso ocorre porque as orientações espaciais em relação a ambos podem variar, e para discernir uns aos outros, atribuições cis-trans ou e-z são usadas.
Em C, di-substituto alceno, os dois r podem ser correntes de qualquer comprimento ou algum heteroácomo. Um está na posição frontal em relação ao outro. Se os dois r consistirem no mesmo substituinte, F, por exemplo, então C é o estereoisômer-cis.
Em D, ambos os grupos R estão ainda mais próximos, pois estão ligados ao mesmo átomo de carbono. Este é o estereoisômer geminal, embora mais do que um estereoisômer, na verdade é uma ligação dupla terminal, ou seja, que está no final ou princípio de uma cadeia (por esse motivo que possui dois hidrogênios do outro carbono).
E em E, o mais estável dos estereoisômeros (ou isômeros geométricos), os dois grupos R são separados por uma distância maior, que atravessa a diagonal da ligação dupla. Por que é o mais estável? É porque, como a separação espacial entre eles é maior, então não há tensão irmã entre os dois.
Por outro lado, F e G são alcenos substituídos por Tri e Tetra. Novamente, eles não são capazes de gerar nenhum estereoisomer.
Propriedades físicas e químicas dos alcenos
Solubilidade
Eles são imiscíveis com água devido à sua baixa polaridade. Mas eles se dissolvem em solventes orgânicos.
Pontos de fusão em ºC
Etano -169, profeno -185, 1 -pentino -165, 1 -hepteno -119, 3 -octein
-101.9, 3 -None -81,4 e 5 -Dechenum -66,3.
Ponto de ebulição em º c
Etano -104, profeno -47, trans2buteno 0,9, cis2buteno 3,7, 1-penten 30, 1 hepteno 115, 3-OK 122, 3-noneno 147 e 5-Decend.
Pode atendê -lo: filtro de laboratório): características, funções, tiposO ponto de ebulição aumenta em relação direta com o número de carbonos alcenos. Por outro lado, quanto mais ramificada sua estrutura, a mais fraca são suas interações intermoleculares, o que se reflete na diminuição do ponto de ebulição ou de fusão.
Densidade
Etano 0,6128 mg/ml, propeno 0,6142 mg/ml e 1-buteno 0,6356 mg/ml, 1 pente 0,64 mg/ml e 1-hexenos 0,673.
Nos alcenos, a densidade máxima é de 0,80 mg/ml. Isto é, eles são menos densos que a água.
Polaridade
Depende da estrutura química, substituições e presença de outros grupos funcionais. Os alcenos têm dipmers, assim o isômero cis de 2-buteno.
Reatividade dos alcenos
Alcenos têm grande capacidade de reagir devido aos links duplos que eles têm. Entre as reações envolvidas estão: adição, eliminação, substituição, hidrogenação, hidratação e polimerização.
Reação de adição
H2C = ch2 + Cl2 => Clch2-Cclh2 (dicloreto de etileno)
Reação de hidrogenação
Ocorre em altas temperaturas e na presença de catalisadores adequados (PT, PD ou finamente divididos)
CH2= Cap2 + H2 => Cap3-CH3 (Etano)
Reação de hidratação
Reação que é a fonte de geração de álcool de derivados de petróleo:
H2C = ch2 + H2O => H3C-CH2Oh (álcool etílico)
Reações de polimerização
Etileno na presença de catalisadores, como testes de alumínio e polimeriza de tetracloreto de titânio em polietileno, que contém cerca de 800 átomos de carbono. Este tipo de polímero é chamado de polímero de adição.
Usos e aplicações de alcenos
Polímeros
- O polietileno de baixa densidade é usado na fabricação de sacolas, plásticos de estufa, embalagens, pratos, vasos, etc. Enquanto a alta densidade é mais rígida e resistente mecanicamente, usando na fabricação de caixas, móveis, protetores como capacetes e joelhos, brinquedos e paletes.
- Polipropileno, polímero de propileno, é usado na elaboração de recipientes, lençóis, equipamentos de laboratório, brinquedos, filmes de embalagem, filamentos de sogas, estofados e tapetes.
- O cloreto de polivinil (PVC) é um polímero de cloreto de vinil que é usado na fabricação de tubos, ladrilhos para pisos, canais, portas e quadros de janelas, etc.
- Polibutadieno, polímero de 1,3-butadieno, destina-se à fabricação de bandas de rolamentos, mangueiras e cintos de veículo, bem como para o revestimento de latas metálicas.
- Os copolímeros de etileno e propileno são usados na fabricação de mangueiras, corpo e partes do chassi para tecidos, etc.
Alcenos
- Eles são usados na obtenção de solventes como etileno glicol e dioxano. O etileno glicol é usado como um anticongelante em radiadores de carro.
- O etileno é um hormônio de plantas que controla seu crescimento, germinação de sementes e desenvolvimento de frutas. Portanto, é usado para induzir a maturação das bananas quando eles chegam ao seu destino.
- Eles são usados como matéria -prima para a fabricação de muitos compostos, como halogenetos de alquil, óxido de etileno e especialmente etanol. Eles também têm uso na indústria, cuidados pessoais e medicina.
- Eles são usados na obtenção e fabricação de lacas, detergentes, aldeídos e combustíveis. 1.3-butadieno é usado como matéria-prima na fabricação de borrachas sintéticas.
Referências
- Tarefa de Química. Propriedades físicas de alcenos. Retirado de: Assignação de Química.com
- Wikipedia. (2018). Alceno. Retirado de: em.Wikipedia.org
- Química Librettexts. Propriedades físicas de alcenos. Tirado de: química.Librettexts.org
- Whitten, Davis, Peck e Stanley. Química. (8ª ed.). Cengage Learning.
- Francis a. Tortoisshell. Quimica Organica. (Sexta edição., Página 194). Mc Graw Hill.
- Houchton Mifflin Harcourt. (2016). Alcenos: fórmulas moleculares e estruturais. Retirado de: CliffsNotes.com
- Chipera, Angie. (25 de abril de 2017). O que é uma olefina na química? Cienting. Retirado de: Cienting.com

