Estrutura de óxido cromo (III), nomenclatura, propriedades, usos

- 5119
- 1085
- Shawn Leffler
Ele Óxido cromo (III) O óxido crômico em U é um sólido verde inorgânico formado pela queima de metal de cromo (Cr) em oxigênio (ou2), deixando o cromo com o estado de oxidação 3+. Sua fórmula química é CR2QUALQUER3. Na natureza, é encontrado no mineral Eskolaíta. Depósitos naturais de óxido cromo (III) não são conhecidos.
Pode ser preparado, entre outras maneiras, aquecendo CR2QUALQUER3 hidratado (cr2QUALQUER3.NH2O) para remover completamente a água. Também é obtido como um produto da calcinação de óxido de cromo (VI) (CRO3).
 Pigmento de óxido cromo (III). FK1954 [domínio público]. Fonte: Wikipedia Commons
Pigmento de óxido cromo (III). FK1954 [domínio público]. Fonte: Wikipedia Commons No entanto, a melhor maneira de obtê -lo pura é pela decomposição do dicromato de amônio (NH4)2Cr2QUALQUER7 a 200 ºC. Industrialmente é produzido pela redução do dicromato de sódio (NA2Cr2QUALQUER7) sólido com enxofre.
Quando é finamente dividido, apresenta uma cor verde brilhante com nuances amareladas. Mas se as partículas são maiores, exibirá um corante azulado. O óxido crômico é o pigmento verde mais estável que é conhecido. Sua resistência térmica e química o torna um corante de cerâmica valioso.
É usado em revestimentos industriais, vernizes, na indústria da construção, em jóias, como coloração em cosméticos ou produtos farmacêuticos, entre outras aplicações.
[TOC]
Estrutura
Óxido de α-CR2QUALQUER3 Tem a estrutura do tipo Corindon. Seu sistema cristalino é romboônico hexagonal. É isomórfico com α-alumina e α-Fe2QUALQUER3.
O Eskolaíta, mineral natural do óxido cromo (III), apresenta a estrutura mostrada abaixo:
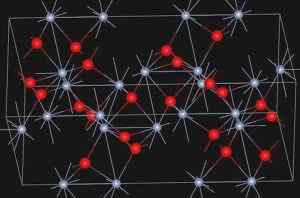 Estrutura cristalina do mineral de Eskolaíta. https: // upload.Wikimedia.Org/Wikipedia/Commons/E/EE/Eskolaite_structure.Jpg. Fonte: Wikipedia Commons
Estrutura cristalina do mineral de Eskolaíta. https: // upload.Wikimedia.Org/Wikipedia/Commons/E/EE/Eskolaite_structure.Jpg. Fonte: Wikipedia Commons Nomenclatura
- Óxido cromo (III).
- Óxido cromo verde.
- Trioxido de Dichroma.
- Cromium Seasquioxide.
- Cromia.
- Eskolaíta: Mineral de óxido cromo (III).
- Hidrato: cr2QUALQUER3.NH2Ou (onde n ≅ 2) é chamado de hidrato de óxido cromo (iii) ou verde guignet.
 Hidrato de óxido cromo (iii). C. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikipedia Commons
Hidrato de óxido cromo (iii). C. Oelen [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0)]. Fonte: Wikipedia Commons Propriedades
Estado físico
Sólido cristalino.
Dureza mohs
9 (seus cristais são extremamente difíceis).
Peso molecular
151,99 g/mol.
Pode atendê -lo: compostos quaternários: características, treinamento, exemplosPonto de fusão
Derrete a 2435 ºC, mas começa a evaporar para 2000 ºC, formando nuvens de fumaça verde.
Densidade
5,22 g/cm3
Solubilidade
Quando foi aquecido a altas temperaturas, é praticamente insolúvel em água (3 microgramas/L a 20ºC); insolúvel em álcoois e acetona; ligeiramente solúvel em ácidos e álcalis; Ssolúvel de ácido perclórico (HCLO4) para 70%, no qual se decompõe.
ph
6.
Índice de refração
2.551.
Outras propriedades
- Se estiver fortemente calculado, torna -se inerte em relação a ácidos e bases. Caso contrário, o cr2QUALQUER3 e sua forma hidratada CR2QUALQUER3.NH2O Eles são anfotéricos, facilmente se dissolvendo em ácido para dar aquáticos [cr (h2QUALQUER)6]3+, e em álcalis concentrados para formar "cromitos".
- Quando foi calcinado, é quimicamente resistente a ácidos, álcalis e altas temperaturas. É extremamente estável para assim2.
- Tem uma excelente resistência à luz porque seus cristais têm opacidade, alta atenuação UV e transparência para luz visível.
- É um material extremamente difícil, você pode arranhar quartzo, tapacio e zirconio.
- Seu hidrato cr2QUALQUER3.NH2Ou (onde n ≅ 2) não tem estabilidade térmica, sua hidratação limita sua aplicabilidade a menos de 260 ºC. Apresenta baixa capacidade de tingimento e nuances limitadas de nuances.
- Mas este hidrato tem uma tonalidade azul verde muito limpa e brilhante. É semi -transparente, apresenta baixa opacidade, excelente resistência à luz e resistência a álcalis.
- O cr2QUALQUER3 Não é classificado como material perigoso e é considerado um pó fino inerte. Não está sujeito a regulamentos internacionais de transporte.
- Não irrite a pele ou as membranas mucosas.
Formulários
Na indústria de cerâmica e vidro
Devido à sua alta resistência ao calor e à resistência química, o CR2QUALQUER3 Calcinado é usado como coloração para colorir ou pigmento vitrificável na fabricação de cerâmica, em esmaltes e misturas de porcelana para vidro.
Em revestimentos industriais
A cerâmica com óxido cromo (III) fornece excelente resistência contra a maioria dos ambientes corrosivos. Tudo isso através do mecanismo de exclusão do substrato circundante.
Por esse motivo, é usado em revestimentos para impedir a corrosão de muitos materiais, sendo aplicada por spray térmico (atomização ou orvalho quente).
Pode servir a você: Processo químico: princípios, tipos, exemplosTambém é usado como proteção contra desgaste abrasivo (quando a remoção do material é causada por partículas que se movem através de uma superfície).
Nesses casos, a aplicação de um revestimento de CR2QUALQUER3 Por deposição com plasma, gera alta resistência à abrasão.
Os dois casos anteriores têm utilidade, por exemplo, em motores turbinas turospaciais a gás.
Na indústria refratária
É usado em tijolos termicamente e quimicamente resistentes, materiais de revestimento e concreto refratário à base de alumina.
Em construção
Como é extremamente resistente a condições atmosféricas, luz e calor, é aplicado como um corante de rocha granulado para telhados de asfalto, cimento de concreto, revestimentos industriais de alta qualidade para exteriores, construções de aço e fachadas de revestimento (tintas emultáveis).
Como pigmento em aplicações variadas
Pode apoiar condições de vulcanização e não se degradar, por isso é usado na pigmentação de borracha.
Por serem não técnicos, é usado como pigmento para brinquedos, cosméticos (especialmente seu hidrato), plásticos, tintas de impressão, pinturas que entram em contato com alimentos e produtos farmacêuticos.
Na indústria de pigmentos, é usado como matéria -prima para produzir corantes penetrantes que contêm cromo e pigmentos com base em fases de óxidos metálicos mistos. Também é usado como coloração de pinturas para revestimento de bobina.
Seu hidrato tem uma transparência que permite a formulação de acabamentos policromáticos na indústria automotiva (acabamentos de carros metálicos).
Devido à sua característica única de refletir a radiação infravermelha (IR) semelhante à clorofila das plantas, sob luz infravermelha, parece folhagem. Por esse motivo, seu uso em pinturas de camuflagem ou revestimentos para aplicações militares é muito difundido.
Em jóias
É usado como um corante de jóias sintéticas. Quando CR é introduzido2QUALQUER3 como impureza na rede cristalina de α-al2QUALQUER3, Como no mineral rubi semiprecioso, a cor é vermelha em vez de verde.
Também é usado como agente de moagem e polido para alta dureza e propriedades abrasivas.
Em reações químicas
Apoiado em alumina (para2QUALQUER3) ou outros óxidos, é usado na química orgânica como catalisador, por exemplo, na hidrogenação de ésteres ou aldeídos para formar álcoois e em ciclização de hidrocarbonetos. Catalisa a reação do nitrogênio (n2) com hidrogênio (H2) Para formar amônia (NH3).
Pode servir a você: lítio: história, estrutura, propriedades, riscos e usosPara sua capacidade de redução de óxido, atuando em conjunto com o óxido de cromo (VI) desempenha um papel importante na desidrogenação de alcanos2 Para produzir ProPeno e isobuteno, já que o ciclo de reativação da desativação do catalisador é facilmente executável. Também é usado como catalisador em química inorgânica.
Na fabricação do Chrome
É usado na produção de aluminotérmica de metal cromado puro. Para fazer isso, deve ser aquecido a 1000 ºC para aumentar o tamanho do grão.
 Preparação de metais cromados por redução de aluminotérmica do óxido de cromo (III). Rando Tuikene [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikipedia Commons
Preparação de metais cromados por redução de aluminotérmica do óxido de cromo (III). Rando Tuikene [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]. Fonte: Wikipedia Commons Em materiais magnéticos
Ele foi adicionado em pequenas quantidades a materiais magnéticos de fitas de áudio e vídeo, ensinando um efeito auto -impressivo para as cabeças de som.
Inovações recentes
Foi obtido pigmentos que melhoraram a refletância de quase ir para as nanopartículas do DoPAR CR2QUALQUER3 com sais de elementos pertencentes ao grupo de terras raras, como o Lantano e o Praseodimio.
Aumentando a concentração desses elementos, a refletância solar do infravermelho próximo aumenta sem afetar a cor verde do porco criminoso2QUALQUER3.
Isso permite classificar CR2QUALQUER3 Doping como pigmento "frio", porque é adequado para controlar o acúmulo de calor.
Aplicado aos tetos, carros e estofados, entre outras aplicações, atinge a alta refletância da luz solar, o que nos permite reduzir significativamente o aumento do calor em ambientes.
Referências
- Algodão, f. Albert e Wilkinson, Geoffrey. (1980). Química inorgânica avançada. Quarta edição. John Wiley & Sons.
- Kirk-Othmer (1994). Enciclopédia de tecnologia química. Volume 19. Quarta edição. John Wiley & Sons.
- Enciclopédia de química industrial de Ullmann. (1990). QUINTA EDIÇÃO. Volume A7 e A20. Vch verlagsgellschaft mbh.
- Elementos americanos. (2019). Óxido de cromo (III). Recuperado dos americanos.com.
- Biblioteca Nacional de Medicina. (2019). Óxido de cromo (III). Recuperado de: pubchem.NCBI.Nlm.NIH.Gov.
- Dorfman, Mitchell R. (2012). Revestimentos de pulverização térmica. No Manual de Degradação Ambiental de Materiais. Capítulo 19. Recuperado de cientedirect.com.
- Takehira, k. et al. (2004). Co2 Desidrogenação do propano sobre o catalisador CR-MCM-41. Em estudos em ciência da superfície e catálise 153. Recuperado de cientedirect.com.
- Selvam Sangeetha et al. (2012). Pigmentos funcionais do óxido de nanopartículas de cromo (III). Corantes e pigmentos 94 (2012) 548-552. Recuperado de cientedirect.com.
- « História dos Emirados Árabes Unidos e Significado
- História, estrutura, propriedades, reações de titânio »

